Краткое описание амальгамы алюминия (Al/Hg). Видео инструкция
MacondoRCМы в телеграмм:
💡 Получите все необходимое вместе с Macondo. Стать членом сообщества можно через Macondo Synthesis или Macondo Shop (ссылка в шапке профиля).
У нас вы найдете:
🟢 Рецепты синтеза:🔹Мефедрон🔹A-PVP🔹МДМА🔹Амфетамин🔹Метамфетамин🔸Рецепты других веществ
🟠 Товары:🔹Реактивы и прекурсоры🔹Лабораторная посуда и оборудование🔹Конструкторы почтой🔹Конструкторы кладом
🟡 Услуги:🔹Консультации для новичков🔹Консультации для магазинов🔸 Справочник WIKI
🟣 Прочее:🔹 Правила🔹 Контакты
Введение
Здесь вы можете найти подробную информацию об амальгаме алюминия, инструкциях по ее производству из нитрата ртути или хлорида ртути. Имеется инструкция по синтезу нитрата ртути с видеоинструкциями. Синтез хлорида ртути не описан, поскольку его получают из нитрата ртути. Амальгама алюминия является одной из многих амальгам металлов, которые здесь не описаны, поскольку в синтетических путях незаконного производства наркотиков в основном используется только амальгама алюминия.
Что такое амальгама
Амальгама – это сплав ртути с другим металлом. Это может быть жидкость, мягкая паста или твердое вещество, в зависимости от содержания ртути. Эти сплавы образуются за счет металлических связей, при этом электростатическая сила притяжения электронов проводимости связывает все положительно заряженные ионы металлов вместе в структуру кристаллической решетки. Почти все металлы могут образовывать амальгамы с ртутью, за исключением железа, платины, вольфрама и тантала. Амальгамы серебра и ртути имеют важное значение в стоматологии, а амальгама золота и ртути используется при добыче золота из руды. В стоматологии используются сплавы ртути с такими металлами, как серебро, медь, индий, олово и цинк.


Алюминий может образовывать амальгаму в результате реакции с ртутью. Алюминиевую амальгаму можно получить либо путем измельчения алюминиевых таблеток или проволоки в ртути, либо путем взаимодействия алюминиевой проволоки или фольги с раствором хлорида сулемы/сульфата ртути. Эту амальгаму используют в качестве реагента для восстановления соединений, например, при восстановлении нитросоединений до аминов. Алюминий является конечным донором электронов, а ртуть служит посредником в переносе электронов. Сама реакция и отходы от нее содержат ртуть, поэтому необходимы особые меры безопасности и методы утилизации. В качестве более экологически чистой альтернативы для достижения того же синтетического результата часто можно использовать гидриды или другие восстановители. Другой экологически чистой альтернативой является сплав алюминия и галлия, который аналогичным образом делает алюминий более реакционноспособным, предотвращая образование оксидного слоя.

Алюминий на воздухе обычно защищен слоем собственного оксида толщиной с молекулу. Этот слой оксида алюминия служит защитным барьером для самого алюминия и предотвращает химические реакции с металлом. Контакт с ним Меркурия не причиняет вреда. Однако если какой-либо элементарный алюминий обнажится (даже в результате недавней царапины), ртуть может объединиться с ним, образуя амальгаму. Этот процесс может продолжаться далеко за пределами немедленно открытой металлической поверхности, потенциально вступая в реакцию с большой частью объемного алюминия, прежде чем он окончательно завершится.
Сообщается, что присутствие воды в растворе необходимо; богатая электронами амальгама окисляет алюминий и восстанавливает H+ из воды, образуя гидроксид алюминия (Al(OH)3) и газообразный водород (H2). Электроны алюминия восстанавливают ион ртути Hg2+ до металлической ртути. Металлическая ртуть может затем образовывать амальгаму с открытым металлическим алюминием. Затем амальгамированный алюминий окисляется водой, превращая алюминий в гидроксид алюминия и выделяя свободную металлическую ртуть. Образовавшаяся ртуть затем проходит через эти последние два этапа, пока запасы металлического алюминия не исчерпаются.
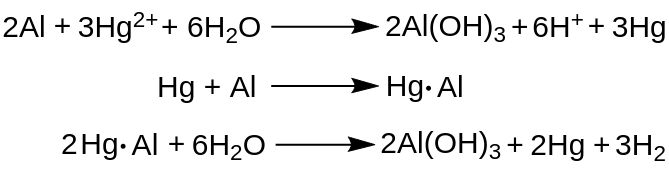
Способы приготовления
Амальгама Al/Hg из HgCl2 в растворе MeOH
Подготовьте двухлитровую плоскодонную трехгорлую колбу и заткните одно из горлышек. Установите обратный конденсатор в центральном отверстии. Аппарат помещали на мешалку/электрическую плитку. Разрежьте алюминиевую фольгу на квадраты размером примерно 1 дюйм.




Поместите порции по 5 г в небольшую кофемолку Braun и измельчите фольгу в течение 8–10 секунд. Фольга на самом деле не «измельчается», а скатывается в маленькие шарики. Это работает удивительно хорошо. Может показаться странным помещать фольгу в кофемолку, но это, без сомнения, прорыв в подготовке алюминия к Al/Hg. Затем 400 мг HgCl2 растворяли в 750 мл МеОН лабораторной чистоты. Когда МеОН был готов (вся HgCl2 растворилась), его также сливали в колбу и ставили конденсатор на место. Его перемешивали в течение 5-10 секунд каждую минуту или около того. Менее чем через 10 минут стало видно слабое пузырение, раствор стал серым, а алюминий стал заметно менее блестящим. Некоторые кусочки начали плавать. Когда амальгама готова, выделение газа прекращается.

Сухая амальгама Al/Hg из Hg(NO3) 2
Берем 14 г алюминиевой фольги и рвем ее руками на кусочки размером 2х2, 3х3 см. Обязательно рвите, а не разрезайте, чтобы увеличить площадь поверхности. Поместите в трехгорлую круглодонную колбу и полностью заполните фольгу водой.
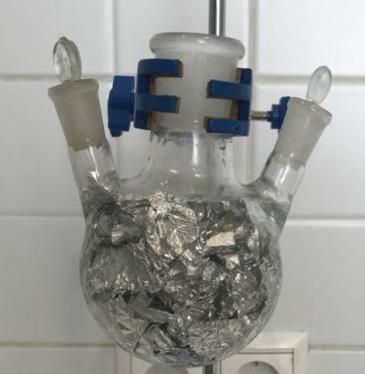
Теперь готовим ртутную соль. Берём из аптеки ртутный градусник, заворачиваем его в бумагу, надламываем у нижнего кончика. Вылейте всю ртуть (~1-2 г) в стакан, куда затем добавьте 4 мл азотной кислоты (70%). Не забывайте, что пары ртути опасны для здоровья! Чтобы инициировать реакцию, стакан нужно было нагреть примерно до 50 градусов, периодически помешивая. Вся ртуть растворилась примерно за 30 минут, и из стекла выделился оранжевый газ — оксид азота (IV). Уравнение реакции выглядит следующим образом:
Hg + 4HNO3 ----> Hg(NO3)2 + 2NO2 + 2H2O

Отнесите пипеткой 2 мл раствора и поместите его в круглодонную колбу с фольгой. Примерно через 5 минут фольга потеряла блеск, потускнела, а на дне колбы собрался небольшой слой серого осадка (гидроксида алюминия). Через 10-15 минут реакция прекращается, об этом можно судить по прекращению газовыделения.
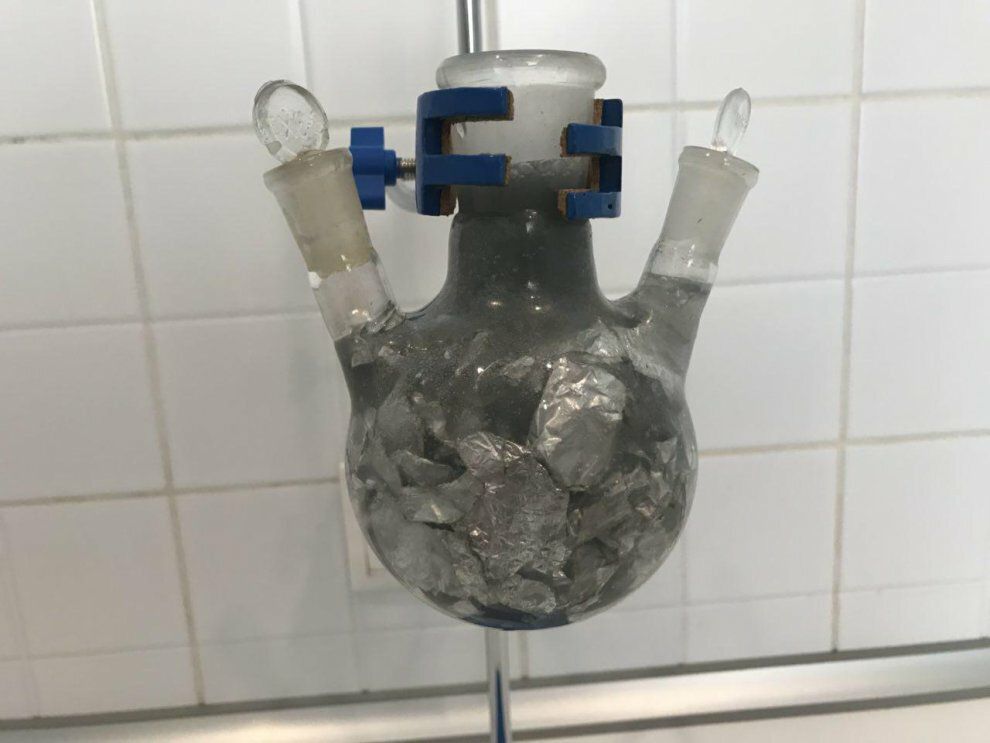
Сливаем жидкость и 3 раза промываем фольгу водой.

Уксусную эссенцию часто используют для получения водорода, но я «запускаю» реакцию получения водорода с помощью воды. Менее кислая среда, а это означает, что позже необходимо добавить меньше щелочи. Многие задаются вопросом: «Как убрать эту воду?» Воду никуда удалять не надо, она реагирует с алюминием и получается водород: 2Al+6H2O --->2Al(OH)3+ 3H2
Видео: Синтез алюминиевой амальгамы (Al/Hg) доступно на нашем портале в телеграмм
Al-амальгама (Al/Hg) широко используется в органических реакциях восстановления нитросоединений до аминов. Реакция восстановления представляет собой однореакторную экзотермическую реакцию Al/Hg с органическим ненасыщенным соединением. Алюминий, вода и ртуть выделяют в реакционную смесь газообразный водород (H2) и насыщают органические соединения. Вы можете встретить Al/Hg в самых популярных реакциях, таких как: синтез амфетамина из P2NP через Al/Hg (видео). Полный синтез МДМА из масла сассафраса, синтез и экстракция d-амфетамина (Набенхауэр, 1942) и так далее.