Афатиниб
HSO talks
Скачать шпаргалку по препарату можно здесь.
В 1970-х годах в изучении онкологических заболеваний произошел ряд революционных событий. В 1970 году ученые Питер Фогт и Питер Дюсберг открыли трансформирующий фактор вируса саркомы Рауса (позже названный v-src), вызывающего опухоли у цыплят.
Спустя 6 лет Гарольд Вармус и Майкл Бишоп обнаружили, что в клетках человека есть аналог вирусного src, клеточный ген с-src. Дальнейшие исследование привели к пониманию, что он кодирует тирозинкиназу, а ключевое различие между его вариациями в нормальных и опухолевых клетках определяется мутацией. После этого открытия ученые получили Нобелевскую премию, научный мир приблизился к пониманию генетической природы канцерогенеза, а протеинкиназы стали рассматриваться в качестве потенциальных мишеней для противоопухолевой терапии.
Наконец, в 1990-х годах был создан иматиниб (“Гливек”) - первый протеинкиназный ингибитор мутантных тирозинкиназ BCR-ABL. Это событие стало огромным рывком вперед, позволив успешно лечить ранее безнадежных больных с хроническим миелолейкозом (ХМЛ). Так появился новый класс препаратов, способных проникать в клетку и воздействовать на молекулы, участвующие в каскадах внутриклеточных биохимических реакций - протеинкиназные ингибиторы (tyrosine kinase inhibitors, или TKIs).
После одобрения FDA иматиниба в 2001 г. сначала для лечения ХМЛ, а затем и для других заболеваний, начался бум ингибиторов киназ, в результате которого были созданы препараты против множества релевантных киназ. И сегодня мы поговорим с вами об одном из них.
… а любители истории фармакологии могут погрузиться в мир открытий и развития фарминдустрии, прочитав замечательную статью от Биомолекулы.
Что за зверь?
Афатиниб (Гиотриф) - селективный и необратимый ингибитор протеинкиназы рецепторов второго поколения семейства ERBB (HER), мишенью которого является цитоплазматический домен всех HER-рецепторов (EGFR (ERBB), HER2 (ERBB2), ERBBЗ и ERBB4). Блокируя их фосфорилирование, афатиниб препятствует инициации клеточной пролиферации, адгезии и инвазии, а также активации антиапоптотических механизмов.
Если вы еще не прочитали прекрасный лонгрид, посвященный EGFR, советуем вам сделать это прямо сейчас :)
Что означают все эти буквы и как это действительно работает?
Начнем с того, что афатиниб относится к так называемым “малым молекулам”. Малые молекулы - это лекарства небольшой молекулярной массы (<900 атомных единиц массы — а.е.м.). У этих компактных ребят есть ряд преимуществ, которых не лишен и афатиниб. Например, способность проникать через мембрану и наводить порядок непосредственно внутри клетки.
Беспокойное семейство тирозинкиназных рецепторов ERBB (они же HER), в котором проживают интересующий нас сегодня EGFR, всем известный HER2, загадочные HER3 и HER4, иногда начинает проявлять нездоровую и чрезмерную активность. Это может провоцироваться разными причинами, но приводит всегда к одному - запуску машины канцерогенеза за счет усиленной пролиферации, инвазии, метастазирования, «поломки» механизмов апоптоза. Рано или поздно весь этот беспредел подкрепляется лекарственной устойчивостью.
Афатиниб блокирует цитоплазматическую (внутриклеточную) часть всех HER-рецепторов, выключая сигнальные пути и каскады “неправильных” биохимических реакций.
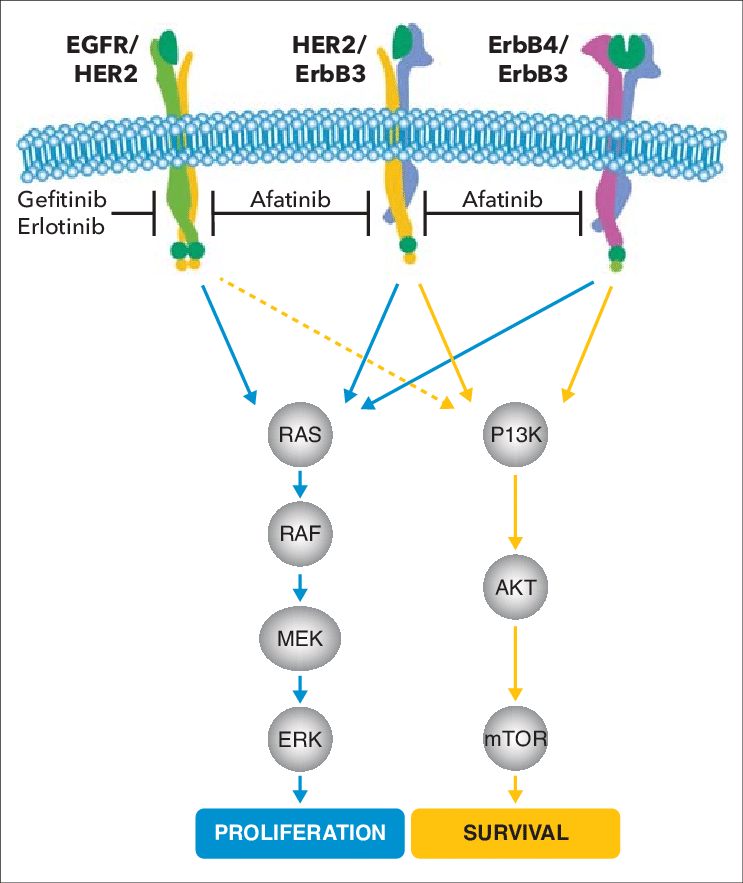
Преимущества афатиниба перед первым поколением ТКИ (эрлотинибом и гефитинибом):
- более мощное угнетение ферментативной активности за счет необратимого связывания с EGFR рецептором (правда, ценой большей токсичности);
- воздействие на дополнительные киназы (пан-HER ингибитор);
- проявляет активность к рецепторам, которые содержат мутацию Т790М (по-крайней мере, в лабораторных условиях);
- проникает через ГЭБ, обладая умеренной интракраниальной активностью, что позволяет рассматривать его как возможную опцию для пациентов с метастазами в головной мозг.
Как выглядит?
Круглые двояковыпуклые со скошенными краями таблетки, покрытые пленочной оболочкой от белого до синего цвета (в зависимости от дозировки), на поперечном разрезе ядро почти белого цвета, с гравировкой символа компании Берингер Ингельхайм на одной стороне и "Т20" (указание дозировки, может быть 30, 40 и 50) на другой стороне таблетки.
Еще одно важное преимущество малых молекул - лекарственная форма у большинства из них предназначается для приема внутрь, что более комфортно для пациентов, а значит повышает приверженность лечению. А это порой важнее, чем самое блестяще подобранное лечение.
Принимается препарат внутрь, натощак (не менее чем за 1 час до или спустя 2-3 часа после приема пищи). Стандартная доза в течение первых 3-х недель терапии - 40 мг/сут, при удовлетворительной переносимости (т.е. при отсутствии нежелательных явлений >1 степени) возможна эскалация дозы до 50 мг/сут.
При снижении СКФ до 15-29 мл/мин рекомендована дозировка 30 мг/сут.
Если прием целых таблеток невозможен, они могут быть диспергированы примерно в 100 мл негазированной питьевой воды. Таблетку следует поместить в воду, не разламывая, и периодически размешивать взвесь в течение 15 минут до тех пор, пока таблетка не распадется на очень мелкие частицы. Таким образом возможно введение через желудочный зонд.
Где его можно увидеть?
На данный момент препарат зарегистрирован для лечения в первой линии пациентов с метастатическим НМРЛ, опухоли которых имеют мутации EGFR, а также для пациентов с местно-распространенным и метастатическим плоскоклеточным НМРЛ, прогрессирующих после химиотерапии на основе препаратов платины.
В 2018 году FDA одобрило афатиниб для лечения рака легкого с редкими точечными мутаций EGFR (S768I, L861Q и G719X) на основании данных объединенного анализа трех клинических исследований (LUX-Lung 2, LUX-Lung 3 и LUX-Lung 6).
В рекомендациях RUSSCO также указано, что афатиниб может быть назначен во второй линии пациентам без мутации EGFR в случае, если имеются противопоказания для иммуно- и ХТ. Однако NCCN делать этого не рекомендует, так как афатиниб менее эффективен и безопасен по сравнению с другими доступными вариантами.
Зато NCCN предлагает комбинацию афатиниба с цетуксимабом как вариант для пациентов с прогрессированием после афатиниба, дакомитиниба, эрлотиниба (± бевацизумаб или рамуцирумаб) или гефитиниба и после химиотерапии. Стоит отметить, что основанием для этого послужило исследование Ib фазы, так что решайте сами, насколько эта комбинация может быть полезной для каждого конкретного пациента.
Афатиниб изучался при плоскоклеточном раке головы и шеи как возможная опция в качестве адъювантной терапии после ХЛТ (LUX-Head & Neck 2), а также во второй линии после прогрессирования на платиносодержащей ХТ (LUX-Head & Neck 3), однако увеличения общей выживаемости добиться не удалось. Тем не менее, в рекомендациях NCCN такая опция рассматривается для предлеченных пациентов.
Чем опасен?
Самой большой проблемой при применений этого класса препаратов остаются дерматологическая и гастроинтестинальная токсичность.
Частота возникновения акнеподобной сыпи при терапии афатинибом составляет 89%. Обычно сыпь возникает через 2–3 недели терапии, часто сопровождается зудом и жжением, реже болезненностью, гиперемией и отечностью.
Мы уже говорили о кожной токсичности EGFR-ингибиторов в предыдущем бестиарии, но на всякий случай оставим полезные материалы еще раз:
- Памятка для пациентов по уходу за кожей во время лечения.
- Гайд по сопроводительной терапии кожной токсичности от HSO talks
- Рекомендации от RUSSCO по профилактике и лечению дерматологической токсичности
Помимо кожных реакций и диареи очень часто (≥1/10 случаев) развиваются:
- тошнота, рвота, стоматит, снижение аппетита;
- паронихии;
- кровотечение из носа;
Часто ( ≥1/100, <1/10 случаев) возникают:
- пирексия, утомляемость, снижение веса;
- анемия, нейтропения.
- хейлит, диспепсия;
- конъюнктивит, сухость глаз;
- ладонно-подошвенный синдром (эритродизестезия), поражение ногтей;
- обезвоживание, гипокалиемия;
- нарушение функции почек/почечная недостаточность, цистит;
- повышение АЛТ, ACT, ЩФ общего билирубина;
- цитолитический гепатит, печеночная недостаточность;
- спазмы мышц, боль в спине;
- ринорея.
Более редко могут возникать проблемы с дыхательной системой (одышка, кашель, пневмонит, интерстициальная болезнь легких). Описаны также случаи кератита, панкреатита, перфорации ЖКТ, синдрома Стивенса-Джонсона, токсического эпидермального некролиза и сердечной недостаточности.
До начала лечения важно обратить внимание на такие детали анамнеза, как:
- кератит (в том числе язвенный);
- выраженная сухость глаз (и ношение контактных линз);
- интерстициальная болезнь легких;
- нарушения фракции выброса левого желудочка (не забываем про ЭхоКГ перед началом лечения);
- сопутствующие заболевания сердца;
- непереносимость галактозы, синдром нарушения всасывания галактозы/глюкозы или дефицит лактазы.
У женщин, у пациентов с более низкой массой тела и при сопутствующих нарушениях функции почек может повышаться риск развития нежелательных явлений, поэтому эта категория пациентов требует больше внимания и осторожности.
Что еще следует учесть:
- препарат обладает низким уровнем эметогенности (рвота возникает у 10-30% пациентов), однако четких рекомендаций по профилактике у нас нет - в рекомендациях RUSSCO указано, что при выборе режима противорвотной терапии для данной категории пациентов следует руководствоваться данными специальной литературы.
- профилактическое лечение диареи имеет важное значение, особенно в первые 6 недель терапии при появлении первых признаков - не забудьте обсудить алгоритм действий пациента при возникновении симптомов и ситуации, когда необходимо связаться с врачом.
Более подробно о диарее, вызванной противоопухолевым лечением, можно почитать здесь.
С кем не дружит этот зверь?
Применение препарата вместе с пищей приводит к существенному снижению концентрации афатиниба в крови.
Увеличивают концентрацию в крови (повышая токсичность):
- Препараты для лечения различных инфекций: ритонавир (и другие -виры), кетоконазол (кроме шампуня), итраконазол, эритромицин
- Препараты, применяемые при заболеваниях сердца - верапамил, хинидин, амиодарон,
- Циклоспорин А, такролимус*
Такролимус, кстати, является дерматотропным средством, антагонистом кальциневрина, который рекомендован RUSSCO в качестве сопроводительной терапии при сыпи всех степеней, выраженном отеке и зуде, возникающих на фоне анти-EGFR терапии. Несмотря на то, что системная абсорбция такролимуса при использовании в форме мази минимальна, взаимодействие с афатинибом не может быть полностью исключено у пациентов с обширными участками поражения и/или эритродермией.
Уменьшают концентрацию в крови (снижая эффективность):
- Препараты для лечения судорожных припадков - карбамазепин, фенитоин, фенобарбитал
- Зверобой продырявленный
- Рифамципин
Что делать? Если есть острая необходимость в совместном приеме - постараться применять их с как можно большим интервалом. Это подразумевает 6-ти (12-ти) часовой интервал от времени приема афатиниба для препаратов, применяемых один (два) раза в сутки. Помимо этого стоит рассмотреть возможность коррекции дозировки афатиниба (+/- 10 мг в зависимости от эффекта).
Когда нужно прекратить общение?
Препарат следует временно отменить в случае возникновения нежелательных явлений (по CTCAE):
- ≥ 3 степени тяжести ;
- затянувшихся на фоне адекватной сопроводительной терапии НЯ 2 степени тяжести (для диареи это более 48 часов, для сыпи - более 7 дней).
При возобновлении лечения после разрешения нежелательных явлений до 0-1 степени в таком случае требуется снижение дозы на 10 мг.
Закономерный вопрос, который возникает у пациента и врача - снижается ли эффективность препарата вместе с дозировкой? Имеющиеся данные позволяют сказать, что скорее всего нет. По крайней мере, адекватная доза помогает уменьшить токсичность, что повышает качество жизни пациента и уменьшает перерывы в лечении.
Окончательно отменить препарат следует в случае:
- развития серьезных нежелательных явлений 3-4 степени тяжести (поражения кожи, интерстициальное поражение легких, перфорация полого органа);
- тяжелой печеночной недостаточности;
- персистирующего язвенного кератита;
- если пациент не переносит дозу 20 мг/день.
Насколько драгоценен этот зверь?
- По данным Государственного реестра предельных отпускных цен стоимость афатиниба зависит от дозировки: от 53792.88 руб за 20 мг до 109449.14 руб за 50 мг.
- Дженериков нет.
Небольшой бонус:
- Доклад Саранцевой К.А. Тактика ведения больных с EGFR-позитивным НМРЛ
- Доклад Реутовой Е.В. Современная терапия EGFR-положительного НМРЛ
- Доклад Семеновой А.И. Коррекция дозы и эффективность терапии Гиотрифом
- Доклад Проценко С.А. Препараты для лечения НМРЛ EGFR+
- Конференция «Ингибиторы тирозинкиназы в лечении распространенного немелкоклеточного рака легкого»
- Optimizing outcomes in EGFR mutation-positive NSCLC: which tyrosine kinase inhibitor and when?
Материал подготовила: Элина Добросоцкая
Редактор: Ксения Петрова, Ирина Гридина
Иллюстрации: Настя Казанцева
Верстка: Мария Красавина