Un llamado a una investigación independiente sobre el origen del virus SARS-CoV-2
Neil L. Harrison y Jeffrey D. Sachs 18.5.2022
Desde la identificación del SARS-CoV-2 en Wuhan, China, en enero de 2020 ( 1 ), el origen del virus ha sido tema de intenso debate científico y especulación pública. Las dos hipótesis principales son que el virus surgió de la exposición humana a un animal infectado [“zoonosis” ( 2 )] o que surgió en un incidente relacionado con la investigación ( 3). La investigación sobre el origen del virus se ha visto dificultada por la falta de evidencia clave desde los primeros días del brote; no hay duda de que una mayor transparencia por parte de las autoridades chinas sería de gran ayuda. Sin embargo, argumentamos aquí que hay mucha información importante que se puede obtener de las instituciones de investigación con sede en los EE. UU., información que aún no está disponible para un escrutinio independiente, transparente y científico.

Los datos disponibles dentro de los Estados Unidos incluirían explícitamente, entre otros, secuencias virales recopiladas y conservadas como parte del proyecto PREDICT y otros programas financiados, así como datos de secuenciación y cuadernos de laboratorio de laboratorios estadounidenses. Hacemos un llamado a las agencias científicas del gobierno de EE. UU., en particular a los NIH, para que apoyen una investigación completa, independiente y transparente sobre los orígenes del SARS-CoV-2. Esto debería tener lugar, por ejemplo, dentro de una investigación bipartidista del Congreso basada en la ciencia y estrictamente enfocada con plenos poderes de investigación, que podría hacer preguntas importantes, pero evitar cazas de brujas equivocadas gobernadas más por la política que por la ciencia.
Investigaciones esenciales de EE. UU.
En 2021, el presidente Joe Biden ( 4 ) encargó a la comunidad de inteligencia estadounidense (CI) que investigara el origen del virus. En su declaración pública resumida, el IC escribe que “todas las agencias evalúan que dos hipótesis son plausibles: la exposición natural a un animal infectado y un incidente relacionado con el laboratorio” ( 4). El IC escribe además que "lo más probable es que se necesite la cooperación de China para llegar a una evaluación concluyente de los orígenes de COVID-19 [enfermedad por coronavirus 2019]". Por supuesto, dicha cooperación está altamente justificada y debe ser buscada por el gobierno de los EE. UU. y la comunidad científica de los EE. UU. Sin embargo, como se describe a continuación, se podría aprender mucho investigando el trabajo apoyado y basado en los EE. UU. que estaba en marcha en colaboración con instituciones con sede en Wuhan, incluido el Instituto de Virología de Wuhan (WIV), China. Todavía no está claro si el IC investigó estas actividades apoyadas y basadas en los EE. UU. Si lo hizo, aún tiene que poner alguno de sus hallazgos a disposición de la comunidad científica de EE. UU. para un análisis y una evaluación independientes y transparentes. Si, por otro lado, el IC no investigó estas actividades apoyadas por los EE. UU. y basadas en los EE. UU.,
Esta falta de una investigación científica independiente y transparente con sede en los Estados Unidos ha tenido cuatro consecuencias muy adversas. En primer lugar, se ha debilitado la confianza pública en la capacidad de las instituciones científicas estadounidenses para gobernar las actividades de la ciencia estadounidense de manera responsable. Segundo, la investigación del origen del SARS-CoV-2 se ha politizado dentro del Congreso de los EE. UU. ( 5 ); como resultado, se ha obstruido y demorado el inicio de una investigación independiente y transparente. En tercer lugar, los investigadores de EE. UU. con un conocimiento profundo de las posibilidades de un incidente asociado con un laboratorio no han podido compartir su experiencia de manera efectiva. En cuarto lugar, el fracaso de los NIH, uno de los principales financiadores del trabajo colaborativo entre EE. UU. y China, para facilitar la investigación sobre los orígenes del SARS-CoV-2 ( 4) ha fomentado la desconfianza con respecto a las actividades de investigación de biodefensa de los Estados Unidos.
Gran parte del trabajo sobre CoV similares al SARS realizado en Wuhan fue parte de un programa de investigación científica activo y altamente colaborativo entre EE. UU. y China financiado por el gobierno de (NIH, Agencia de Reducción de la Amenaza de Defensa [DTRA] y Agencia de los Estados Unidos para el Desarrollo Internacional [USAID]), coordinado por investigadores de EcoHealth Alliance (EHA), pero con la participación de investigadores de varias otras instituciones estadounidenses. Por esta razón, es importante que las instituciones estadounidenses sean transparentes sobre cualquier conocimiento de las actividades detalladas que se estaban llevando a cabo en Wuhan y en los Estados Unidos. La evidencia también puede sugerir que instituciones de investigación en otros países estuvieron involucradas, y también se les debe pedir que envíen información relevante (p. ej., con respecto a secuencias no publicadas).
Las instituciones estadounidenses participantes incluyen la EHA, la Universidad de Carolina del Norte (UNC), la Universidad de California en Davis (UCD), el NIH y la USAID. Bajo una serie de subvenciones NIH y contratos de USAID, EHA coordinó la recolección de CoV de murciélagos similares al SARS del campo en el suroeste de China y el sudeste asiático, la secuenciación de estos virus, el archivo de estas secuencias (que involucran UCD), y el análisis y manipulación de estos virus (sobre todo en la UNC). Se realizó un amplio espectro de trabajo de investigación sobre el coronavirus no solo en Wuhan (incluidos grupos de la Universidad de Wuhan y el CDC de Wuhan, así como WIV) sino también en los Estados Unidos. Los detalles exactos del trabajo de campo y de laboratorio de la asociación EHA-WIV-UNC, y la participación de otras instituciones en los Estados Unidos y China, no se han revelado para un análisis independiente.
EHA, UNC, NIH, USAID y otros socios de investigación no han revelado sus actividades a la comunidad científica de los EE. UU. y al público de los EE. UU., sino que han declarado que no estaban involucrados en ningún experimento que podría haber resultado en el surgimiento de SARS-CoV- 2. El NIH ha declarado específicamente ( 6 ) que existe una distancia evolutiva significativa entre las secuencias virales publicadas y la del SARS-CoV-2 y que el virus pandémico no pudo haber resultado del trabajo patrocinado por el NIH. Por supuesto, esta declaración es tan buena como los datos limitados en los que se basa, y la verificación de esta afirmación depende de obtener acceso a cualquier otra secuencia viral no publicada que esté depositada en bases de datos relevantes de EE. UU. y China ( 7 , 8). El 11 de mayo de 2022, el director interino de los NIH, Lawrence Tabak, testificó ante el Congreso que varias secuencias de este tipo en una base de datos de EE. UU. se eliminaron de la vista del público, y que esto se hizo a pedido de investigadores chinos y estadounidenses.
Las negativas generales de los NIH ya no son lo suficientemente buenas. Aunque el NIH y USAID se han resistido enérgicamente a la divulgación completa de los detalles del programa de trabajo de EHA-WIV-UNC, varios documentos filtrados al público o publicados a través de la Ley de Libertad de Información (FOIA) han generado inquietudes. Estas propuestas de investigación dejan en claro que la colaboración EHA-WIV-UNC participó en la recopilación de una gran cantidad de virus similares al SARS hasta ahora no documentados y se dedicó a su manipulación dentro del nivel de seguridad biológica (BSL) -2 y BSL-3. instalaciones de laboratorio, lo que genera preocupaciones de que un virus en el aire podría haber infectado a un trabajador de laboratorio ( 9). Otros han discutido una variedad de escenarios, incluida una infección que involucró un virus natural recolectado del campo o quizás un virus manipulado en uno de los laboratorios ( 3 ).
Detalles pasados por alto
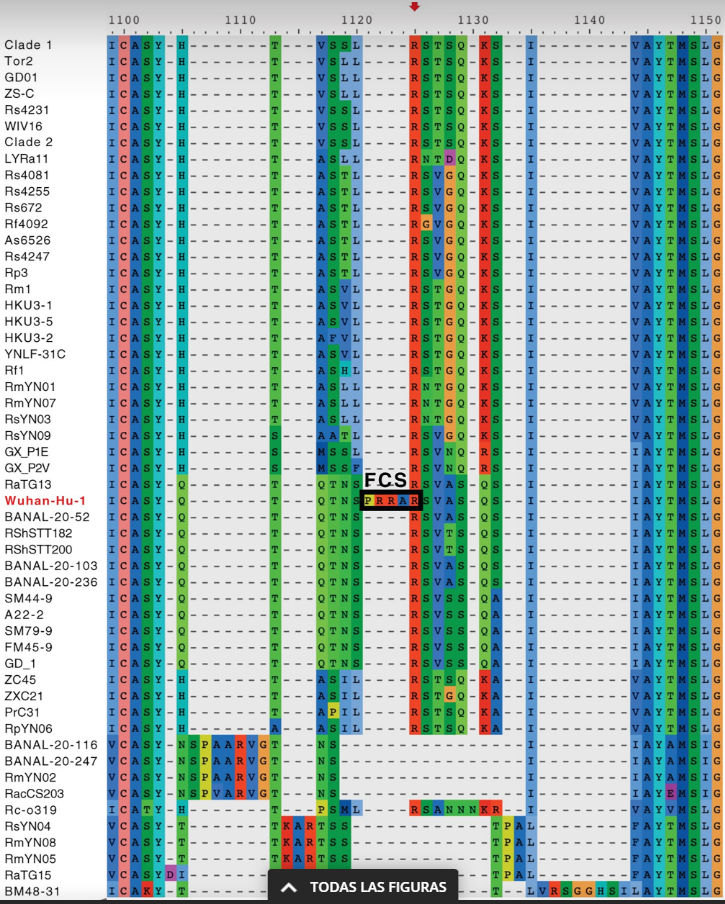
Preocupaciones especiales rodean la presencia de un sitio de escisión de furina inusual (FCS) en el SARS-CoV-2 ( 10 ) que aumenta la patogenicidad y la transmisibilidad del virus en relación con virus relacionados como el SARS-CoV-1 ( 11 , 12 ). SARS-CoV-2 es, hasta la fecha, el único miembro identificado del subgénero sarbecovirus que contiene un FCS, aunque estos están presentes en otros coronavirus ( 13 , 14 ). Una parte de la secuencia de la proteína espiga de algunos de estos virus se ilustra en la alineación que se muestra en la Fig. 1 , lo que ilustra la naturaleza inusual del FCS y su aparente inserción en el SARS-CoV-2 ( 15). Desde las primeras semanas después de que la secuencia del genoma del SARS-CoV-2 estuvo disponible, los investigadores han comentado sobre la presencia inesperada del FCS dentro del SARS-CoV-2, lo que implica que el SARS-CoV-2 podría ser un producto de manipulación de laboratorio. . En un artículo de revisión que argumentaba en contra de esta posibilidad, se afirmó que la secuencia de aminoácidos del FCS en el SARS-CoV-2 es una secuencia inusual y no estándar para un FCS y que nadie en un laboratorio diseñaría un FCS tan novedoso ( 13 ) .
De hecho, la afirmación de que el FCS en el SARS-CoV-2 tiene una secuencia de aminoácidos inusual y no estándar es falsa. La secuencia de aminoácidos del FCS en el SARS-CoV-2 también existe en la subunidad α del ENaC humano ( 16 ), donde se sabe que es funcional y se ha estudiado ampliamente ( 17 , 18 ). El FCS del ENaC α humano tiene la secuencia de aminoácidos RRAR'SVAS ( Fig. 2 ), una secuencia de ocho aminoácidos que es perfectamente idéntica al FCS del SARS-CoV-2 ( 16 ).
ENaC es un canal de sodio epitelial, expresado en la superficie apical de las células epiteliales en el riñón, el colon y las vías respiratorias ( 19 , 20), que juega un papel fundamental en el control del intercambio de fluidos. La subunidad ENaC α tiene un FCS funcional ( 17 , 18 ) que es esencial para la función del canal iónico ( 19 ) y se ha caracterizado en una variedad de especies. La secuencia FCS de ENaC α humano ( 20 ) es idéntica en chimpancé, bonobo, orangután y gorila ( Apéndice SI , Fig. 1 ), pero diverge en todas las demás especies, incluso en primates, excepto en una. (La única especie no humana que no es un gran simio con la misma secuencia es Pipistrellus kuhlii , una especie de murciélago que se encuentra en Europa y Asia occidental; otras especies de murciélagos, incluido Rhinolophus ferrumequinem, tienen una secuencia FCS diferente en ENaC α [RKAR 'SAA]).

Una consecuencia de este "mimetismo molecular" entre el FCS del pico de SARS CoV-2 y el FCS del ENaC humano es la competencia por la furina del huésped en la luz del aparato de Golgi, donde se procesa el pico de SARS-CoV-2. Esto da como resultado una disminución en la expresión de ENaC humano ( 21 ). Una disminución en la expresión de ENaC humano compromete la función de las vías respiratorias y se ha implicado como un factor contribuyente en la patogénesis de COVID-19 ( 22 ). Otra consecuencia de este sorprendente mimetismo molecular se evidencia en la aparente reactividad cruzada con ENaC humano de anticuerpos de pacientes con COVID-19, con los niveles más altos de anticuerpos con reacción cruzada dirigidos contra este epítopo que se asocian con la enfermedad más grave ( 23 ).
No sabemos si la inserción del FCS fue el resultado de la evolución natural ( 2 , 13 ), quizás a través de un evento de recombinación en un mamífero intermedio o un humano ( 13 , 24 ), o fue el resultado de una introducción deliberada del FCS en un virus similar al SARS como parte de un experimento de laboratorio. Sabemos que la inserción de tales secuencias FCS en virus similares al SARS fue un objetivo específico del trabajo propuesto por la asociación EHA-WIV-UNC dentro de una propuesta de subvención de 2018 ("DEFUSE") que se envió a los Proyectos de Investigación Avanzada de Defensa de EE. UU. Agencia (DARPA) ( 25). La propuesta de DARPA de 2018 no fue financiada, pero no sabemos si parte del trabajo propuesto se llevó a cabo posteriormente en 2018 o 2019, quizás utilizando otra fuente de financiación.
También sabemos que este equipo de investigación estaría familiarizado con varios experimentos anteriores relacionados con la inserción exitosa de una secuencia FCS en el SARS-CoV-1 ( 26 ) y otros coronavirus, y tenían mucha experiencia en la construcción de quiméricos similares al SARS. virus ( 27 – 29 ). Además, el equipo de investigación también estaría familiarizado con la secuencia FCS y el mecanismo de activación dependiente de FCS del ENaC α humano ( 19 ), que se caracterizó ampliamente en la UNC ( 17 , 18).
Para un equipo de investigación que evalúa el potencial pandémico de los coronavirus relacionados con el SARS, el FCS de ENaC humano, un FCS que se sabe que se escinde de manera eficiente por la furina del huésped presente en la ubicación objetivo (células epiteliales) de un órgano objetivo importante (pulmón), del organismo objetivo (humano): podría ser una elección racional, si no obvia, de FCS para introducir en un virus para alterar su infectividad, en línea con otros trabajos realizados anteriormente.
Por supuesto, el mimetismo molecular de ENaC dentro de la proteína del pico del SARS-CoV-2 podría ser una mera coincidencia, aunque con una probabilidad muy baja. La secuencia FCS exacta presente en el SARS-CoV-2 se introdujo recientemente en la proteína espiga del SARS-CoV-1 en el laboratorio, en una elegante serie de experimentos ( 12 , 30 ), con consecuencias predecibles en términos de transmisibilidad viral mejorada y patogenicidad. Obviamente, la creación de tales “quimeras” SARS-1/2 es un área de cierta preocupación para los responsables de la regulación presente y futura de esta área de la biología. [Tenga en cuenta que estos experimentos en la ref. 30 se realizaron en el contexto de un virus "pseudotipado" seguro y, por lo tanto, no representaron ningún peligro de producir o liberar un nuevo patógeno]. Estos experimentos simples muestran que la introducción de los 12 nucleótidos que constituyen la inserción FCS en el SARS-CoV-2 no ser difícil de lograr en un laboratorio. Por lo tanto, parecería razonable solicitar que las comunicaciones electrónicas y otros datos relevantes de los grupos estadounidenses estén disponibles para su escrutinio.
Buscando Transparencia
Hasta la fecha, el gobierno federal, incluido el NIH, no ha hecho lo suficiente para promover la confianza pública y la transparencia en la ciencia que rodea al SARS-CoV-2. Un goteo constante de información inquietante ha arrojado una nube oscura sobre la agencia. El NIH podría decir más sobre el posible papel de sus beneficiarios en el surgimiento del SARS-CoV-2, pero la agencia no ha revelado al público la posibilidad de que el SARS-CoV-2 haya surgido de un evento asociado con la investigación, a pesar de que varios investigadores expresaron esa preocupación el 1 de febrero de 2020, en una conversación telefónica que fue documentada por correo electrónico ( 5 ). Esos correos electrónicos se dieron a conocer al público solo a través de la FOIA y sugieren que el liderazgo de los NIH asumió un papel temprano y activo en la promoción de la "hipótesis zoonótica" y el rechazo de la hipótesis asociada al laboratorio (5 ). El NIH se ha resistido a la publicación de pruebas importantes, como las propuestas de subvenciones y los informes de proyectos de la EHA, y ha continuado redactando los materiales publicados bajo la FOIA, incluida una notable redacción de 290 páginas en un comunicado reciente de la FOIA.
La información que ahora posee el equipo de investigación encabezado por la EHA ( 7 ), así como las comunicaciones de ese equipo de investigación con las agencias de financiación de la investigación de EE. UU., incluidos NIH, USAID, DARPA, DTRA y el Departamento de Seguridad Nacional, podrían arrojar mucha luz sobre los experimentos realizados por el equipo de investigación financiado por los EE. UU. y sobre la posible relación, si la hay, entre esos experimentos y la aparición del SARS-CoV-2. No afirmamos que la manipulación de laboratorio estuvo involucrada en la aparición del SARS-CoV-2, aunque es evidente que podría haberlo sido. Sin embargo, afirmamos que hasta la fecha no ha habido ningún examen científico independiente y transparente del alcance total de las pruebas basadas en los Estados Unidos.
La evidencia relevante basada en EE. UU. incluiría la siguiente información: cuadernos de laboratorio, bases de datos de virus, medios electrónicos (correos electrónicos, otras comunicaciones), muestras biológicas, secuencias virales recopiladas y conservadas como parte del proyecto PREDICT ( 7 ) y otros programas financiados, y entrevistas del equipo de investigación dirigido por EHA por investigadores independientes, junto con un registro completo de la participación de la agencia estadounidense en la financiación de la investigación sobre virus similares al SARS, especialmente con respecto a proyectos en colaboración con instituciones con sede en Wuhan. Sugerimos que una investigación bipartidista también debería dar seguimiento a la conclusión tentativa del CI ( 4) que el brote inicial en Wuhan pudo haber ocurrido a más tardar en noviembre de 2019 y que, por lo tanto, el virus circulaba antes del grupo de casos clínicos conocidos en diciembre. El IC no reveló la evidencia de esta declaración, ni cuándo partes del gobierno de los EE. UU. o investigadores con sede en los EE. UU. se dieron cuenta por primera vez de un posible nuevo brote. Cualquier información y conocimiento disponible sobre los primeros días del brote, incluidas las secuencias virales ( 8 ), podría arrojar mucha luz sobre la cuestión de los orígenes.
Seguimos reconociendo el tremendo valor de la cooperación entre EE. UU. y China en los esfuerzos continuos para descubrir los orígenes próximos de la pandemia. Gran parte de la información vital aún reside en China, en los laboratorios, muestras de hospitales e información epidemiológica temprana que aún no está disponible para la comunidad científica. Sin embargo, una investigación basada en los EE. UU. no necesita esperar: hay mucho que aprender de las instituciones de los EE. UU. que participaron ampliamente en la investigación que puede haber contribuido o documentado la aparición del virus SARS-CoV-2. Solo una investigación independiente y transparente, tal vez como una investigación bipartidista del Congreso, revelará la información que se necesita para permitir un proceso científico completo de escrutinio y evaluación.
References
1.- P. Zhou et al., A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature 579, 270–273 (2020).
2.- K. G. Andersen, A. Rambaut, W. I. Lipkin, E. C. Holmes, R. F. Garry, The proximal origin of SARS-CoV-2. Nat. Med. 26, 450–452 (2020).
3.- D. A. Relman, To stop the next pandemic, we need to unravel the origins of COVID-19. Proc. Natl. Acad. Sci. U.S.A. 117, 29246–29248 (2020).
4.- Office of the Director of National Intelligence, National Intelligence Council, Updated assessment on COVID 19 origins. https://www.dni.gov/files/ODNI/documents/assessments/Declassified-Assessment-on-COVID-19-Origins.pdf. Accessed 21 February 2022.
5.- M. Hibbett, R. Grim, House republicans release text of redacted Fauci emails on COVID origins. The Intercept (12 January 2022). https://theintercept.com/2022/01/12/covid-origins-fauci-redacted-emails/. Accessed 21 February 2022.
6.- NIAID, SARS-COV-2 and NIAID-supported bat coronavirus research. An analysis: Evolutionary distance of SARS-CoV-2 and bat coronaviruses studied under the NIH-supported research grant to EcoHealth Alliance (2021). https://www.niaid.nih.gov/diseases-conditions/coronavirus-bat-research. Accessed 21 February 2022.
7.- S. Suryanarayanan, Ecohealth alliance wanted to block disclosure of covid-19-relevant virus data from China. US Right to Know (10 January 2022). https://usrtk.org/biohazards-blog/ecohealth-alliance-wanted-to-block-disclosure-of-covid-19-relevant-virus-data-from-china/. Accessed 21 February 2022.
8.- J. D. Bloom, Recovery of deleted deep sequencing data sheds more light on the early Wuhan SARS-CoV-2 epidemic. Mol. Biol. Evol. 38, 5211–5224 (2021).
9.- M. Field, A lab assistant involved in COVID-19 research in Taiwan exposed 110 people after becoming infected at work. Bulletin of the Atomic Scientists (25 January 2022). https://thebulletin.org/2022/01/a-lab-assistant-involved-in-covid-19-research-in-taiwan-exposed-110-people-after-becoming-infected-at-work/. Accessed 21 February 2022.
10.- B. Coutard et al., The spike glycoprotein of the new coronavirus 2019-nCoV contains a furin-like cleavage site absent in CoV of the same clade. Antiviral Res. 176, 104742 (2020).
11.- M. Hoffmann, H. Kleine-Weber, S. Pöhlmann, A multibasic cleavage site in the spike protein of SARS-CoV-2 is essential for infection of human lung cells. Mol. Cell 78, 779–784.e5 (2020).
12.- T. P. Peacock et al., The furin cleavage site in the SARS-CoV-2 spike protein is required for transmission in ferrets. Nat. Microbiol. 6, 899–909 (2021).
13.- E. C. Holmes et al., The origins of SARS-CoV-2: A critical review. Cell 184, 4848–4856 (2021).
14.- Y. Wu, S. Zhao, Furin cleavage sites naturally occur in coronaviruses. Stem Cell Res. (Amst.) 50, 102115 (2020).
15.- Y. A. Chan, S. H. Zhan, The emergence of the spike furin cleavage site in SARS-CoV-2. Mol. Biol. Evol. 39, msab327 (2022).
16.- P. Anand, A. Puranik, M. Aravamudan, A. J. Venkatakrishnan, V. Soundararajan, SARS-CoV-2 strategically mimics proteolytic activation of human ENaC. eLife 9, e58603 (2020).
17.- A. García-Caballero, Y. Dang, H. He, M. J. Stutts, ENaC proteolytic regulation by channel-activating protease 2. J. Gen. Physiol. 132, 521–535 (2008).
18.- P. Kota, M. Gentzsch, Y. L. Dang, R. C. Boucher, M. J. Stutts, The N terminus of α-ENaC mediates ENaC cleavage and activation by furin. J. Gen. Physiol. 150, 1179–1187 (2018).
19.- T. R. Kleyman, D. C. Eaton, Regulating ENaC’s gate. Am. J. Physiol. Cell Physiol. 318, C150–C162 (2020).
20I. Hanukoglu, A. Hanukoglu, Epithelial sodium channel (ENaC) family: Phylogeny, structure-function, tissue distribution, and associated inherited diseases. Gene 579, 95–132 (2016).
21.- S. N. Grant, H. A. Lester, Regulation of epithelial sodium channel activity by SARS-CoV-1 and SARS-CoV-2 proteins. Biophys. J. 120, 2805–2813 (2021).
22.- M. Gentzsch, B. C. Rossier, A pathophysiological model for COVID-19: Critical importance of transepithelial sodium transport upon airway infection. Function 1, zqaa024 (2020).
23.- W. A. Haynes et al; Yale IMPACT Team, High-resolution epitope mapping and characterization of SARS-CoV-2 antibodies in large cohorts of subjects with COVID-19. Commun. Biol. 4, 1317 (2021).
24.- W. R. Gallaher, A palindromic RNA sequence as a common breakpoint contributor to copy-choice recombination in SARS-COV-2. Arch. Virol. 165, 2341–2348 (2020).
25.- S. Lerner, M. Hvistendahl, New details emerge about coronavirus research at Chinese lab. The Intercept (6 September 2021). https://theintercept.com/2021/09/06/new-details-emerge-about-coronavirus-research-at-chinese-lab/. Accessed 22 February 2022.
26.- K. E. Follis, J. York, J. H. Nunberg, Furin cleavage of the SARS coronavirus spike glycoprotein enhances cell-cell fusion but does not affect virion entry. Virology 350, 358–369 (2006).
27.- R. S. Baric, A. C. Sims, Development of mouse hepatitis virus and SARS-CoV infectious cDNA constructs. Curr. Top. Microbiol. Immunol. 287, 229–252 (2005).
28.- V. D. Menachery et al., A SARS-like cluster of circulating bat coronaviruses shows potential for human emergence. Nat. Med. 21, 1508–1513 (2015).
29.- B. Yount et al., Reverse genetics with a full-length infectious cDNA of severe acute respiratory syndrome coronavirus. Proc. Natl. Acad. Sci. U.S.A. 100, 12995–13000 (2003).
30.- H. Winstone et al., The polybasic cleavage site in SARS-CoV-2 spike modulates viral sensitivity to type I interferon and IFITM2. J. Virol. 95, e02422-20 (2021).