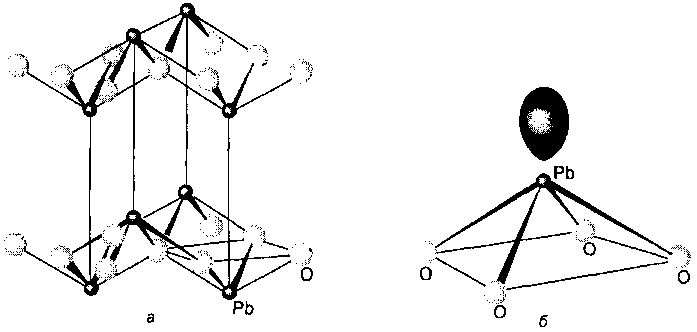
Тетрахлорид Олова
🛑 👉🏻👉🏻👉🏻 ИНФОРМАЦИЯ ДОСТУПНА ЗДЕСЬ ЖМИТЕ 👈🏻👈🏻👈🏻
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии , проверенной 13 мая 2018; проверки требуют 9 правок .
У этого термина существуют и другие значения, см. Хлорид олова .
Это заготовка статьи о неорганическом веществе . Вы можете помочь проекту, дополнив её.
↑ Промышленные фторорганические продукты: справочное издание / Б. Н. Максимов, В. Г. Барабанов, И. Л. Серушкин и др.. — 2-е, перераб. и доп. — СПб. : Химия, 1996. — 544 с. — ISBN 5-7245-1043-X .
Вики любит памятники: ваш взгляд на культурное наследие России!
Фотографируйте исторические и архитектурные памятники. Авторы лучших снимков получат призы!
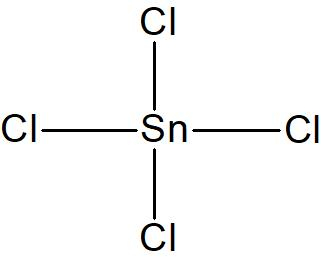
Хлори́д о́лова(IV) ( тетрахлорстанна́н , тетрахлори́д о́лова , оловя́нное ма́сло , хло́рное о́лово , четырёххло́рное о́лово ) — бинарное соединение олова и хлора с формулой Sn Cl 4 . Может рассматриваться как соль олова и соляной кислоты , а также как хлорпроизводное станнана .
Тяжёлая бесцветная (иногда желтоватая) жидкость с плотностью 2,226 г/см 3 , кипит около 114 °C, затвердевает около −33 °C. На воздухе дымит. Алхимики называли её Spiritus fumans (fammus) Libavii («дымящий/дымящийся спирт Либавия»).
Вещество получено немецким врачом и химиком Андреасом Либавием в 1597 году.
Мелкораспылённый тетрахлорид олова образует с парами воды густой дым и оказывает раздражающее действие на кожу, поэтому он использовался как дымообразователь и химическое оружие во время Первой мировой войны .
В лабораторных условиях тетрахлорид может быть получен одним из следующих способов:
При растворении в воде происходит гидролиз :
Безводный хлорид олова (IV) - основной предшественник в химии оловоорганических соединений .
Так, при обработке хлорида олова (IV) реактивом Гриньяра образуются соединения ряда тетраалкилолова:
Такие же соединения образуются в реакции с алюминийорганическими веществами в присутствии диэтилового эфира :
Безводный хлорид олова (IV) способен реагировать с соединениями тетраалкилолова с образованием оловоорганических хлоридов:
Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное.
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии , проверенной 13 мая 2018; проверки требуют 9 правок .
У этого термина существуют и другие значения, см. Хлорид олова .
Это заготовка статьи о неорганическом веществе . Вы можете помочь проекту, дополнив её.
↑ Промышленные фторорганические продукты: справочное издание / Б. Н. Максимов, В. Г. Барабанов, И. Л. Серушкин и др.. — 2-е, перераб. и доп. — СПб. : Химия, 1996. — 544 с. — ISBN 5-7245-1043-X .
Вики любит памятники: ваш взгляд на культурное наследие России!
Фотографируйте исторические и архитектурные памятники. Авторы лучших снимков получат призы!
Хлори́д о́лова(IV) ( тетрахлорстанна́н , тетрахлори́д о́лова , оловя́нное ма́сло , хло́рное о́лово , четырёххло́рное о́лово ) — бинарное соединение олова и хлора с формулой Sn Cl 4 . Может рассматриваться как соль олова и соляной кислоты , а также как хлорпроизводное станнана .
Тяжёлая бесцветная (иногда желтоватая) жидкость с плотностью 2,226 г/см 3 , кипит около 114 °C, затвердевает около −33 °C. На воздухе дымит. Алхимики называли её Spiritus fumans (fammus) Libavii («дымящий/дымящийся спирт Либавия»).
Вещество получено немецким врачом и химиком Андреасом Либавием в 1597 году.
Мелкораспылённый тетрахлорид олова образует с парами воды густой дым и оказывает раздражающее действие на кожу, поэтому он использовался как дымообразователь и химическое оружие во время Первой мировой войны .
В лабораторных условиях тетрахлорид может быть получен одним из следующих способов:
При растворении в воде происходит гидролиз :
Безводный хлорид олова (IV) - основной предшественник в химии оловоорганических соединений .
Так, при обработке хлорида олова (IV) реактивом Гриньяра образуются соединения ряда тетраалкилолова:
Такие же соединения образуются в реакции с алюминийорганическими веществами в присутствии диэтилового эфира :
Безводный хлорид олова (IV) способен реагировать с соединениями тетраалкилолова с образованием оловоорганических хлоридов:
Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное.
https://ru.wikipedia.org/wiki/%D0%A5%D0%BB%D0%BE%D1%80%D0%B8%D0%B4_%D0%BE%D0%BB%D0%BE%D0%B2%D0%B0(IV)
https://ru.wikipedia.org/wiki/%D0%A2%D0%B5%D1%82%D1%80%D0%B0%D1%85%D0%BB%D0%BE%D1%80%D0%B8%D0%B4_%D0%BE%D0%BB%D0%BE%D0%B2%D0%B0
Порно Фильмы С Гермафродитами
Порно Спящие
Порно Минет Красивый Бесплатно
Хлорид олова(IV) — Википедия
Хлорид олова (IV) — Википедия
Олово тетрахлорид - Справочник химика 21
Тетрахлорид олова - это... Что такое Тетрахлорид олова?
Купить Олова тетрахлорид 1000 гр в интернет-магазине ...
Тетрахлорид - олово - Большая Энциклопедия Нефти и Газа ...
Тетрахлорид - олово - Большая Энциклопедия Нефти и Газа ...
Тетрахлорид олова плотность - Справочник химика 21
Тетрахлорид олова и хлоростаннаты (IV) | khimie.ru
тетрахлорид олова - Неорганическая химия - Форум …
Тетрахлорид Олова
_chloride.jpg)