Создавая бреши
БиомолекулаТеперь рассмотрим большую группу методик, связанных с доставкой препаратов непосредственно через ГЭБ. Условно их можно разделить на две группы:
1) подразумевающие временное повреждение ГЭБ
2) использующие физико-химические подходы и свойства мембран эндотелиальных клеток для аккуратного внедрения через ГЭБ.
Сейчас пробежимся по тем методикам, что «погрубее».
Химическое разрушение плотных контактов
Учитывая, что плотные контакты — важный конструктивный элемент ГЭБ, вполне логично стремление их ослабить — и «расцепить», подобно вагонам, клетки эндотелия. Есть такой пептид, способный расширять кровеносные сосуды, — брадикинин. Нам он интересен тем, что снижает экспрессию окклюдинов и клаудина-5, из которых и состоят в основном плотные контакты.
Введение брадикинина и его аналогов усиливает проницаемость ГЭБ, и при совместной инъекции с терапевтическими агентами можно ожидать лучшего их проникновения в мозг. В первую очередь брадикинин заинтересовал нейроонкологов, так как на опухолях особенно велико число рецепторов к брадикинину. Но клинические испытания были остановлены из-за нежелательных явлений, поскольку большое число брадикининовых рецепторов «внезапно» обнаружилось во многих тканях. По этой же причине отказались и от использования антител к клаудину-5 — этот белок также широко экспрессируется в периферических сосудах. Но, кажется, исследователи «нащупали», как можно разъединить плотные контакты в ГЭБ, не разрушив все сосуды пациента. В эндотелиальном слое есть много участков, где контактируют три клетки: там формируются триклеточные плотные контакты. В их строительстве участвует белок ангулин-1, довольно специфичный именно для эндотелиоцитов ГЭБ. Так вот, относительно недавно был создан ингибитор ангулина-1 — ангубиндин-1. Это вещество позволяет обратимо разъединять триклеточные контакты и проникать действующим веществам в нервные клетки без заметных нежелательных эффектов. Правда, пока дальше экспериментов на мышах дело не продвинулось.
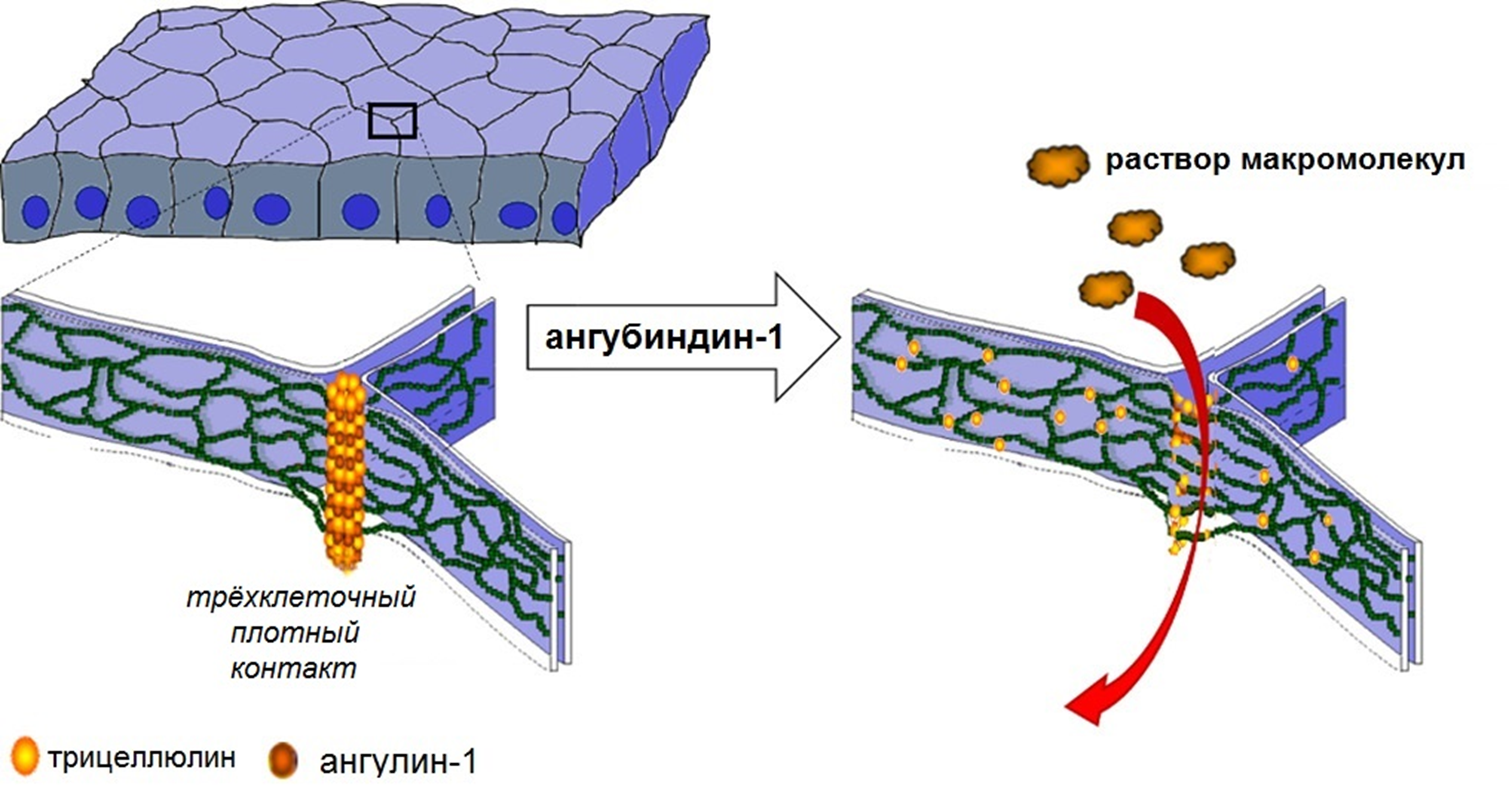
Осмотическое разрушение ГЭБ
Разъединить плотные контакты можно, если сами клетки съежатся. Для этого их достаточно поместить в гипертонический раствор, что приведет к дегидратации эндотелиоцитов и их физическому сжиманию. Для осмотического разрушения ГЭБ использовалось много разных веществ, таких как лактамид, мочевина, соли, но лучше всего подошел маннитол. Он, кстати, широко используется в клинике при отеке мозга, делая ровно то, что и должен делать диуретик — выводит избыточную жидкость. Еще в 1980-х годах был проведен ряд доклинических и клинических испытаний, в которых «концентрированный» гиперосмотический маннитол вместе с противоопухолевыми препаратами вводился через сонную артерию . С тех пор было проведено более 30 различных клинических испытаний. В некоторых были очевидные успехи. Например, при попытке лечить лимфому ЦНС комбинированным введением циклофосфамида и маннитола (плюс радиотерапия) удалось значительно увеличить медианную общую выживаемость пациентов (с 17,8 до 44,5 месяцев!).
Как вы уже догадались, что-то пошло не так. В последующих испытаниях (правда, уже с другими препаратами) осмотическое разрушение ГЭБ останавливало рост опухоли... но частично лишало слуха. Многие испытания после многообещающих результатов первой фазы застопорились на второй. В целом, как указывают авторы уже процитированного обзора, вычленить из этих испытаний полезную информацию не так-то просто. Везде разный дизайн, разные препараты, разные группы пациентов. Просто невозможно понять, насколько эта методика может быть эффективной в клинической практике, а главное — безопасной. Такие проблемы осмотического разрушения ГЭБ, как неизбирательность, нейротоксичность и воспалительные ответы, не решены до сих пор.
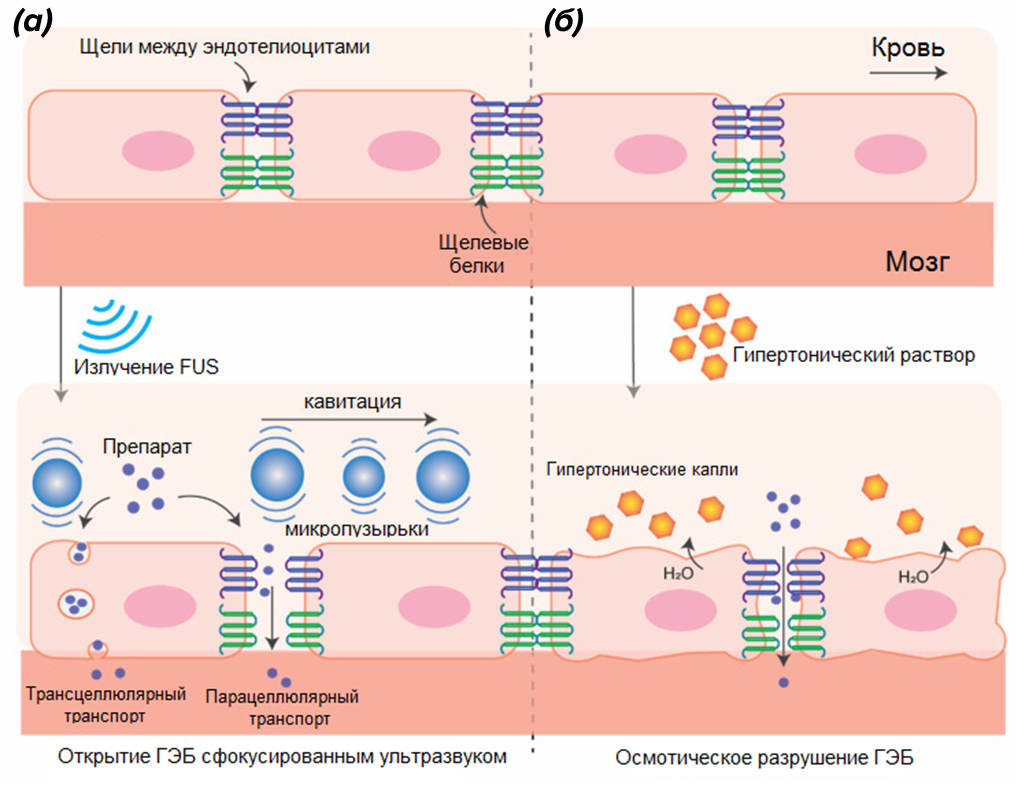
Разрушение ГЭБ сфокусированным ультразвуком
Проблему специфичности открытия ГЭБ может решить применение ультразвука высокой частоты, который можно сфокусировать в нужном месте (от того и название методики — focused ultrasound, FUS), а кроме того, варьируя частоту и длительность применения, можно контролировать степень открытия барьера. Плюс ко всему, метод неинвазивен и несет меньшие издержки от открытия ГЭБ, поскольку создает довольно короткое «окно» от 6 до 24 часов. Важным дополнением к ультразвуку могут стать вводимые микропузырьки. Их колебания под действием ультразвука вызывают кавитацию, что, в свою очередь, приводит к открытию полостей между эндотелиальными клетками. Пузырьки для FUS коммерчески доступны и, в зависимости от производителя, имеют размер от 1 до 5 мкм, иногда уже продаются покрытыми препаратом. Чем больше размер пузырька, тем сильнее раскрывается ГЭБ и дольше остается открытым; такова же зависимость и от концентрации вводимых пузырьков. С помощью FUS можно пропихнуть через ГЭБ молекулу огромных размеров — до 2000 кДа; но это в целом излишне и сопряжено с рисками инерционной кавитации и кровотечения. Достаточно того, что в присутствии ультразвука молекулы противоопухолевых препаратов и антител (например, герцептин или трастузумаб с молекулой размером 150 кДа) через ГЭБ проходят хорошо. На этот счет имеется достаточно убедительных данных, полученных в том числе и в клинических испытаниях.
Важно сделать оговорку. Есть подход, подразумевающий низкочастотную стимуляцию. Однако для этого в череп должен быть вмонтирован имплант, генерирующий волны низкой интенсивности. Во Франции даже разработали и провели клиническое испытание такого устройства (CarThera, SonoCloud-1) на пациентах с глиобластомой. По сообщениям компании CarTera, сейчас продолжаются клинические испытания улучшенных версий предложенной системы.
Это в прямом смысле пузырьки газа, покрытые слоем фосфолипидов с пришитыми цепочками полиэтиленгликоля, чтобы на них цеплять лекарственные средства. Коммерческая доступность этой диковинки не должна вас смущать. Терапия неврологических расстройств с помощью FUS это, так сказать, верхушка айсберга. На сайте Focused Ultrasound Foundation можно ознакомится с великим множеством направлений, в которых нашел применение FUS. Для целого ряда заболеваний уже получено одобрение на использование метода в клинической практике.
Сфера применения FUS очень широка и год от года расширяется. Объектом нашего интереса является проницаемость ГЭБ для доставки препаратов, но с помощью ультразвука можно осуществлять точечную термоабляцию (дословно — «выжигание») пораженных мозговых структур. Есть примеры успешного устранения эссенциального тремора и хронических болей после таламотомии с помощью FUS. В 2019 году этот подход даже получил высокую оценку и одобрение Американского общества стереотаксической и функциональной нейрохирургии. Интересно, что применение FUS на умеренных режимах, даже без каких-либо препаратов, усиливает выведение белковых агрегатов, например, белка tau или β-амилоида. Пока это показано только на мышах, но наблюдение весьма интересное.
К счастью, на тех мощностях, что используются для разрушения ГЭБ, температура повышается незначительно, поэтому риска для целостности мозговой ткани не возникает.
Любопытно и то, что FUS активирует сигнальный каскад PI3K/Akt, участвующий в нейрогенезе, и таким образом усиливает его в гиппокампе подопытных мышей. Все это еще может найти применение при терапии болезни Альцгеймера. По крайней мере, проведено два пилотных исследования на пациентах, но выборки там очень маленькие (по пять—шесть человек), и судить о результатах трудно. Пока единственное, что могут сказать авторы данных работ, — что методика FUS безопасна. Хотя с этим вряд ли согласились бы авторы обзора 2019 года, проанализировавшие 422 исследования с применением FUS. Они отмечают, что три четверти рассмотренных ими работ, строго говоря, о безопасности ничего толком не сообщают. В нейроонкологии (а в этой области выполнено примерно 40% всех клинических испытаний FUS) порог допустимого ущерба невысок. Кровотечение, воспаление, глиоз, апоптоз, некроз и прочие страшные слова теряют значимость, когда вам нужно справится с глиобластомой. Здесь, к слову, FUS достаточно эффективен и демонстрирует хорошие результаты.
Но когда мы имеем дело с нейродегенеративными заболеваниями, вопрос безопасности становится уже на первое место. Например, осложняющим фактором становится то, что естественные (если можно так сказать) патологические изменения по ходу течения заболевания могут маскировать урон от применения FUS. На самом деле, для отработки метода нужно сделать еще очень многое. Эксперименты на трансгенных мышах, моделирующих болезнь Альцгеймера, показали, что эти животные имеют меньшую проницаемость сосудов, и при обработке ультразвуком вещество проходит через ГЭБ хуже, чем у нормальных животных. А это значит, что с учетом сосудистых особенностей при нейродегенерации нужно оптимизировать размер и число частиц, а также режим обработки ультразвуком. Куда уж там исследованиям на шести пациентах!