¿Quién controla a quién?
Jeanne A. RungbyPor la Dra. Jeanne A. Rungby, médica, WCH-Escandinavia y Lucinda van Buuren, enfermera titulada, investigadora independiente, WCH Nursing and Midwifery y WCH Australia.
Si bien muchos se regocijan y otros pintan escenarios de terror sobre la posible salida de Estados Unidos de la OMS, es relevante analizar cómo la OMS influye en la política nacional e internacional y viceversa.
Una cosa es “excluirse” oficialmente, pero otra muy distinta es rescindir los numerosos acuerdos de cooperación que Estados Unidos mantiene con la OMS.
Abandonar definitivamente la OMS implica rescindir todos los acuerdos con dicha organización. Al parecer, esto no ha ocurrido en Estados Unidos.
De lo contrario.
El 22 de enero de 2025, Estados Unidos puso fin oficialmente a su membresía en la OMS con un año de preaviso.
A pesar de esta rescisión, el Instituto Nacional de Salud de Estados Unidos (NIH), por ejemplo, firmó un contrato con la OMS el 17 de enero de 2025 en relación con virus y pandemias. El contrato estará vigente hasta el 17 de enero de 2029.
Desde entonces, Estados Unidos ha firmado al menos tres nuevos acuerdos de colaboración (Centros Colaboradores) con la OMS tras el anuncio de su retirada de dicha organización.
Además, la FDA de EE. UU. mantiene un acuerdo vigente con la OMS (Autoridad Asociada a la OMS), que actualmente se extiende hasta junio de 2029. Este acuerdo otorga a la OMS una influencia significativa sobre el registro y la comercialización de medicamentos y vacunas, incluyendo el monitoreo, el control, las autorizaciones de comercialización, las inspecciones regulatorias, el control de laboratorios, la supervisión de ensayos clínicos y mucho más. Véase la captura de pantalla a continuación:
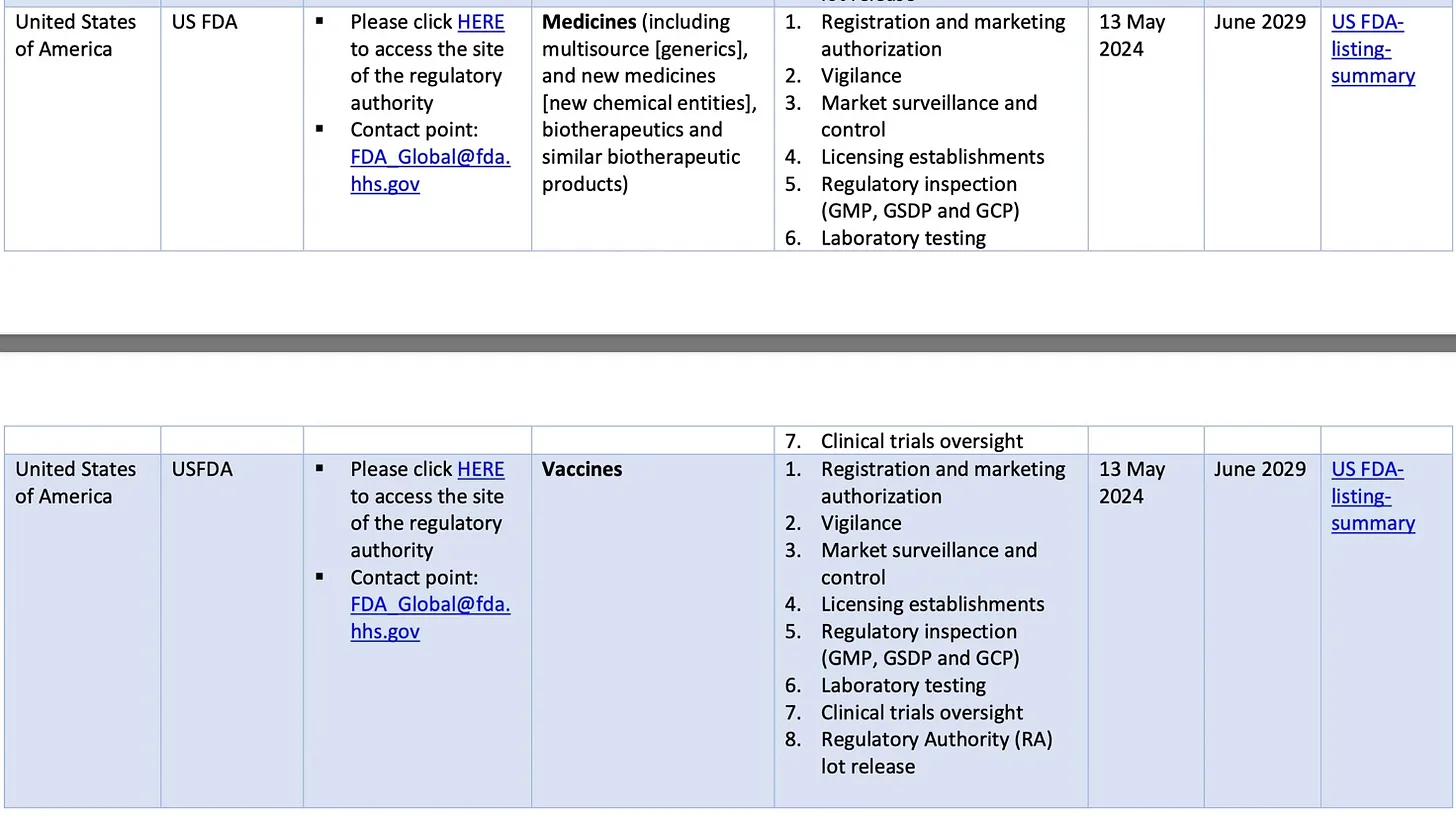
Fuente: https://cdn.who.int/media/docs/default-source/medicines/regulatorysystems/wla/list_of_wla.pdf?sfvrsn=1f6c2140_49&download=true
A través de estas alianzas, la OMS tiene una influencia considerable en
· decisiones políticas, por ejemplo, en materia de política exterior y preparación ante pandemias,
· agricultura y alimentación,
· salud, incluida la formación de profesionales de la salud,
· normas para laboratorios, empresas, etc.
· códigos de diagnóstico para enfermedades, incluidas las decisiones sobre qué enfermedades deben registrarse,
· aprobación de solicitudes de medicamentos y vacunas,
• Seguimiento de los efectos secundarios y mucho más.
Esta influencia ejercida por la OMS se ha desarrollado a lo largo de muchos años, comenzando inmediatamente después de la Segunda Guerra Mundial a través de los centros colaboradores de la OMS.
Además, existe una regulación exhaustiva y detallada de las autoridades reguladoras médicas en una proporción significativa de los países del mundo a través de las Autoridades Asociadas de la OMS (AAM) y con bases de datos globales comunes desarrolladas y controladas por la OMS.
Centros colaboradores de la OMS (CCOMS).
La investigadora australiana Lucinda van Buuren ha analizado detenidamente estos centros colaboradores. Ha constatado que la influencia de la OMS en las políticas nacionales se ejerce a través de sus más de 800 centros colaboradores en todo el mundo. La OMS también mantiene numerosos acuerdos y contratos, entre ellos con 367 socios de GOARN (Red Mundial de Alerta y Respuesta ante Brotes Epidémicos) .
Los centros colaboradores de la OMS son entidades, como universidades o agencias gubernamentales, que colaboran con la OMS. Han suscrito un acuerdo vinculante (formulario de designación) que obliga a la entidad a seguir un plan de trabajo establecido por la OMS.
El producto (producto entregable), incluidos los derechos de propiedad intelectual, pertenece a la OMS .
Esta información proviene de la guía de la OMS para centros colaboradores. Lamentablemente, la página web ha sido eliminada recientemente. Puede encontrar una copia de la guía en formato PDF en la lista de fuentes al final del documento.
El acuerdo con la OMS está sujeto a una cláusula similar a una cláusula de no competencia, que debe firmarse con la posibilidad de rescindirlo con un preaviso de tres meses.
La institución es totalmente responsable legalmente, incluyendo cualquier daño a sujetos humanos, información falsa, etc.
La OMS se ha eximido de responsabilidad en estos acuerdos, al igual que los fabricantes de vacunas están exentos de responsabilidad.
Los centros colaboradores de la OMS pueden ser
· Universidades
• Centros de formación para médicos, enfermeras y matronas,
· El ejército
· Ministerios y
¡¡¡Gobiernos!!!
El primer acuerdo de cooperación (OMS) se firmó con el Instituto Estatal Danés de Sueros (SSI). La tarea se refería a los estándares biológicos inmediatamente después del final de la Segunda Guerra Mundial, desde el 1 de enero de 1948 hasta el 20 de septiembre de 1999. Cabe suponer que la OMS (y sus partes interesadas) influyó en el método científico y la cultura del SSI durante los 51 años en que dictó las tareas en al menos algunos de sus departamentos. A lo largo de los años, el SSI danés produjo, compró y revendió vacunas. Por lo tanto, cabe suponer que la producción de vacunas estuvo, en cierta medida, bajo el control de la OMS.
SSI tiene una función de asesoramiento para el Ministro del Interior y de Salud de Dinamarca.
Entre otras cosas, el Instituto del Suero ayudó a desarrollar las primeras vacunas contra la polio, en las que se descubrió que el virus simio 40, un virus de mono, había contaminado algunas vacunas contra la polio entre aproximadamente 1955 y 1963, debido a que las vacunas se producían en células de riñón de mono. Las muestras de prueba archivadas de la producción del SSI mostraron el virus simio 40 infeccioso en algunos casos. Esto significa que los niños daneses vacunados entre abril de 1955 y 1962 estuvieron expuestos al virus simio 40 a través de la vacuna. Posteriormente, se sospechó que el virus simio 40 tenía propiedades cancerígenas, principalmente en roedores .
Estados Unidos
En Estados Unidos, el primer centro de colaboración (WHOCC) se estableció en 1950 en la Universidad Johns Hopkins para la biología molecular y la genética, incluyendo la sífilis. El acuerdo se dio por terminado el 31 de octubre de 1994. La Universidad Johns Hopkins ha tenido 10 centros de colaboración de la OMS inactivos y actualmente cuenta con 8 centros de colaboración de la OMS activos.
El segundo acuerdo de colaboración con la OMS en Estados Unidos se estableció en 1958 con el Departamento de Defensa de EE. UU.: Departamento de Patología, Instituto de Patología de las Fuerzas Armadas, Departamento de Defensa . Clasificación histológica de tumores de tejidos blandos . Finalizó el 7 de junio de 1994.
El Centro Colaborador n.º 204 de la OMS en Estados Unidos se ocupaba del síndrome de inmunodeficiencia adquirida (SIDA) en los Institutos Nacionales de Salud (NIH), y el director/jefe de este centro era el Dr. Anthony Fauci, quien desarrolló medicamentos para el VIH.
Los NIH (Institutos Nacionales de Salud) y el NIAID (Instituto Nacional de Alergias y Enfermedades Infecciosas, que forma parte de los NIH) han recibido importantes regalías de Moderna y Pfizer/BioNTech por el uso de tecnologías desarrolladas por los NIH en sus vacunas contra la COVID-19. Estas regalías incluyen patentes sobre la estabilización de la proteína de la espícula.
En diciembre de 2022, Moderna pagó un único pago de 400 millones de dólares al NIAID/NIH por el uso de patentes sobre las proteínas de la espícula del coronavirus en estado de prefusión.
Además, existen regalías pendientes de pago sobre ventas futuras como parte del acuerdo modificado. Como parte de un acuerdo más amplio, se pagarán hasta 1260 millones de dólares, que también incluyen a la Universidad de Pensilvania (467 millones de dólares), pero la parte correspondiente a los NIH se refiere específicamente a regalías.
Por lo tanto, se estima que los ingresos totales por regalías para los NIH/NIAID provenientes de las vacunas de ARNm (2020-2026) ascienden a aproximadamente 1.191,5 mil millones de dólares (400 millones de dólares de Moderna + 791,5 millones de dólares de BioNTech). Estas regalías representan entre el 1 y el 5 % del superávit total generado por estas vacunas.
En el momento de redactar este informe, Estados Unidos cuenta con 70 centros colaboradores activos de la OMS . Ocho de ellos parecen haber sido desconectados durante 2025.
Por lo tanto, la rescisión de estos acuerdos con la OMS parece ser un proceso muy lento para Estados Unidos. La siguiente figura muestra una visión general de los centros de colaboración de la OMS a lo largo de la historia.
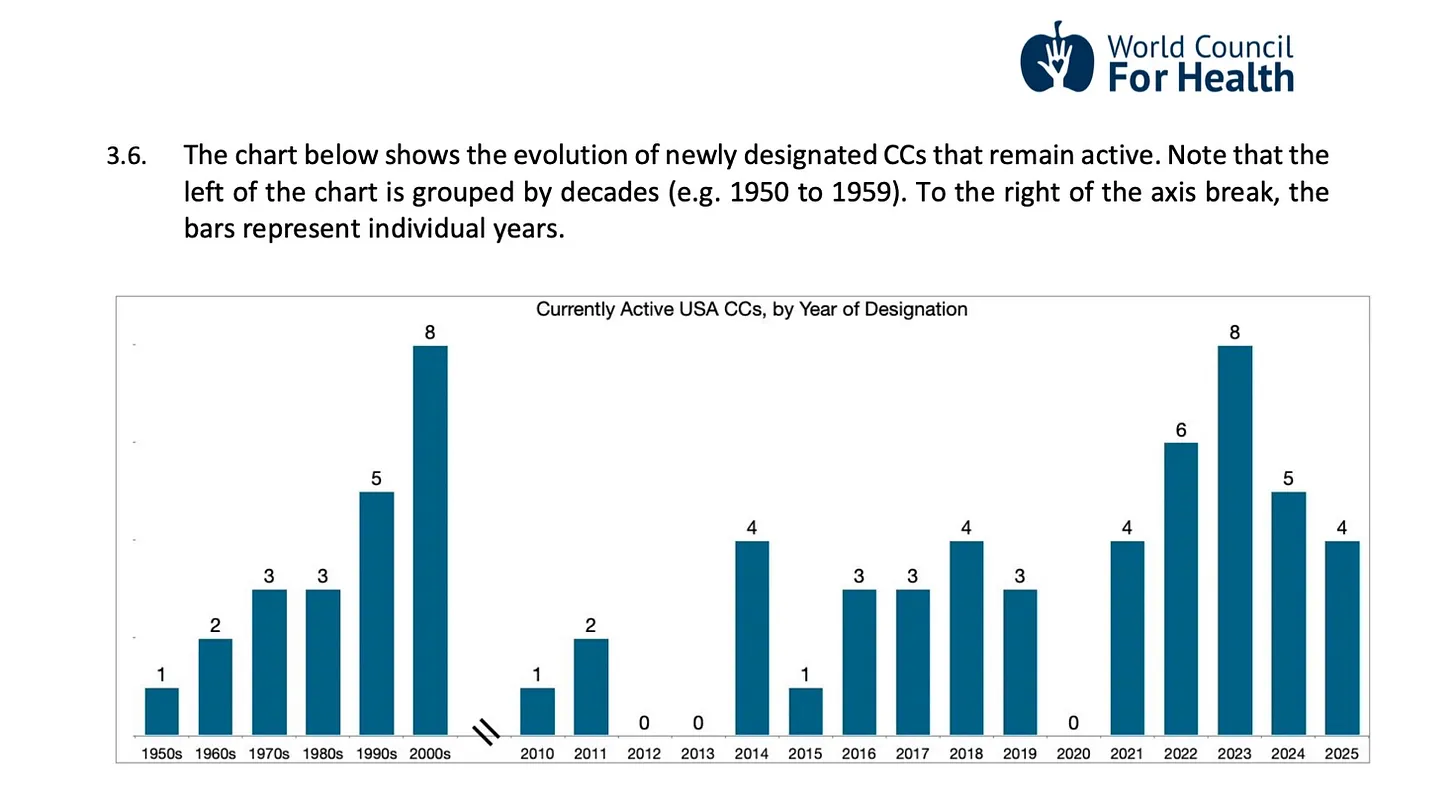
Fuente: ¿Qué significa abandonar la OMS?
Australia
El primer Centro Colaborador de la OMS australiano que figura en la lista fue el AUS-2, el Centro Colaborador de la OMS para la Clasificación Histológica de Tumores Cutáneos , designado el 1 de enero de 1965. Actualmente, Australia cuenta con 44 Centros Colaboradores de la OMS activos y 84 discontinuados; sin embargo, la numeración actual llega hasta el AUS-174. Desconocemos el método utilizado por la OMS para la numeración de los Centros Colaboradores y por qué ciertos números no están disponibles públicamente o simplemente no existen; por ejemplo, no hay ninguna entrada para el AUS-1.
Algunos coordinadores federales australianos activos de la OMS son:
• Instituto del Ejército Australiano, AUS-37, Coordinador de la OMS para la Malaria
• Agencia Australiana de Regulación de Profesionales de la Salud (AHPRA) AUS-137, Coordinador de la OMS para la Regulación del Personal Sanitario
· Administración de Productos Terapéuticos (TGA) AUS-42, Comité de Control de la OMS para el Aseguramiento de la Calidad de las Vacunas y Otros Productos Biológicos
Australia cuenta con su propia Red Mundial de Centros Colaboradores de la OMS .
• “La Red Australiana de Centros Colaboradores de la OMS se estableció en 2019 tras una extensa fase de análisis, llevada a cabo por el Departamento de Salud y Servicios Humanos de Victoria, en consulta con la Alianza Australiana para la Salud Global, el Departamento de Asuntos Exteriores y Comercio (DFAT) y el Departamento Federal de Salud.”
• “La Red busca intercambiar información, fomentar buenas prácticas y desarrollar la cooperación técnica entre los Centros Colaboradores de la OMS en Australia, así como con los gobiernos estatales y federales y otras partes interesadas pertinentes.”
• “ A junio de 2023, existen 54 Centros de Control de la OMS en Australia , la mayor cantidad per cápita del mundo.”
Estrategia de cooperación entre la OMS y Australia
El Departamento de Salud del Gobierno australiano, en colaboración con los organismos gubernamentales responsables del sector salud, y la Oficina Regional para el Pacífico Occidental de la Organización Mundial de la Salud (OMS) se complacen en presentar la Estrategia de Cooperación entre Australia y la OMS para el período 2018-2022 , la primera estrategia de este tipo entre Australia y la OMS. Esta es la primera estrategia de cooperación con un país que se centra en un país de altos ingresos de la región del Pacífico Occidental.
Este CCS se centró en cuatro áreas estratégicas prioritarias;
1) “Mejorar la seguridad sanitaria”
2) “Promover sistemas de salud centrados en las personas y la cobertura sanitaria universal (CSU)”
3) “Fortalecimiento de la regulación sanitaria”
4) “Trabajar juntos para apoyar a la OMS en sus esfuerzos por alcanzar la excelencia organizativa”.
Dinamarca
Dinamarca cuenta actualmente con cinco Centros de Cooperación de la OMS (WHOCC ). Estos se encuentran en la Universidad de Copenhague, la Universidad Técnica de Dinamarca (DTU), el Hospital Bispebjerg, el Rigshospitalet y el Instituto Parker en Frederiksberg. Al parecer, a lo largo de los años se han rescindido 46 acuerdos de cooperación con la OMS en Dinamarca.
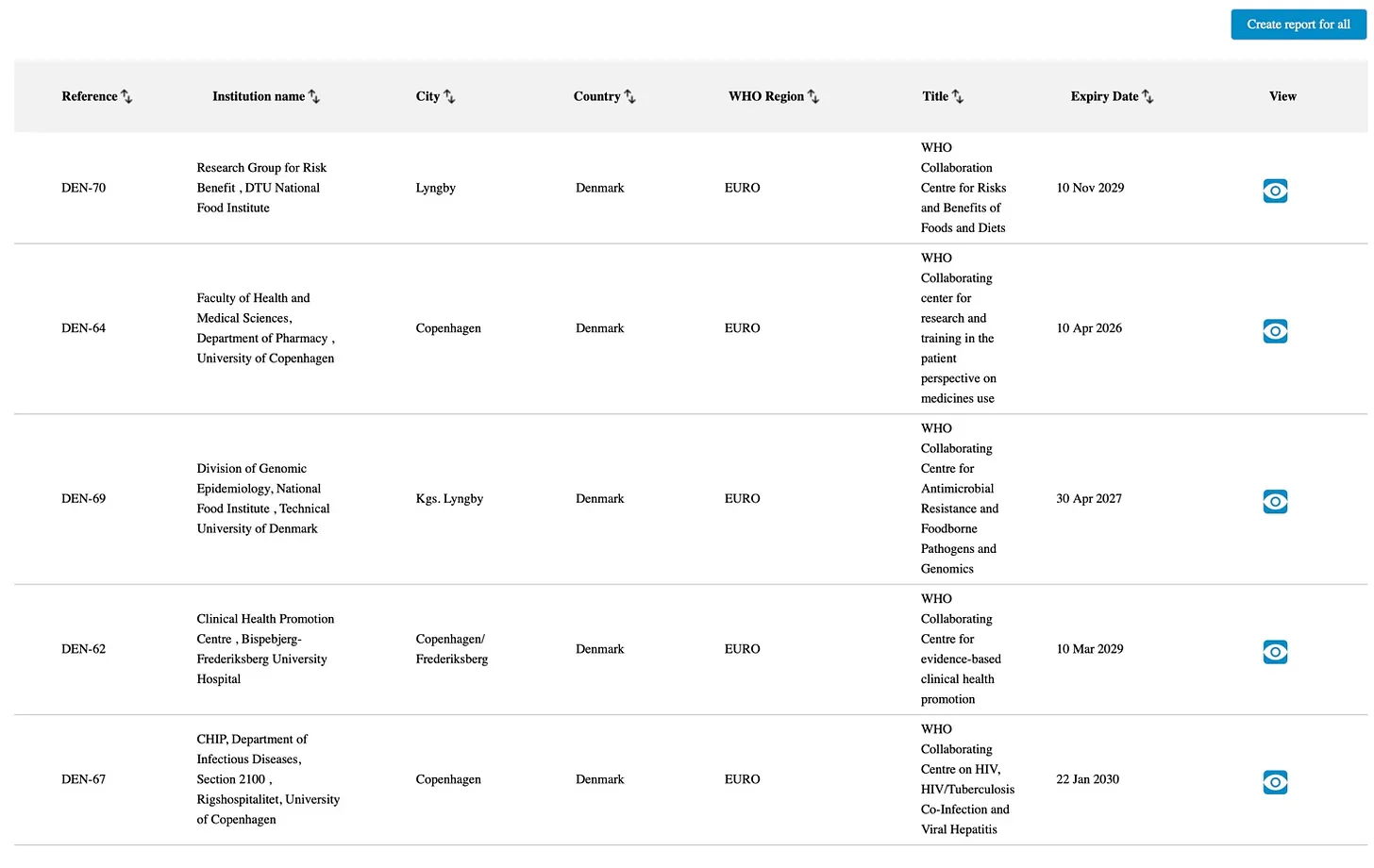
Ministerio de Salud y Ministerio de Asuntos Exteriores
Sin embargo, la OMS también mantiene estrechos acuerdos de cooperación con el Ministerio de Salud y el Ministerio de Asuntos Exteriores de Dinamarca. Este acuerdo se adjunta en formato PDF al final de la página, ya que el enlace parece haber dejado de funcionar.
El acuerdo es un documento estratégico que
“Constituye la base de la contribución voluntaria de Dinamarca a la OMS para el período 2024-2028 y es la plataforma central para el diálogo y la colaboración del Ministerio de Asuntos Exteriores con la OMS. El presupuesto para el período estratégico asciende a 390 millones de coronas danesas a lo largo de cinco años (véase la sección 6 para un presupuesto detallado). El objetivo general del apoyo de Dinamarca es contribuir al logro de los Objetivos de Desarrollo Sostenible de las Naciones Unidas en el ámbito de la salud, en particular los Objetivos 3 (salud y bienestar), 5 (igualdad de género), 10 (reducción de las desigualdades) y 17 (alianzas).”
También hay indicios de que la Administración Veterinaria y Alimentaria Danesa colabora estrechamente con la OMS y la ONU. Su plan de acción contra la resistencia a los antimicrobianos (RAM) es prácticamente idéntico al plan de acción mundial de la OMS. Si bien no está claro si existen acuerdos de cooperación específicos entre la OMS y la Administración Veterinaria y Alimentaria Danesa, esta última colabora estrechamente con el Instituto de Ciencias de la Salud (SSI) y la Universidad Técnica de Dinamarca (DTU), con la que mantiene dos acuerdos de cooperación (OMS).
La OMS parece ejercer, por tanto, una influencia considerable en la agenda política general a nivel nacional en Dinamarca.
Es posible que existan acuerdos similares con la ONU.
Con el paso de los años, las autoridades nacionales han ido transfiriendo gradualmente el control a la OMS, quizás sin comprender del todo las implicaciones de la cesión de soberanía. Dinamarca parece ser un claro ejemplo de esta transición.
¿De qué control estamos hablando?
Todo el sistema educativo, las universidades, la investigación, las normas ISO, las pruebas de laboratorio (PCR y pruebas de anticuerpos), la orientación a las autoridades sanitarias sobre la gestión de pandemias, la nutrición y los suplementos dietéticos, la agricultura, los medicamentos y las vacunas.
Es probable que la lista no esté completa.
¿Qué es una autoridad asociada a la OMS (AAM)?
Una WLA es una autoridad reguladora nacional (Agencia de Medicamentos) o regional (EMA y Comisión Europea) reconocida por la OMS por cumplir con los estándares definidos por esta organización para, entre otras cosas, la regulación de medicamentos y vacunas. Las WLA son autoridades nacionales y regionales de medicamentos. Algunos ejemplos son la Administración de Productos Terapéuticos (Australia), el Instituto Paul Ehrlich (Alemania) y la Administración de Alimentos y Medicamentos (EE. UU.).
A continuación se muestra la WLA de Australia:

Todas las autoridades nacionales europeas de medicamentos están reguladas por la Red Europea de Regulación de Medicamentos (EMRN), ¡una WLA! La Comisión Europea y la EMA forman parte de la red WLA .
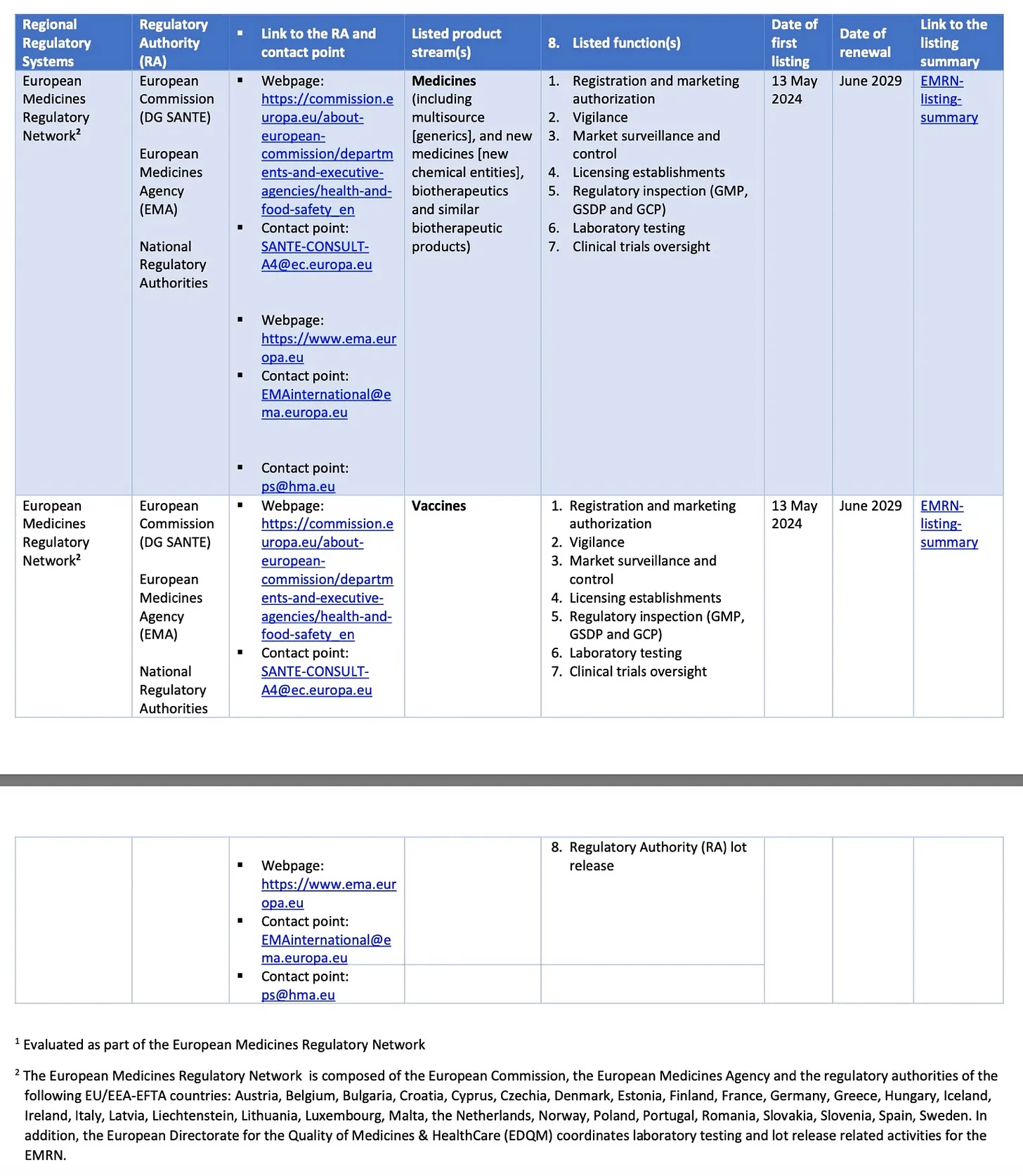
Las WLAs comparten un marco jurídico y regulatorio común . La armonización de las leyes a través de las fronteras nacionales está precedida por un proceso de cabildeo que dura un año y que necesariamente debe prepararse a nivel ministerial.
Las WLA deben cumplir con los criterios establecidos por la OMS y son supervisadas por la OMS a través de un proceso de evaluación denominado “Evaluación del desempeño” .
“Antes de cualquier actividad de evaluación de riesgos, ya sea presencial o a distancia, la Secretaría de la OMS deberá elaborar un pliego de condiciones.”
La OMS elabora un plan de trabajo obligatorio detallado, que la WLA debe seguir para alcanzar un determinado “Nivel de Madurez”. El propósito es
“garantizar que la RA controle los medicamentos exportados desde su jurisdicción y que cumpla con las últimas directrices y requisitos de la OMS para la expedición de certificados de productos farmacéuticos, incluyendo un sistema fiable para la aprobación de medicamentos y la concesión de licencias e inspección de las instalaciones de fabricación.”
¿Es fiable e independiente la inspección de una planta de fabricación regulada por la OMS?
En el caso de los medicamentos y las vacunas, a través de este proceso, la OMS verifica el registro y la autorización de comercialización, la vigilancia, el control y la vigilancia del mercado, la concesión de licencias, la inspección reglamentaria, las pruebas de laboratorio y la supervisión de los ensayos clínicos.
https://iris.who.int/server/api/core/bitstreams/8ba0873d-fab7-4cd9-aaee-e3e43be037ed/content
Evaluación del desempeño (ED)
Mientras el mundo se centraba en el Reglamento Sanitario Internacional (RSI) de la OMS, a principios de 2024 (del 9 de febrero al 15 de abril) se llevó a cabo discretamente una evaluación del desempeño de 30 agencias de salud pública . El equipo de expertos de la OMS realizó la evaluación de forma presencial o remota a través de una plataforma segura de la OMS.
Se analizaron varios indicadores preseleccionados. Estos indicadores fueron determinados por la OMS.
Varios de estos indicadores de evaluación eran obligatorios para las WLA.
El Anexo 3 contiene preguntas detalladas que el experto de la OMS formula a las autoridades reguladoras nacionales (ARN) durante una evaluación de desempeño, la cual constituye la base para la aprobación como WLA. Véase la captura de pantalla a continuación:
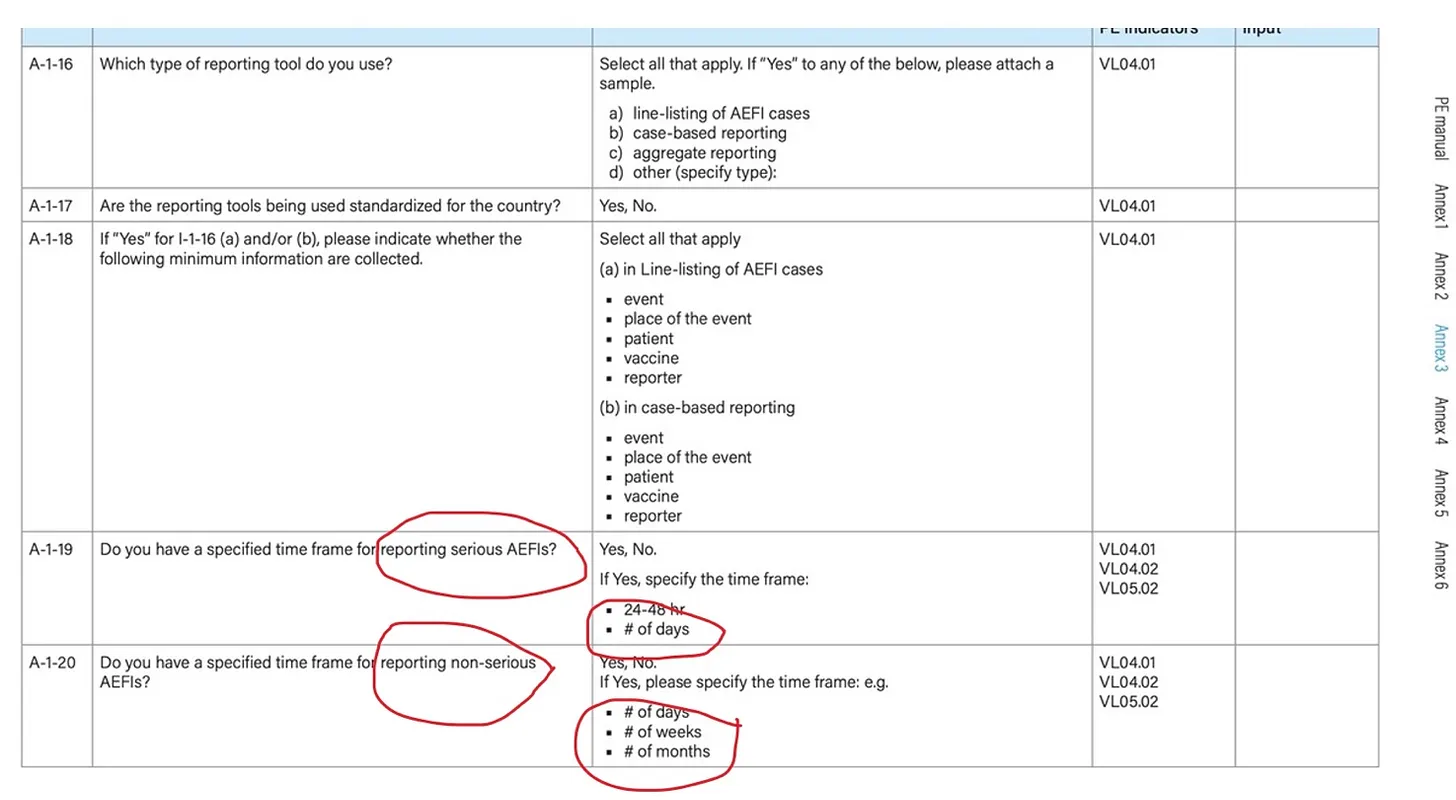
Un AEFI es una reacción adversa que ocurre después de la inmunización (vacunación) .
Cabe señalar que estas autoridades están siendo influenciadas indirectamente. Al parecer, las reacciones adversas graves deben notificarse horas o días después de la vacunación (no semanas ni meses), mientras que las reacciones adversas leves pueden notificarse meses después. Esto podría ser una manipulación para priorizar las señales de seguridad aceptadas en beneficio de los fabricantes, desviando la atención de los efectos secundarios graves, permanentes y de aparición tardía, como la inmunosupresión inducida por la vacuna, los trastornos del espectro autista, el cáncer y las muertes tardías debidas a afecciones inflamatorias prolongadas y trastornos autoinmunes. Si un niño fallece, por ejemplo, tres semanas después de la vacunación, probablemente se considerará que no existe un vínculo causal con la vacuna, ya que la muerte podría no ajustarse a los criterios preestablecidos por la OMS.
Requisitos de la OMS para WLA al subcontratar tareas.
Si un proveedor externo de WLA tiene acuerdos técnicos regulatorios con terceros para la realización de tareas, el ejercicio de evaluación de riesgos puede extenderse a estos, dependiendo de la importancia que la OMS otorgue a las actividades subcontratadas. Se espera que existan contratos por escrito con las organizaciones subcontratadas, aprobados (¿por la OMS?) para el tipo de actividad regulatoria que se realiza.
Los contratos deben definir claramente: los deberes y responsabilidades de cada parte; el proceso de toma de decisiones para la emisión, renovación o rescisión de contratos de servicios subcontratados; los procedimientos establecidos e implementados para la gestión de las actividades subcontratadas; y los procedimientos para el manejo de los intercambios de comunicación .
De este modo, la OMS controla las decisiones financieras y técnicas de estas autoridades reguladoras.
“La entidad contratante potencial es responsable de evaluar periódicamente —mediante el seguimiento continuo de todas las actividades subcontratadas— la capacidad técnica, material, humana y financiera, así como las instalaciones, el equipo y la tecnología de la(s) organización(es) contratada(s). La organización contratada no debe subcontratar a terceros el trabajo que le ha sido asignado en virtud del contrato sin la previa evaluación y aprobación de los acuerdos por parte de la entidad contratante.”
Parece evidente que estas autoridades reguladoras nacionales, incluidas las empresas subcontratadas y afiliadas, operan bajo el mando de la OMS, y no bajo un control democrático con los principios asociados de rendición de cuentas pública y transparencia.
Declaración de intereses y obligación de confidencialidad
Antes de que se inicien las actividades relacionadas con la evaluación del desempeño, todos los miembros del equipo de la OMS que participen en el ejercicio de evaluación del desempeño para una RA (WLA) específica deben firmar acuerdos de confidencialidad y declaraciones de intereses, excepto los empleados de la OMS.
En otras palabras, los empleados de, por ejemplo, el Instituto Paul Erlich de Alemania o la TGA de Australia no pueden revelar detalles sobre la evaluación del desempeño y otros aspectos.
Los acuerdos de confidencialidad y las declaraciones de intereses debidamente cumplimentados y firmados deberán ser evaluados y archivados por la Secretaría de la OMS antes de la actividad de evaluación de riesgos, de conformidad con los procedimientos pertinentes de la OMS. Los formularios firmados estarán disponibles en la OMS y podrán compartirse con las autoridades competentes si fuera necesario .
¿Quién puede decidir qué es necesario?
¿Es soberano un país si firma este tipo de acuerdos con una organización no gubernamental, una ONG, gobernada por autoridades no electas?
División de responsabilidades
La propia autoridad regional, por ejemplo la EMA o la FDA de EE. UU., es responsable de:
• Designar uno o más coordinadores para coordinar las actividades relacionadas con la evaluación.
• Designar a funcionarios que tendrán acceso a la plataforma segura de la OMS para el intercambio de información.
Compartir con la OMS toda la información y los documentos necesarios a través de la plataforma segura de intercambio de información u otros medios acordados, incluidos, entre otras cosas, los códigos/normas/directrices nacionales, los procedimientos pertinentes y los datos específicos de los documentos seleccionados para su evaluación.
· Proporcionar al equipo de la OMS acceso a todos los datos e información relevantes durante toda la evaluación.
• Proporcionar las aclaraciones y explicaciones necesarias en respuesta a las preguntas del equipo de la OMS.
• Obtener y asegurar el consentimiento necesario de todas las partes interesadas para compartir la información pertinente con la OMS.
Cadena de mando
La Secretaría de la OMS es responsable de la sede central de la OMS, las oficinas regionales y las oficinas en los países (Anexo 6, página 243).
La sede central de la OMS, en colaboración con las oficinas regionales de la OMS y las oficinas nacionales pertinentes, es responsable de:
• Establecer y mantener herramientas y bases de datos para evaluaciones.
• Seleccionar y elaborar una lista de expertos cualificados de la OMS.
· Capacitar a expertos de la OMS para mantener el control sobre los procesos y las autoridades regionales y nacionales afiliadas a la OMS.
• Crear un sitio web específico para cada país en la plataforma de intercambio de información de la OMS para la evaluación y cargar toda la documentación pertinente para su acceso y archivo.
• Selección de los miembros del equipo de la OMS de la lista de expertos cualificados para llevar a cabo la evaluación en nombre de la OMS.
• Elaborar los acuerdos contractuales necesarios.
VigiBase y el Centro de Monitoreo de Uppsala (UMC).
Una de las bases de datos en uso es VigiBase, desarrollada, suministrada y actualizada por la OMS-UMC. Según su propio sitio web, el Centro de Monitoreo de Uppsala (UMC) en Suecia es una fundación independiente, autofinanciada y sin fines de lucro que gestiona el programa internacional de monitoreo de medicamentos de la OMS como centro colaborador de la OMS (WHOCC).
VigiBase es la base de datos mundial de la OMS que recopila informes sobre reacciones adversas a medicamentos y vacunas. El sitio web de UMC indica que UMC financia sus propias operaciones.
“Al proporcionar productos y servicios de farmacovigilancia a diversos organismos externos, la financiación de sus propias operaciones garantiza su independencia intelectual y científica.”
La OMS-UMC no está sujeta a las leyes de libertad de información. Por lo tanto, no es posible acceder a datos sobre, por ejemplo, reacciones adversas a las vacunas contra la COVID-19, ya que la UMC no está obligada a cumplir con las leyes de acceso público a la información.
¿Cómo es posible que la OMS-UMC no esté sujeta a las leyes de publicidad, y cómo es posible que no exista un control democrático sobre la UMC, cuando los datos provienen de múltiples países?
Según la OMS-UMC, investigan las reacciones adversas (RAE) analizando los ensayos clínicos basados en el proceso 1 de los ensayos de fase 3 y el folleto del producto, que también se basa en los ensayos clínicos primarios de fase 3 (proceso 1). Si los “expertos” de la UMC encuentran efectos secundarios en estos, los aceptan como eventos adversos .
En otras palabras, si los informes de las autoridades regionales a través de VigiBase contienen reacciones adversas o señales de seguridad que no se ajustan a las definiciones de EAPI (preguntas de PE) ni figuran en el resumen del producto, no pueden considerarse biológicamente plausibles, es decir, se clasifican como sin relación causal. Por lo tanto, es muy probable que se trate de un proceso de selección preliminar en el que se descartan algunas de las reacciones adversas notificadas que no están incluidas en el resumen de las características del producto. Como resultado, las reacciones adversas pueden volverse muy raras, a pesar de los informes.
Si analizamos en detalle un producto concreto, como las inyecciones de ARNm contra la COVID-19 de Pfizer (Comirnaty) , cabe destacar que la vacuna comercial final no siempre coincide con la que se menciona en el resumen de las características del producto. Esto se desprende de la respuesta a una solicitud de acceso a la información presentada ante la Agencia Danesa de Medicamentos (número de caso 2024024182).
La Agencia Danesa de Medicamentos confirma que, específicamente para Comirnaty de Pfizer (vacuna contra la COVID-19) , no se han realizado ensayos clínicos aleatorios controlados con placebo en humanos con material del proceso 2, el producto terminado de producción masiva que se administró a más de la mitad de la población mundial.
En la misma respuesta, la Agencia Danesa de Medicamentos escribe:
“No es inusual que una empresa farmacéutica realice cambios en su proceso de fabricación durante el desarrollo de un medicamento o vacuna, y Comirnaty evaluó, mediante su aprobación, que los cambios en el proceso de fabricación eran aceptables y no tenían ningún impacto en la seguridad ni en la eficacia de la vacuna.”
Por lo tanto, es común que el producto final administrado se fabrique utilizando un proceso diferente al del producto que ha sido aprobado.
Por lo tanto, el resumen de las características del producto para las vacunas se basa generalmente en los procesos iniciales (fase 3), no en los procesos de fabricación comercial finales, ni, aparentemente, en los efectos secundarios notificados.
En la mayoría de los países, el resumen de las características del producto se utiliza para informar a los profesionales sanitarios que administran las vacunas.
La pregunta sigue en pie: ¿Se obtendrá legalmente el consentimiento informado si la información del folleto no se corresponde con el producto final destinado al usuario?
Un documento de la FDA de 2019 muestra que la mayoría de los Estados miembros, incluida la región del Pacífico, ya están armonizados con la base de datos de Uppsala, VigiBase. El documento se adjunta en formato PDF al final del artículo, ya que el enlace ya no funciona (fuente 978929…pdf).
¿Qué papel desempeña el experto de la OMS en relación con las visitas de evaluación nacionales (PE)?
Un experto de la OMS es designado por la OMS y, según el “código de conducta para expertos de la OMS” (página VIII), tiene las siguientes afiliaciones:
“El experto deberá respetar el carácter confidencial de las deliberaciones del comité o de las reuniones, así como la función de asesoramiento que le asigne la OMS, y no deberá hacer declaraciones públicas sobre el trabajo del comité o de las reuniones ni sobre su propio asesoramiento.”
El experto también se compromete a tener en mente “ los mejores intereses de la OMS, en lugar de representar las opiniones de sus empleadores, otras instituciones o gobiernos ”.
Por lo tanto, no cabe duda de que los expertos de la OMS trabajan para la OMS y no para las autoridades democráticas nacionales (AND), aunque puedan estar empleados por ellas y, por consiguiente, pagados por los contribuyentes de las respectivas democracias.
De este modo, la OMS ejerce un control casi parasitario sobre la organización anfitriona , en este caso las autoridades reguladoras nacionales. En este sentido, la estructura y los términos del Acuerdo de Licencias de la OMS (WLA) son muy similares a los de los Centros Colaboradores de la OMS (WHOCC), como se mencionó anteriormente. Los contratos deben ser firmados por la autoridad regional o nacional y por la OMS.
Así pues, UMC (VigiBase) funciona aparentemente como un caballo de Troya para la OMS y sus propietarios. Todas las autoridades reguladoras de medicamentos suministran datos a UMC.
Soberanía nacional y derecho público
Esta obligación de remitir los casos a la OMS para los centros colaboradores (WHOCC) y las autoridades afiliadas a la OMS (WLA) constituye una clara violación de las leyes de soberanía nacional y entra en conflicto con la legislación nacional sobre acceso público, como se evidencia en casos como las solicitudes de acceso a documentos. Los empleados que deben responder a las solicitudes de acceso a documentos de los ciudadanos entran en conflicto con la legislación nacional, ya que están sujetos a acuerdos de confidencialidad contractuales. Esto convierte dichos contratos en ilegales, puesto que estos empleados, en la práctica, trabajan para una potencia extranjera.
Ejemplo.
En otoño de 2025, el Consejo Mundial de la Salud de Escandinavia solicitó acceso a documentos a los tres centros colaboradores de la OMS en Dinamarca en aquel momento: la Universidad Técnica de Dinamarca (DTU), la Universidad de Copenhague (KU) y el Instituto Parker (PI). La KU y el PI no han respondido a pesar de las reiteradas solicitudes. Recibimos la siguiente respuesta preliminar de la DTU:
La DTU le informa que no es posible tomar una decisión sobre su caso dentro del plazo legal. Esto se debe a que la DTU está evaluando si se pueden divulgar todos los documentos que ha identificado en relación con su solicitud. En este sentido, estamos aclarando si la DTU debe consultar con terceros antes de tomar una decisión .
¿Quién podría ser este actor externo? ¿La sede de la OMS?
Respuesta de WCH-Escandinavia:
“ Si se requiere consulta externa —por ejemplo, si es necesario consultar a la OMS o a los ministerios antes de la divulgación—, también solicitamos acceso a esta comunicación y una justificación legal para cualquier retención de documentos que consideremos de interés público.”
Esta solicitud no fue respondida al momento de redactarla.
Conclusión
En resumen: Las autoridades nacionales de regulación de medicamentos parecen haber sido intervenidas por la OMS. Esto parece haberse gestado a la sombra de la pandemia de Covid, que aparentemente sirvió de pretexto para una “toma de poder global”.
De este modo, la OMS controla la notificación de efectos adversos. Al parecer, las señales de seguridad son filtradas por la OMS y no por las autoridades nacionales en el caso de todos los medicamentos y vacunas.
Dado que la OMS está controlada por intereses de la industria, cabe preguntarse si la OMS puede ser imparcial en este control regulado y detallado de las autoridades nacionales.
Un artículo de The Guardian revela que más del 60 % de los donantes de la OMS son anónimos y están sujetos a condiciones. Análisis previos han demostrado que la industria farmacéutica, ya sea directamente o a través de fundaciones, se encuentra entre los mayores donantes y quienes imponen las condiciones, mientras que los Estados miembros representan una proporción mínima de los donantes. Cabe suponer que la influencia y las políticas van de la mano del dinero.
Es evidente que existen enormes conflictos de intereses, y resulta incomprensible que nuestros políticos electos hayan permitido que se produzca este secuestro de las autoridades reguladoras.
Es inaceptable que las autoridades reguladoras estén controladas por aquellos a quienes se supone que deben controlar.
Es necesaria una comisión independiente que investigue esta usurpación de poder y determine quién es el responsable de la cesión de soberanía.
¿Quieres profundizar más?
Fuentes:
https://www.worldcouncilforhealth.org/open-letter-to-the-trump-administration/
https://foedevarestyrelsen.dk/Media/638610430209006066/AMR-handlingsplan 2024 web.pdf
https://www.who.int/publications/i/item/9789241509763
https://iris.who.int/server/api/core/bitstreams/8ba0873d-fab7-4cd9-aaee-e3e43be037ed/content
https://www.wch-scandinavia.org/en/post/answers-from-the-danish-medicines-agency-lmst
https://www.who.int/publications/i/item/9789241516990
Centros de Control de la OMS australianos para el 10 de marzo de 2026
Cicalá. SV40 en roedores: https://pmc.ncbi.nlm.nih.gov/articles/PMC1886912/
Plan de acción de la Administración Veterinaria y Alimentaria Danesa para la RAM: https://foedevarestyrelsen.dk/Media/638610430209006066/AMR-handlingsplan 2024 web.pdf
Plan de acción mundial de la OMS para la resistencia a los antimicrobianos. https://www.who.int/publications/i/item/9789241509763
Resumen de los Centros de Coordinación de la OMS daneses: https://who.my.site.com/ecc/s/database-search?name=&city=&title=&country=a0M3X00001Fwg3fUAB®ion=&status=&activity=&initiator=&responsibleOfficer=&technicalCounterpart=&designationDateValue=&startDateValue=&endDateValue=&designationEndDate=&cchead=&referenceNumber=&ref2=&focus=&tor=
Información general del país Autoridades vinculadas a la OMS:
https://cdn.who.int/media/docs/default-source/medicines/regulatory-systems/wla/list_of_wla.pdf?sfvrsn=1f6c2140_49&download=true
Debido a la eliminación de enlaces, los siguientes tres documentos (en formato PDF) estarán disponibles en WCH-Scandinavia.org en el mismo artículo “WHO controla a quién” en la sección Blogs:
- El acuerdo entre el Ministerio de Asuntos Exteriores danés
- Documento 978929…Región del Pacífico Sur.
- Guía de la OMS sobre el cambio climático
Traducido del original: WHO controls whom? por Jeanne A. Rungby