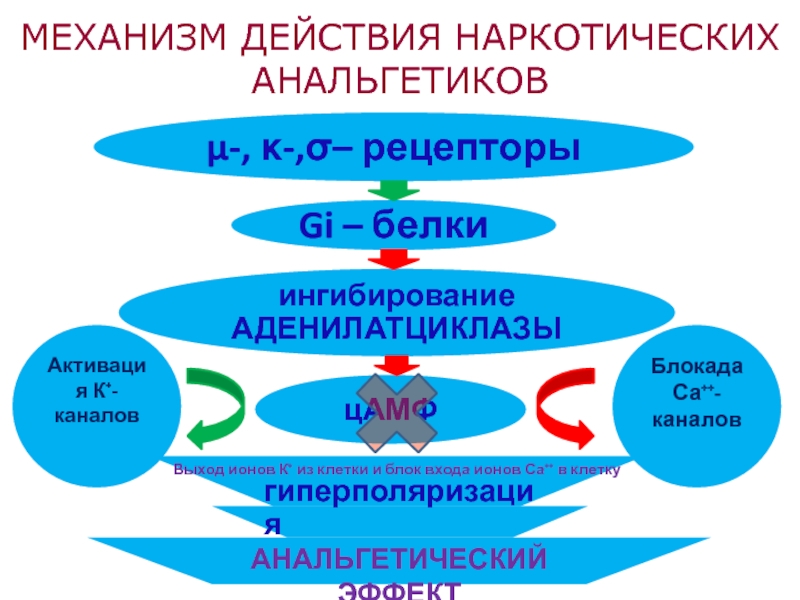
Механизм Действия Анальгетика

⚡ 👉🏻👉🏻👉🏻 ИНФОРМАЦИЯ ДОСТУПНА ЗДЕСЬ ЖМИТЕ 👈🏻👈🏻👈🏻
Автор: Sinitski ·
Опубликовано 2017/04/10 · Обновлено 2018/01/04
Опиоидные анальгетики – это вещества природного или синтетического происхождения, которые являются агонистами опиоидных рецепторов, то есть стимуляторами эндогенных опиопептидов в центральной нервной системе (ЦНС).
Как уже говорилось выше, опиоидные анальгетики являются агонистами опиоидных рецепторов . Разберем подробнее опиоидные рецепторы.
Опиоидные рецепторы разделяются на три основных подтипа:
В обезболивании участвуют все эти три типа рецеторов. Расположены они в ЦНС, но самую главную роль играют именно ОР3 (мю) рецеторы. Возбуждение мю рецепторов приводит к угнетению дыхания, эйфории и физической лекарственной зависимости. Периферические опиоидные рецепторы регулируют моторику кишечника. При стимуляции опиоидных рецепторов кишечника развивается обстипация (запор).
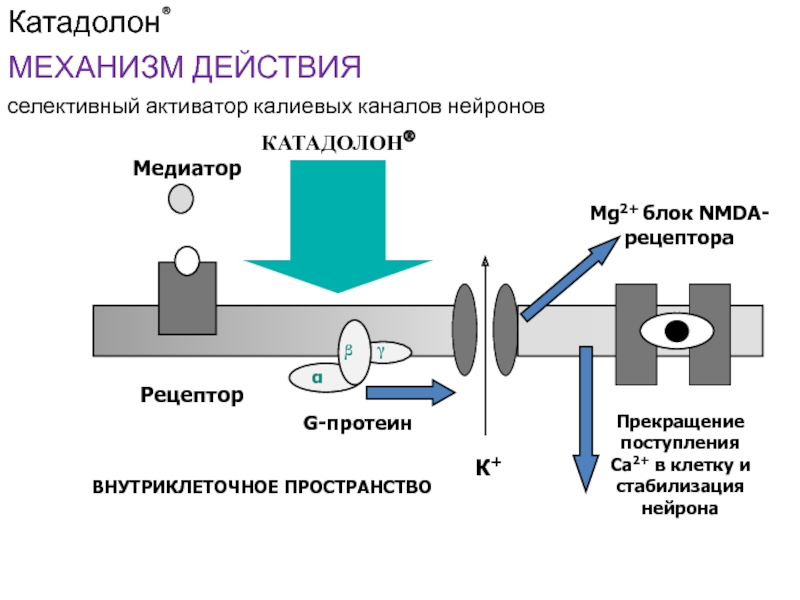
Все типы опиоидных рецепторов связаны с особым G-белком. Передача сигнала с мембранного рецептора осуществляется через:
Опиоидные анальгетики нарушают нейронную передачу болевого импульса за счет того, что уменьшается выброс в синаптическую щель медиаторов боли (глютамат, ацетилхолин, норэпинефрин, серотонин и субстанция П) и стабилизируется постсинаптическая нейрональная мембрана из-за открытия калиевых каналов.
В последние годы обнаружено, что опиоидные анальгетики (эндогенные и экзогенные) могут вызывать анальгезию посредством действия также и на периферические ткани. В окончаниях периферических чувствительных нервов обнаружены мю-рецепторы. Боль воспалительного характера тоже чувствительна к периферическому действию опиоидных анальгетиков. Так, назначение в коленный сустав опиодных анальгетиков при артроскопической хирургии на коленном суставе приносило уменьшение боли. Поэтому сейчас ведутся работы по поиску опиоидных анальгетиков с селективным периферическим действием для лечения воспалительных болей.
Эндогенные опиоидные анальгетики отличаются по сродству к опиоидным рецепторам – леу-энкефалин имеет высокое сродство к дельта рецепторам, а динорфин – к каппа. С целью снижения риска лекарственной зависимости и угнетения дыхания целенаправленно производился поиск лекарственных веществ с преимущественным действием на каппа-рецепторы. Примером таких веществ являются, например, опиоидные анальгетики буторфанол и налбуфин. Однако они вызывают дисфорию и довольно слабы.
Опиоидные анальгетики и их антагонисты могут разделяться:
Для врача-практика незаменима именно вторая, так называемая клиническая классификация.
Природные опиоидные анальгетики (производные фенантрена): морфин, кодеин.
Синтетические опиоидные анальгетики :
Смешанные агонисты-антагонисты и частичные агонисты : бупренорфин, буторфанол, пентазоцин, трамадол.
Чистые антагонисты опиоидных рецепторов : налоксон, налмефен, налтрексон, альвимопан, метилнатрексон.
Чистые агонисты опиоидных рецепторов устраняют эффекты опиоидных анальгетиков. Налоксон и налмефен незаменимы при угнетении дыхания, вызванном передозировкой опиоидных анальгетиков, налтрексон – при лечении опиоидной наркомании, алкоголизма. Последние два вещества не проникают в ЦНС и испольщуются для устранения вызванного опиоидами запора.
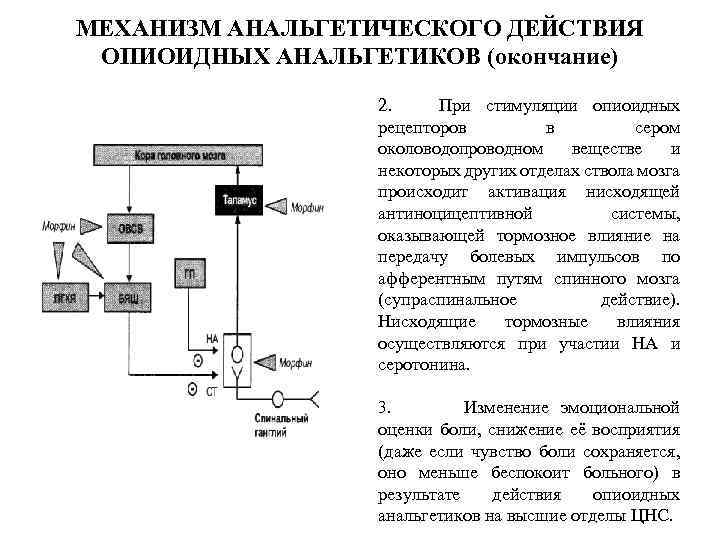
Опиоидные анальгетики устраняют боль путем стимуляции специфических опиоидных рецепторов, регулирующих передачу и модулирование боли и расположенных преимущественно в головном и спинном мозге. Они тормозят освобождение возбуждающих медиаторов из афферентных нейронов и угнетают передачу болевого импульса в дорсальных рогах спинного мозга, а на супраспинальном уровне – нарушают передачу и модулирование боли.
Особенно важный момент это модулирование боли в нисходящих путях, включающих передний мозговой киль, серую периакведуктуальную зону и locus ceruleus. Опиоидные анальгетики подавляют все эти нейрона и способствуют освобождению эндогенных опиопептидов, которые, в свою очередь, действуют и на другие, чем сами опиоидные анальгетики, типы рецепторов. Поэтому селективных к одному типу рецепторов анальгетиков нет.
Прототипом опиоидных анальгетиков является морфин . Другие опиоидные анальгетики вызывают только лишь морфиноподобные эффекты. Все эффекты морфина можно разделить на центральные и периферические.
Анальгезия , вызванная изменением восприятия боли, изменением реакции на боль ( боль воспринимается как что-то постороннее) и эйфорией (сильнейшим чувством удовлетворения и благополучия). У здоровых людей, которые не имеют боли, иногда может быть и дисфория. Наиболее выраженным действием обладают сильные агонисты мю-рецепторов.
Угнетение дыхания , вызванное снижением чувствительности дыхательного центра к углекислому газу. Частота дыхания снижается и при передозировке может быть его остановка (смерть). Снижение частоты дыхания, вызванное морфином полезно при одышке, сопровождающей отек легких (снижается страх пациента от самой одышки). Накопление углекислого газа при урежении дыхания приводит к расслаблению церебральных сосудов и повышению внутричерепного давления (а это опасно при травмах головы).
Подавление кашлевого центра не является пропорциональным анальгетическому действию. Так, слабые опиоидные анальгетики кодеин и дектрометорфан обладают сильным противокашлевым действием.
Сон , которые объясняется последствием устранения болей – пациент успокаивается и засыпает.
Рвота (вследствие стимуляции хеморецепторов пусковой зоны рвотного центра) чаще бывает у пациентов, находящихся в движении, и не сопровожлается неприятными ощущениями. При хроничеком использовании рвоты нет.
Миоз (сужение зрачка), вызванный стимулирующим влиянием парасимпатической иннервации на тонус ядра глазодвигательного нерва. Этот эффект сохраняется при хроническом применении (т.е. отсутствует привыкание). Миоз, брадипнож (редкое дыхание) и кома являются надежными диагностическими симптомами передозировки опиодными анальгетиками.
Судороги. Это крайне редкий эффект меперидина, тримепиридина (промедола) при их передозировке на фоне почечной недостаточности из-за накопления токсических метаболитов.
Ригидность мышц туловища снижает объем дыхательных движений и может нарушить дыхание пациента. Она наиболее выражена при быстром внутривенном назначении больших доз опиоидных анальгетиков с высокой липидной растворимостью (фентанил и близкие к нему вещества). Для снятия ригидности ( причина ее – опиоидные анальгетики действуют на супраспинальном уровне) назначаются курареподобные миорелаксанты.
Запор из-за подавления перистальтики кишечника при одновременном увеличении тонуса гладкой мускулатуры толстого кишечника и спазме анального сфинктера. Все это приводит к замедлению продвижения химуса (пищевого комка), всасыванию воды и к запору. Этот эффект широко используется при поносе неинфекционного происхождения. При диарее опиоидные анальгетики считаются наиболее эффективной группой веществ. Используются родственные по химическому строению с опиоидными анальгетиками лоперамид (имодиум) и дифеноксилат. Они безопасны, так как не проникают в ЦНС и поэтому не вызывают ни эйфории, ни анальгезии, ни наркомании.
Спазм мускулатуры желчевыводящих путей (могут вызвать печеночную колику).
Повышение тонуса мочеточника, детрузора и сфинктера мочевого пузыря , что может усилить течение почечной колики и (при аденоме простаты) вызвать задержку мочи.
Сердечно-сосудистая система изменяется лишь веществами с М-холиноблокирующим действием. Например, тримеперидин (промедол) и меперидин могут вызвать тахикардию . Однако на фоне стресса опиоидные анальгетики могут вызвать небольшую гипотензию из-за выделения гистамина и снижения тонуса сосудодвигательного центра.
Выделение гистамина из тучных клеток приводит к расширению сосудов кожи, из-за чего возможно незначительное снижение АД. Также могут быть кожный зуд, крапивница и бронхоспазм у астматиков.
Снижение выделительной функции почек : уменьшение почечного кровотока и гломерулярной фильтрации.
Снижение тонуса матки , что может вызвать замедление родов. Механизм этого эффекта неизвестен.
Опиоидные анальгетики в абсолютном большинстве хорошо всасываются в ЖКТ , затем они метаболизируются в печени и в виде метаболитов (глюкуронидов и др.) выделяются с мочой. Однако существуют различия в скорости и величине всасывания в ЖКТ (поэтому опиоидные анальгетики чаще всего назначаются парентерально, это более точный метод) и особенностях метаболизма печени. Так, например, назначение большой дозы морфина на фоне почечного повреждения приводит к накоплению в организме нейротоксичного метаболита морфина (морфин-3-глюкуронид), который может вызвать судороги. Подобный эффект может быть и при накоплении метаболитов меперидина или его аналогов. При повторных назначениях больших доз опиоидных анальгетиков (особенно с высокой липофильностью, типа фентанила) возможно накопление их в жировой ткани, что создает опасность токсических эффектов.
Угнетающие эффекты опиоидных анальгетиков (в том числе и анальгезия) усиливаются:
Различаются опиоидные анальгетики друг от друга по длительности действия, выраженности (силе) отдельных эффектов, риску лекарственной зависимости.
По длительности действия опиоидные анальгетики подразделяются на вещества:
По риску лекарственной зависимости опиоидные анальгетики подразделяются на вещества, назначение которых сопряжено:
Опиоидные анальгетики применяются в слудющих случаях:
Cильная острая боль (инфаркт миокарда, травмы, ожоги, колики) и сильная хроническая боль невоспалительного характера (рак). Обезболивание должно быть адекватно силе боли и время от времени пересматриваться в сторону увеличения или уменьшения дозировок. например, при печеночной или почечной колике после введение опиоидов боль может, наоборот, увеличиваться, а не уменьшаться. Это объясняется увеличением спазма гладкой мускулатуры. Поэтому при коликах важно увеличить дозу опиоидов, которая и вызовет эффективное обезболивание. При неоперабельном раке возможно даже пойти на риск создания лекарственной зависимости у таких пациентов (большие дозы веществ, постоянное введение), но добиться эффективного обезболивания.
В иных случаях предпочтение отдается сильным агонистам (при острой боли) и частичным агонистам при хронической боли (из-за малого риска наркомании). Следует учитывать, что частичные агонисты уступают по эффективности сильным агонистам
Обезболивание при хирургических операциях (премедикация и непосредственно во время операции). Особенно часто используются фентанил и его производные.
Отек легких (уменьшение частоты дыхания снижает страх пациента) и снижение преднагрузки и постнагрузки на сердце (из-за расширения венозных и артериальных сосудов). Наиболее часто применяют морфин.
Боль при родах . В СНГ используется аналог зарубежного меперидина – тримеперидин (промедол). Он слабо, по сравнению с морфином, угнетает дыхание плода. Кроме того, его метаболизм (быстрое деметилирование) безопасен для плода, по сравнению с метаболизмом морфина (медленная конъюгация в печени). В отличие от других опиоидных анальгетиков тримеперидин и меперидин не ослабляют, а усиливают родовую деятельность.
Диарея (не инфекционная): дифеноксилат (реасек), лоперамид (имодиум).
Опиоидные анальгетики оказывают побочные эффекты, которые являются продолжением их фармакологического действия: угнетение дыхания, запор, лекарственная зависимость, тошнота, рвота и (токсические дозы тримеперидина, меперидина, трамадола, реже – морфина) судороги. У агонистов могут быть психотомиметические реакции (галлюцинации, ночные кошмары и тревога).
Соответственно побочным эффектам, опиоидные анальгетики противопоказаны при:
Причина лекарственной зависимости до конца не выяснена. Среди возможных причин – изменение функционирования опиоидных рецепторов при постоянном назначении опиоидных анальгетиков (снижение числа рецепторов и их сродства к агонистам), дисфункция структурного взаимодействия цепочки: рецептор – G-белок – вторичные клеточные медиаторы – ионные каналы. В частности, большое значение придается специфическому комплексу с ионными каналами – NMDA-рецептору (обнаружено, что кетамин, антагонист NMDA-рецептора блокирует развитие привыкания и физической зависимости).
Характеристика лекарственной зависимости опиодной наркомании. Она очень тяжелая (психическая и физическая) и сопровождается выраженным привыканием (толерантностью) ко всем эффектам опиоидных анальгетиков, за исключением миоза и запоров. Зависимому от них человеку (наркоману) требуется все большая и большая доза опиоидных анальгетиков, а прекращение их приема вызывает крайне тяжелый (но обычно не смертельный абстинентный синдром).
Абстинентный синдром – это признак наличия физической лекарственной зависимости. Вначале (первые 12 часов после приема последней дозы морфина) возникают признаки психической зависимости, нервозность, потливость и жажда наркотика. Они смягчаются назначением плацебо. Затем появляются признаки тяжелой физической зависимости, в большинстве своем связанные с нарушением функции вегетативной нервной системы: мидриаз, тахикардия, гусиная кожа, кишечная колика, боли в мышцащ, рвота, понос, одышка, лихорадка, зевота, тремор, чихание, слезотечение, а также анорексия и депрессия. У морфина максимум абстиненации падает на 1-2 день, а ее длительность около 5 дней. В большинстве случаев наркоман ее не выдерживает и возвращается к наркотикам.
Лечение наркомании проводят метадоном. Это длительнодействующий сильный агонист опиоидных рецепторов, близкий к морфину. Пик абстинентного синдром (значительно более мягкого, чем у морфина) – первая неделя, длительность – три недели. Вместо метадона все чаще используют частичный агонист опиоидных рецепторов бупренорфин. Оба вещества назначают в таблетках с постепенным снижением суточной дозы до полной их отмены. Длительнодействубющий (48 часов) антагонист опиоидных рецепторов налтрексон назначается внутри при лечении наркоманов. Он устраняет смысл приема наркотиков-опиоидов наркоманами, находящимися на лечении, так как блокирует опиоидные рецепторы и предотвращает все эффекты, которые осуществляют опиоидные анальгетики. Для лечения наркоманов недавно стал использоваться клонидин (клофелин), который устраняет симптомы гиперактивности симатической нервной системы, наблюдаемые при опиоидной абстиненции.
Острое отравление морфином и его аналогами устраняется внутривенным введением антагониста опиоидных анальгетиков налоксона. В течение 30 секунд он вытесняет опиоидные анальгетики из клеток дыхательного центра и восстанавливает нормальное дыхание отравленного человека. Действие его непродолжительно (1-2 часа), что требует повторного введение налоксона при отравлении длительнодействующими опиоидными анальгетиками. В последнем случае предпочтителен налмефен (длительность действия около 8-10 часов), который является производным налтрексона, но назначается только внутривенно.
Морфин относится к группе опиоидные анальгетики – их прототип. Он медленно и в индивидуально изменчивом количестве всасывается внутрь, подвергаясь сильному эффекту первого прохождения. Поэтому его парентеральное назначение дает более предсказуемый эффект. Действует длительно (около 4-6 часов). Печень новорожденных слабо, по сравнению с взрослыми, метаболизирует (конъюгация с глюкуроновой кислотой) метформин. ИЗ-за этого морфин нельзя назначать для обезболивания родов и новорожденным.
Практически идентичен морфину по свойствам, хотя не сходен с ним по строению, пиритрамид. Единственное отличие от морфина гидроморфона и оксиморфона – более длительное действие. Омнопон – новогаленовый препарат опия, содержащий морфин и другие алкалоиды опия, включая папаверин. Действует аналогично, но слабее морфина. Однако спазм гладкой мускулатуры моче и желчевыводящих путей меньше, так как он содержит в своем составе спазмолитик – папаверин.
Тримеперидин (промедол) относится к группе опиоидные анальгетики, он слабее морфина и меньше угнетает дыхательный центр. ПОэтому это вещество считается препаратом выбора в акушерстве и педиатрии. Оно обладает слабыми М-холиноблокирующими свойствами поэтому не вызывает такого сильного спазма гладкой мускулатуры, как морфин, может вызывать тахикардию, сухость во рту и расширение зрачков. Он не имеет заметного противокашлевого действия, что может быть полезно у пациентов с заболеваниями легких, когда надо сохранить кашлевой рефлекс. также не обладает клинически значимым обстипирующим эффектом. Он лучше морфина всасывается в ЖКТ, но уступает ему по силе и длительности действия (2-4 часа). Тримеперидин близок по строению и свойствам к зарубежному аналогу меперидину. Характерный эффект передозировки этих веществ – нейротоксичность (тремор и судороги).
Метадон относится к группе опиоидные анальгетики, полностью всасывается в ЖКТ, обладает более длительным действием (период полувыведения около 24 часов), чем морфин и не уступает ему по силе, но из-за медленного наступления эффекта вызывает меньшую эйфорию. Длительное действие и хорошая всасываемость при приеме внутрь делают его основным препаратов для освобожления наркоманов от страданий, вызванных абстинентным синдромом (так как из-за длительного действия метадон вызывает значительно более мягкий абстинентный синдром, чем морфин и другие сильные агонисты опиоидных рецепторов). При этом метадон дают в постепенно убывающей суточной дозе. Леворфанол очень похож по свойствам на метадон, но более сильный.
Фентанил относится к группе опиоидные анальгетики, действует значительно сильнее, чем морфин, но кратковременно ( до 30 минут). Часто используют вместе с нейролептиков дроперидолом, который усиливает его действие. Эта комбинация используется для обезболивания хирургических операций (нейролептаналгезия). Близки по свойствам к фентанилу фальентанил, суфентанил, ремифентанил.
Кодеин относится к группе опиоидные анальгетики – слабый аналог опиоидных рецепторов, поэтому редко и только при длительном применении в больших дозах создает угрозу развития наркомании. как и другие слабые агонисты (гидрокодон, оксикодон, пропоксифен) применяется в комбинации с парацетамолом или аспирином для устранения несильных болей. Отлично всасывается в ЖКТ. Высоко эффективен при кашле в тех дозах, которые не вызывают анальгезии, однако в настоящее время он вытеснен декстометорфаном, так как последний вообще не вызывает наркомании.
Пентазоцин относится к группе опиоидные анальгетики – действует кратковременно, всасывание из ЖКТ неполное. Он относится к агонистам-антагонистам опиоидных рецепторов, то есть одни рецепторы (каппа) возбуждает, а другие (мю) блокирует. В отличие от морфина пентазоцин вызывает тахикардию и повышение АД (противопоказан при ишемической болезни сердца). У наркоманов вызывает абстиненцию, то есть действует как антагонист опиоидных рецепторов. Часто вызывает дисфорию (из-за возбуждения сигма рецепторов), поэтому редко развивается наркомания. Химически близок к пентазоцину дезоцин (однако, он прежде всего, агонист мю, а затем каппа рецепторов).
Бупренорфин относится к группе опиоидные анальгетики, имеет большое сродство к мю рецепторам, но возбуждает их слабо. На дельта и каппа рецепторы он действует как антаг
https://optimusmedicus.com/farmakologiya/opioidnye-analgetiki/
http://narkozis.ru/obshhaya-anesteziya/narkoticheskie-analgetiki-klassifikaciyamexanizm-dejstviya-primenenie.html
Смотреть Порно Фильмы Итальянские Старые
Самая Красивая Пизда Порно
Телки В Юбках На Толчке
Опиоидные анальгетики. Виды, механизм действия, …
Наркотические анальгетики классификация,механизм …
Опиоидные анальгетики. Виды, механизм действия, …
Механизм действия наркотических анальгетиков — …
Безопасные анальгетики – механизм действия, принципы ...
Опиоидные анальгетики. Виды, механизм действия, …
Наркотические анальгетики классификация,механизм …
Наркотические анальгетики классификация,механизм …
Механизм действия ненаркотических анальгетиков ...
Наркотические анальгетики классификация,механизм …
Механизм Действия Анальгетика