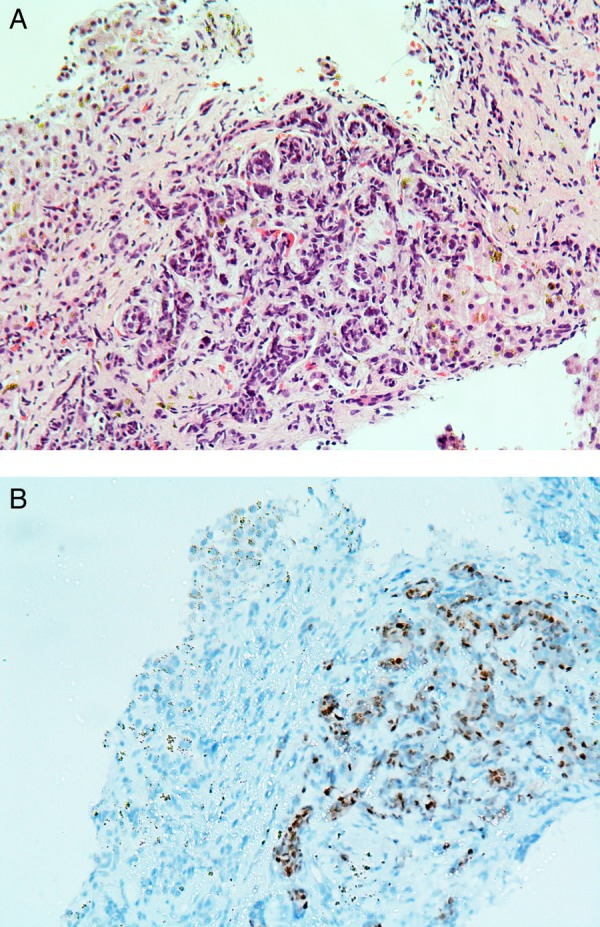
Метастазы и трансаминазы
Трофимовская Наталья, врач-гепатологКлиническая задача без правильного ответа:
На приёме пациент с онкологическим анамнезом, у которого в период или после лечения возникает и в последующем сохраняется бессимптомное повышение “печёночных” показателей. (Уточним, что функция печени остаётся нормальной и признаков портальной гипертензии нет). Круг дифференциальной диагностики кажется очевидным:
- метастатическое поражение печени
- вариант лекарственной токсичности (если лечение проводилось)
- первые проявления PSVD (порто-синусоидальная сосудистая болезнь)
- новое, манифестировавшее заболевание, не связанное с анамнезом (например, вирусная инфекция)
А вот алгоритм понятен не всегда.
Допустим: Мы исследовали у пациента стандартные сывороточные маркеры (вирусные, церулоплазмин, ферритин, НТЖ, аутоантитела, IgG), у него также нет и не было ожирения, ЖКБ, заболевания щитовидной железы. По результатам плановых КТ грудной клетки и брюшной полости: признаков прогрессирования основного заболевания / других интересных находок - нет.
Иначе говоря, в фокусе внимания пункт первый. Вопросы для рассмотрения:
- Может ли повышение показателей предвосхищать появление очевидных метастатических очагов
- Можем ли мы рассматривать такое повышение как повод для сокращения интервалов КТ/МР- скрининга
- Существуют ли более чувствительные методики выявления метастазов (микрометастазов?)
- Нужно ли продолжать поиски самостоятельного заболевания печени, проводить дополнительные тесты, или лучше отложить? Если отложить, то на какой срок?
- Насколько этично обсуждать с пациентом вероятность прогрессирования в отсутствие лучевых признаков
Обратимся к литературе:
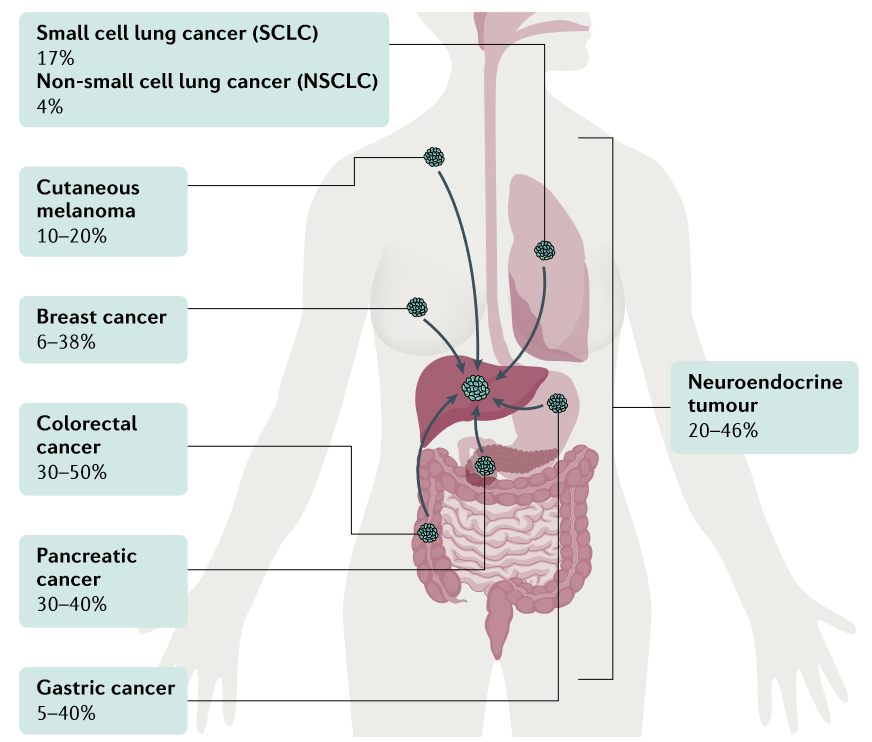
Чаще всего метастатическое поражение печени встречается при колоректальном раке, раке поджелудочной железы, лёгких и при раке молочной железы.
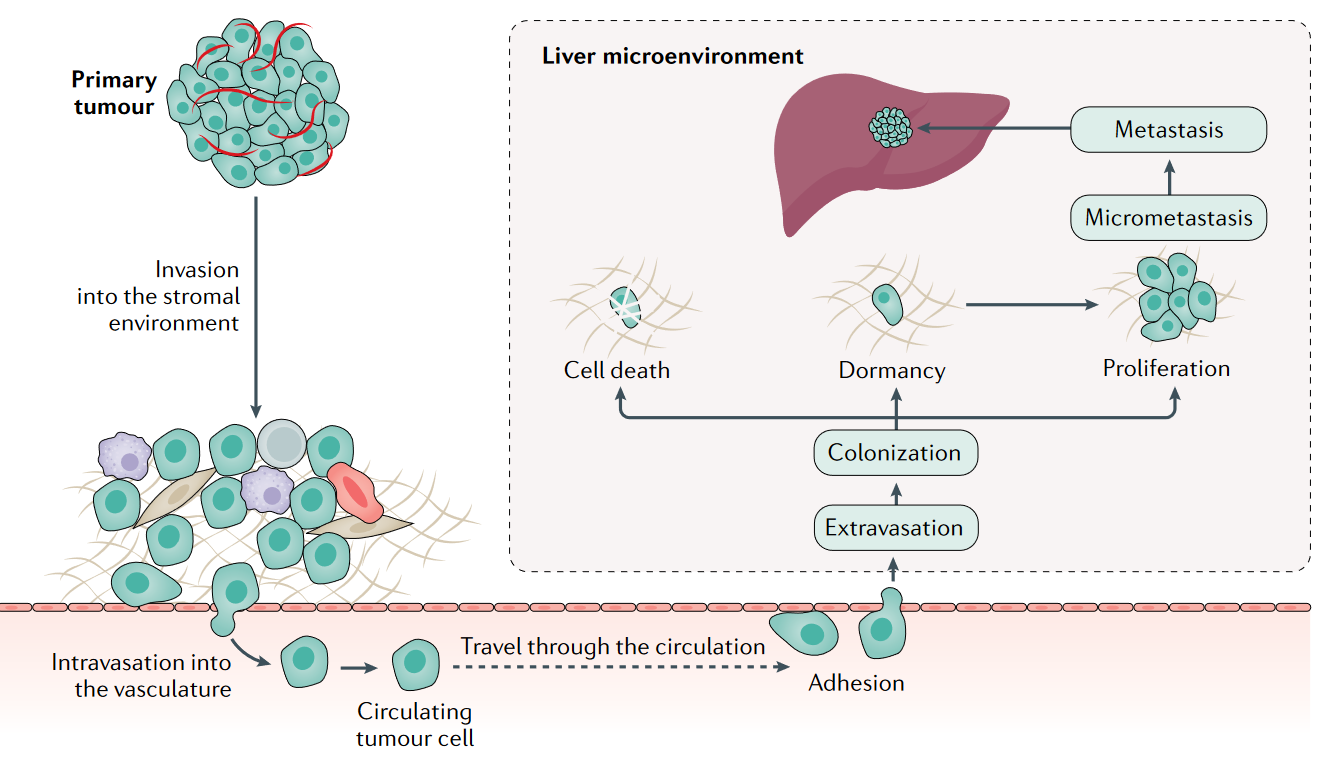
Метастазирование - это процесс в т.ч. гематогенной диссеминации опухолевых клеток, в котором можно выделить основные этапы
- интравазация в микроциркуляторное русло органа-мишени
- экстравазация в окружающие ткани
После экстравазации опухолевые клетки могут погибнуть, замереть или начать активную пролиферацию с образованием исходно микрометастазов, а затем и макро-очагов.
О молекулярных механизмах, определяющих сценарий, подробнее можно почитать ЗДЕСЬ.
Наиболее распространённое определение микрометастазов: конгломерат опухолевых клеток от 0.2 до 2 мм, не определяемый стандартными лучевыми методами.
Таким образом
Аргументация может быть лишь косвенной: в публикациях обнаруживается корреляция между “печёночными” показателями и выживаемостью / отсутствием метастазирования / ответом на терапию.
В большинстве случаев проанализированы пациенты с уже выявленными метастазами, биохимическая активность часто пропорциональна количеству и размеру очагов, и довольно логично коррелирует с прогнозом.
Но попытки проанализировать показатели ДО начала терапии, появления объективных признаков метастазирования или в рамках их полного хирургического устранения (резекции R0) - предпринимались, приведём в качестве примера именно их.
Щелочная фосфатаза и гамма-глутамилтранспептидаза
Оба фермента имеют многогранные взаимоотношения с различными типами рака, широко исследованы и рассматриваются в качестве самостоятельных, независимых прогностический факторов ответа на терапию и течения самого заболевания.
Щелочная фосфатаза неспецифична, имеет изоформы, (эскпрессируется в тканях различных органов в т.ч. почек, кишки), информативна для оценки вероятности метастатического поражения не только печени, но и костной ткани.
Но интересно также, что оба фермента вероятно могут отражать метаболическую активность и скорость пролиферации самих опухолевый клеток. Таким образом более высокие показатели на момент включения пациентов в КИ имеют две основные гипотетические трактовки (помимо самостоятельных заболеваний печени)
- отражают стадию экстравазации опухолевых клеток и микрометастазирования
- отражают активность пролиферации и гематогенной диссеминации опухолевых клеток
Примеры:
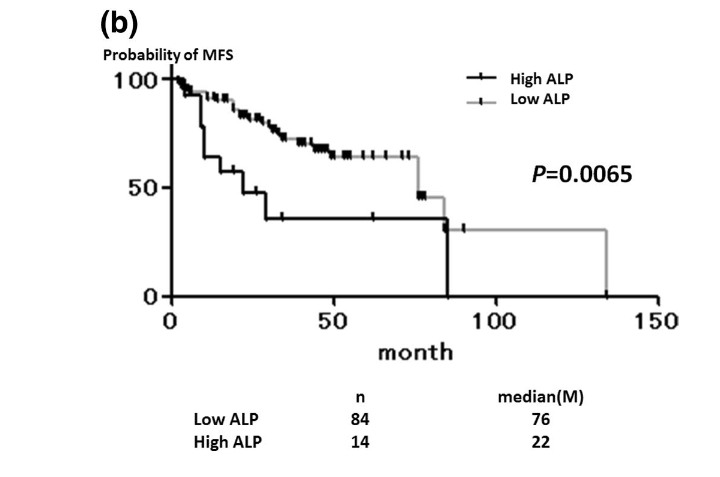
В исследовании пациентов с формально НЕ метастатическим раком предстательной железы (критерий включения) продемонстрирована корреляция между исходным уровнем щелочной фосфатазы и ответом на проводимую терапию / выживаемостью без отдалённых метастазов. Авторы отмечают, что исходный уровень ЩФ мог бы стать потенциальным аргументом в выборе лечебной тактики.
Высокий или низкий уровень ЩФ в данном исследовании определялся как >322 Ед/л или <322 Ед/л соответственно.
ГГТ оказался независимым предиктором прогрессирования у пациентов после R0 - резекции печени по поводу метастазирования колоректального рака, в т.ч. независимо от количества и размера метастазов. То есть вероятность возникновения новых очагов после оперативного лечения оказалась выше, а общая выживаемость - ниже
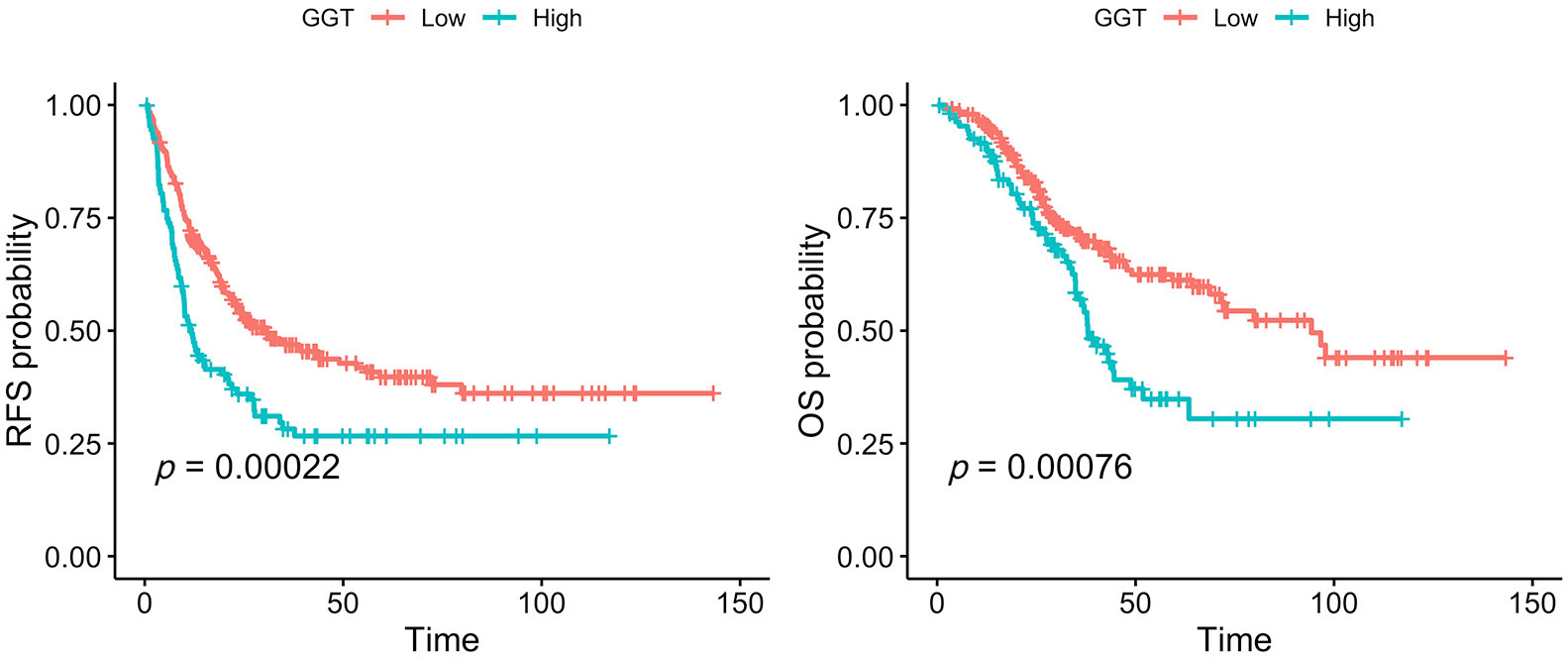
Аналогичные данные были получены в другом подобном исследовании для периоперационного показателя АСТ.
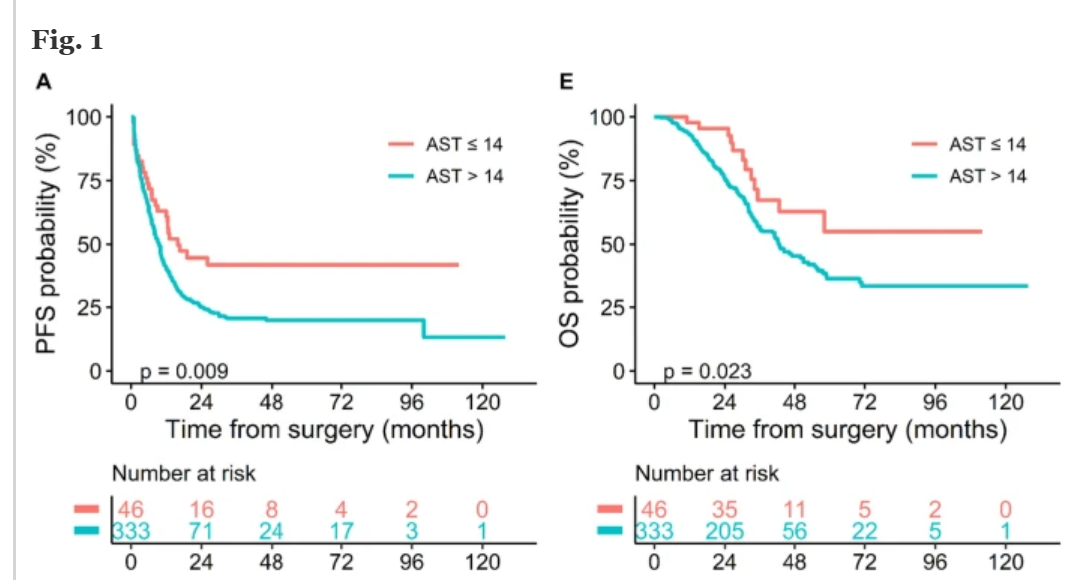
АСТ и АЛТ.
Трансаминазы (преимущественно АСТ) также звучат в ассоциации с пролиферативной активностью опухолевых клеток. Отмечается, что фермент АСТ является важным участником каскадов анаэробного гликолиза, свойственного злокачественным процессам. Поэтому исследовалась роль коэффициента де Ритиса.
В частности, после длительного наблюдения за соотношением АСТ/АЛТ у пациентов с раком предстательной железы была продемонстрирована худшая общая выживаемость пациентов даже с формально неметастатическим заболеванием при показателе коэффициента де Ритиса ≥ 1.467.
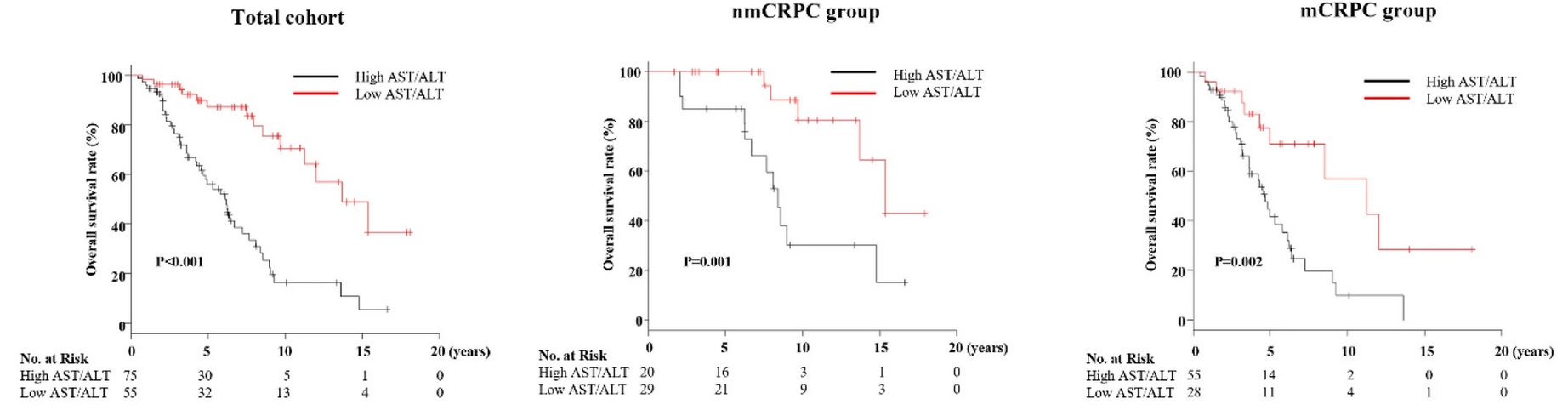
У пациентов меланомой была попытка проанализировать тренд динамики печёночных показателей до обнаружения метастатического поражения. С учётом малой выборки и других ограничений, убедительных выводов не получилось, динамика ГГТ и ЛДГ оказалась более наглядной, чем АЛТ и АСТ, однако в публикации звучит предложение о сокращении интервала наблюдения у пациентов с лабораторными отклонениями.
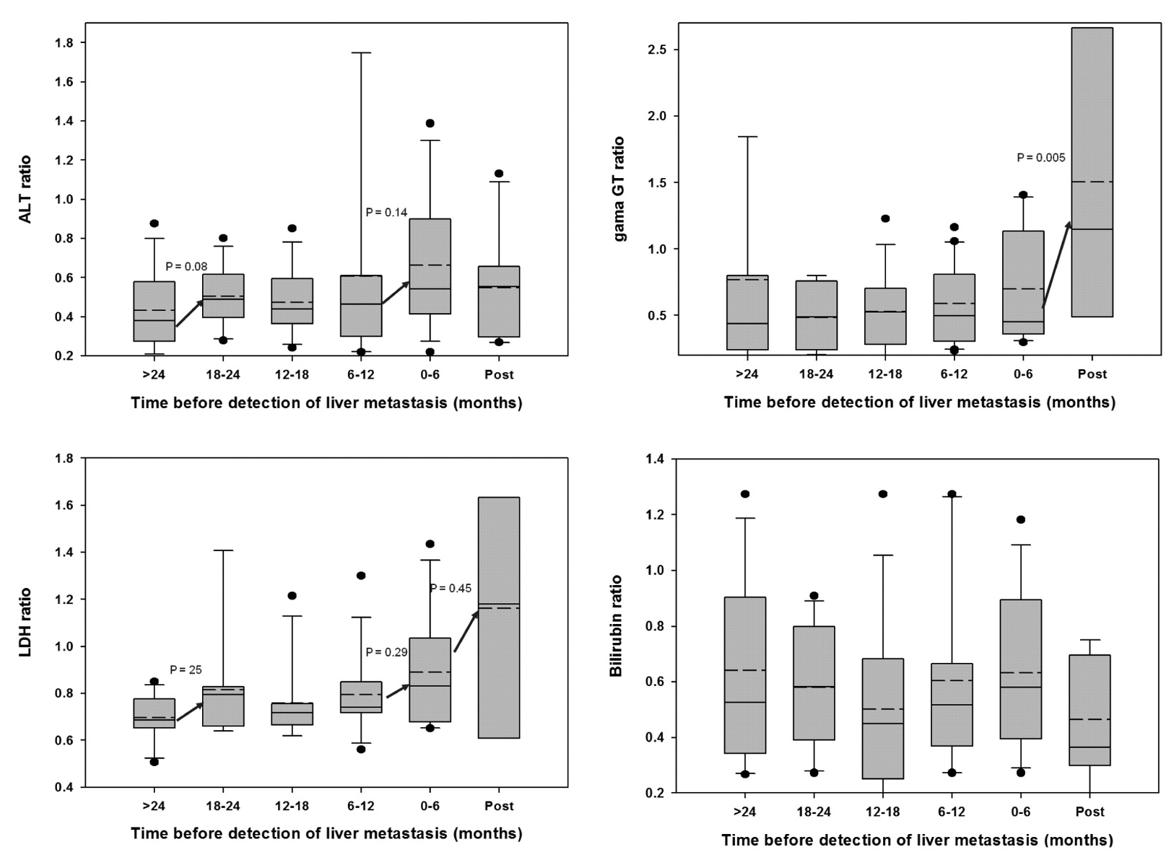
А всегда ли мы находим?
Например: Почти в 77% случаев метастазы в печени обнаруживаются при аутопсии у пациентов с меланомой, и только у 10–20% из них отмечались клинические признаки при жизни.
Определён ли хотя бы приблизительный CUTOFF?
С учётом количества факторов, способных повлиять на биохимические показатели, определение прогностических величин крайне затруднено. Тем не менее, некоторые авторы предлагают:
- АСТ≥1.5 -2 × N
- АЛТ≥1.25 - 1.5× N
- ЩФ≥1.5 × N
Данные получены при анализе показателей в точке обнаружения метастатического поражения у пациентов с меланомой, раком молочной железы и колоректальным раком.
Какие методы кроме УЗИ и КТ есть в арсенале:
- Высокой чувствительностью и потенциалом выявления образований <1 см обладает МРТ с гадоксетовой кислотой (Примовист).
- Дополнительную информацию можно получить при использовании ПЭТ с 18F-фтордезоксиглюкозой.
- Среди онкомаркеров информативным для диагностики метастатического поражения является РЭА при КРР, роль других молекул, похоже, окончательно не определена.
- Потенциально эффективны для оценки прогноза и индивидуализации плана наблюдения (но в меньшей степени касаются гепатолога): секвенирование генома опухоли и жидкостная биопсия.
Заключение:
Безусловно, всё вышеизложенное в большей степени касается практики онкологов, чем гепатологов, но попытаемся сделать некоторые практические выводы:
- показатели АЛТ, АСТ, ГГТ и ЩФ, судя по всему, могут быть вспомогательными в оценке прогноза пациентов со злокачественными новообразованиями и предикторами появления доступных визуализации метастазов
- таким образом, сложно не придавать отклонениям значения, и тем более, назначать "гепатопротекторы", отмахиваясь
- при встрече на приёме, может ли гепатолог аргументированно говорить с пациентом о возможном прогрессировании, предлагать досрочное проведение лучевого скрининга или применение гепатоспецифичного контрастирования?
- может ли в реальной жизни подобная тактика повлиять на прогноз или станет напрасной активностью?
Приглашение для дискуссии, обмена мнениями, критических замечаний
Довесок:
Можно ли заподозрить метастатическое поражение печени в отсутствие характерного очагового паттерна при КТ?
Редко - но можно.
В метаанализе объединены случаи инфильтративного поражения печени при РМЖ, которые клинически выглядят как цирроз с признаками портальной гипертензии.
При КТ как правило обнаруживается уменьшение размеров печени и бугристость контуров, при ЭГДС - ВРВП, лабораторно - признаки нарушения синтетической функции. Ответ дают анамнез и гистологическое исследование.
Описаны также редкие случаи острой и быстро прогрессирующей печёночной недостаточности на фоне такой инфильтрации, что не является типичным сценарием, но стоит иметь его в виду.
Почитать - ТУТ