MGMT: что это и в чем его биологическая суть
Григорий ЧижКонтекст ситуации. Повреждение ДНК может принимать различную биохимическую картину. Одна из портретов повреждения ДНК – алкилирование азотистых оснований, т.е. присоединение какой – нибудь метильной (СН3) группы к азотистому основанию нуклеотида.
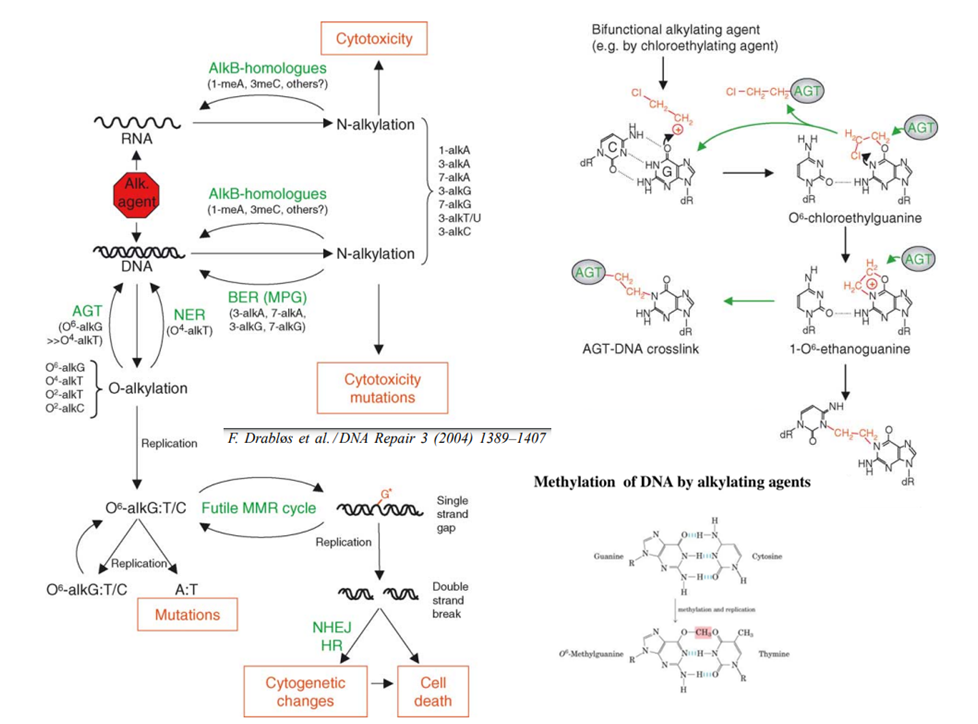
В результате происходит ослабление водородных связей между цепями ДНК, пространственная дезорганизация ДНК, а при попытке репликации с такими алкилированными остатками происходят одноцепочечные и даже двухцепочные разрывы ДНК(процесс достраивания цепи и транскрипции ДНК в условиях алкилирования дают сбой),что, в конечном счете, ведет клетку на пути к остановке клеточной пролиферации (р53 – зависимым путем) и гибели.
Как вы уже догадались, это ведущий механизм действия так называемых алкилирующих агентов, которые реализуют свое противоопухолевое действие путем алкилирования ДНК опухолевых клеток (конечно, страдают и нормальные клетки, но опухоль страдает в наибольшей степени как быстро пролиферирующая ткань).
В контексте лечения глиом таким препаратом является темозоломид. Так уж получилось, что он неплохо проникает в ткани центральной нервной системы и оказывает противоопухолевую эффективность в отношении глиомы.
Помимо темозоломида и других алкилирующих агентов, подобное действие оказывает на клетки и лучевая терапия.
Но существует механизм, который позволяет оперативно восстанавливать нормальную структуру ДНК и избавлять ДНК от ненужных ей алкильных групп. Этот процесс опосредуется метилтрансферазной реакцией, опосредуемый специальным ферментом – О6 – метилгуанин – ДНК – метилтрансферазой. Сокращенно MGMT.

MGMT присутствует и в клетках глиомы, и в условиях лечения темозоломидом, данный фермент имеет для их выживание и резистентности жизненно важное значение.

Но, как мы выяснили ранее, при глиомах возникает множество генетических изменений, в том числе эпигенетическая перепрограммирование, мишени которого пока невозможно предсказать в каждом конкретном случае. Случается так, что в некоторых глиомах происходит метилирование промотора MGMT – соответственно, в них она не экспрессируется и не защищает глиомы от воздействия темозоломида и лучевой терапии. А значит, что результаты лечения (лучевая терапия/химиотерапия темозоломидом, химиолучевая терапия) глиом могут значительно различаться в зависимости от отсутствия или наличия метилирования MGMT (отсутствия или наличия экспрессии MGMT в глиомах).
Клинические данные о предиктивной и прогностической роли метилирования MGMT в глиобластомах
Первые клинические данные о предиктивной роли метилирования MGMT в лечении глиом получены в 2005 году на популяции пациентов с глиобластомой (grade IV).
Пациенты рандомизировались в группы либо химиолучевой терапии (темозоломид плюс лучевая терапия) либо одной лучевой терапии в соответствии с протоколом EORTC26981/2298. Пациенты в группе химиолучевой терапии получали алкилирующий препарат темозоломид 75 мг/м2 ежедневно на фоне стандартной фракционированной лучевой терапии (60 Гр) в течение 6–7 нед. По окончанию лучевой терапии, данная группа пациентов продолжала получать темозоломид 150 - 200 мг/м2 Д1 -Д5 каждые 28 дней в объеме 6 - ти циклов. Конечными точками выступали беспрогрессивная и общая выживаемость.
Оценка статуса гена MGMT была доступна у 206 пациентов. Из 206 оцененных опухолей 92 (44,7%) имели детектируемое метилирование промотора MGMT , тогда как 114 (55,3%) не имели. Примечательно, что доля метилированных опухолей была одинаковой в двух группах лечения

Что вышло? Что статус метилирования промотора гена MGMT оказался сильнейшим прогностическим и предиктивным фактором, независимо от лечения.
- При наличии метилирования промотора MGMT, при добавлении темодала к ЛТ наблюдалось существенное улучшение общей выживаемости по сравнению с пациентами с глиобластомой, в котором данная молекулярно - генетическая особенность не прослеживалась (P<0,001, log rank test):

- Исходы между лучевой и химиолучевой терапии в подгруппе пациентов без метилирования MGMT в отношении общей выживаемости статистически не различались.
- В то время как в группе метилирования, добавление темозоломида к лучевой терапии конвертировалось в значимое преимущество в общей выживаемости. Что касается беспрогрессивной выживаемости, выигрыш от добавления темозоломида к лучевой терапии прослеживался для всех биологических подгрупп:

Вне зависимости от статуса MGMT, все пациенты с глиобластомой выигрывают от добавления темозоломида к лучевой терапии в отношении безпрогрессивной выживаемости, что позволило провозгласить химиолучевую (темозоломид – содержащую) терапию стандартом лечения MGMT - метилированной глиобластомы.
В тот же момент, экспрессия MGMT нивелировала положительный эффект добавления темозоломида в отношении общей выживаемости у таких пациентов и роль добавления темозоломида при экспрессии MGMT представляется уже менее очевидной...
Мне могут возразить, мол "как же! а как же знаменитое исследование от 2005 года, где был продемонстрирован бенифит при добавлении к лучевой терапии темозоломида у пациентов с глиобластомой? Смотри неуч, какой там выигрыш в выживаемости":

Речь об исследовании, проведенной командой Роджера Ступа (в соавторах мелькает и знаменитая фамилия Фишера) и опубликованного в 2005 году, в то же время, что и исследование, представленное ранее, и к самому исследованию существенных предъяв нет - первичная конечная точка по выживаемости достигнута (HR = 0,52 при запланированной 0,75, статистических погрешностей нет), но беда в том, что стратификации по статуса MGMT не было. Учитывая, что метилирование MGMT встречается в 4 случаях из десяти (что достаточно много), где уверенность о том, что в группе с темозоломидом их не могло быть больше, чем в группе лучевой терапии?
Да и если пробежаться по результатам всех исследований, можно заметить, что MGMT - unmethylated фенотип глиобластомы не особо - то и выигрывает от добавления темозоломида к лучам, во всяком случае проигрыш по сравнению с группой метилированных пациентов заметный:

Давать или не давать - вот в чём вопрос. Неблагоприятный прогноз глиобластом провоцирует на более агрессивные действия, но насколько они оправданы в отсутствие MGMT - метилирования - вопрос. Добавление темозоломида чревато гематологической токсичностью, риском пневмоцистной пневмонии (не знаю почему, но во всех протоколах исследований описано, что все пациенты получали профилактику сульфаниламидами), возможными отсрочками в лечении и ухудшением качества жизни ценой недоказанного преимущества в общей выживаемости при unmethylated MGMT - глиобластоме.
В тот же момент, в отношении MGMT - метилированного промотора при глиобластоме вопросов нет - ХЛТ с темозоломидом более чем оправдана.