Капнография у интубированного пациента. Часть 1.
C G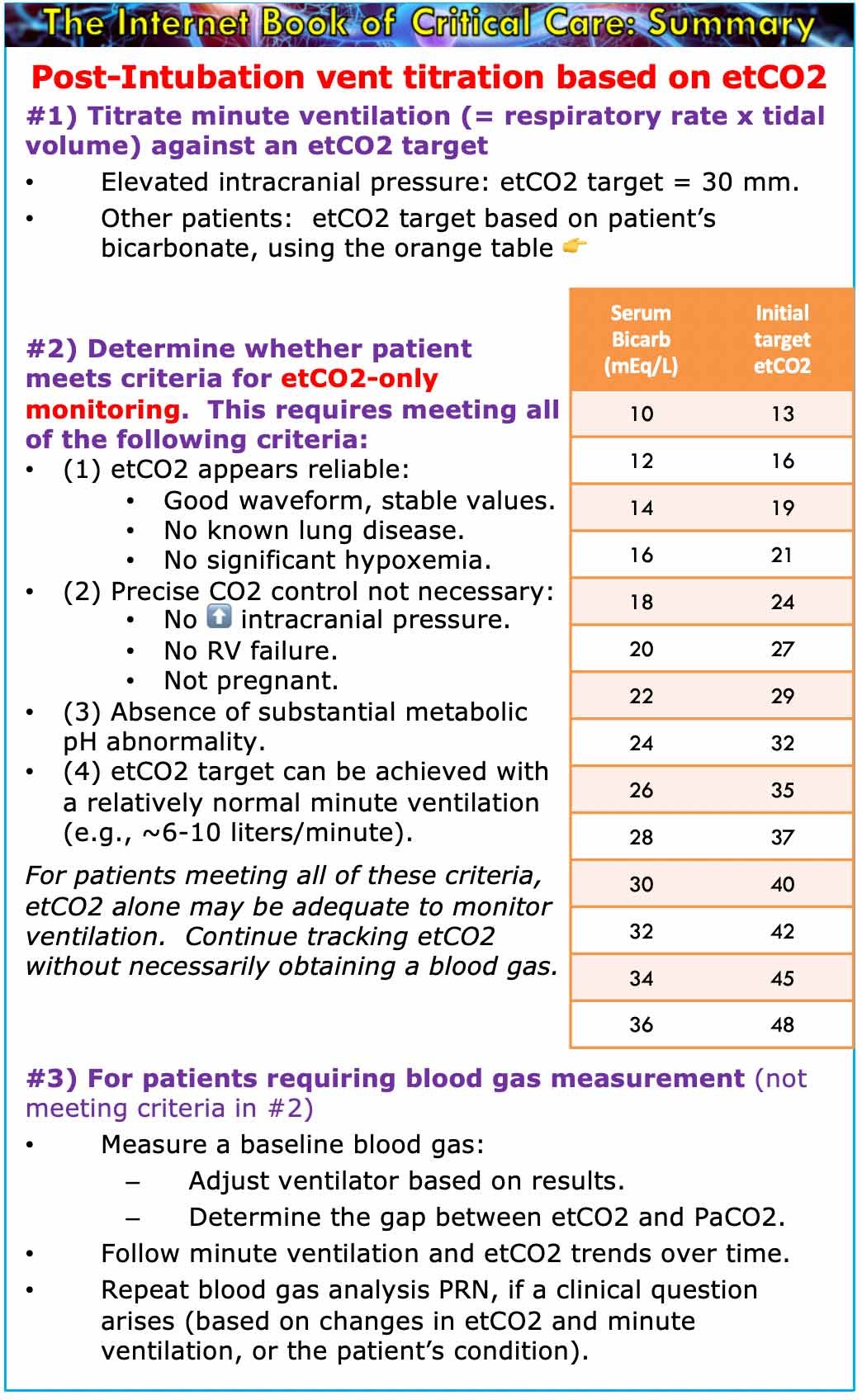
Новый стандарт медицинской помощи
Капнография становится стандартным инструментом мониторинга для повышения безопасности у интубированных пациентов. Отказ от использования капнографии приводит к увеличению смертности в ОРИТ на >70 %, согласно NAP4 . Капнография была впервые применена в операционной, но её важность для безопасности всех критических пациентов очевидна (стандарт мониторинга в отделении интенсивной терапии не должен быть ниже, чем в операционной). Капнография все чаще рекомендуется как для подтверждения положения эндотрахеальной трубки при интубации, так и для последующего контроля проходимости дыхательных путей и эффективности вентиляции в течение всего периода интубации. В течение следующего десятилетия капнография, вероятно, станет универсальным стандартом оказания медицинской помощи во всех хорошо оснащенных отделениях интенсивной терапии.
По мере расширения использования капнографии нам необходимо подумать об интеграции её в нашу практику. Что включает в себя несколько компонентов:
- Оценка значения EtCO2 (например, отмечая её ежедневно в дневниках пациента, наряду с другими жизненно важными показателями).
- Понимание изменений EtCO2 в контексте других данных (особенно тенденций в минутной вентиляции).
- Понимание того, как интерпретировать данные EtCO2.
- Оценка ограничений EtCO2.
еtCO2, PaCO2 и мертвое пространство
Что такое CO2 в конце выдоха (EtCO2)?
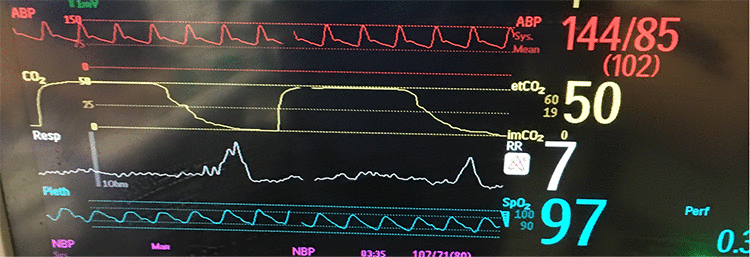
- еtCO2 - это измерение парциального давления CO2 в газе, выдыхаемом в конце выдоха (когда выдыхаемый газ будет наиболее близко напоминать альвеолярную концентрацию CO2).
- Капнография должна мониторироватся у всех интубированных пациентов и отображаться на мониторе (как показано выше).
- Важны как числовое значение, так и форма кривой EtCO2. Если кривая EtCO2 не достигает плато, то числовое значение менее надежно.
Понимание мертвого пространства
- Мертвое пространство относится к вдыхаемому газу, который не участвует в обмене углекислого газа. Тремя основными источниками мертвого пространства являются:
а) Анатомическое мертвое пространство (например, трахея и крупные бронхи) – при каждом вдохе газ поступает в эти области, но не участвует в газообмене.
б) Инструментальное мертвое пространство – для интубированных пациентов включает любую трубку, расположенную между дыхательными путями пациента и местом инсуфляции свежего газа.
в) Альвеолярное мертвое пространство – дисфункциональные альвеолы, которые вентилируются, но плохо обменивают CO2 (или вообще не обменивают).
- Анатомическое и инструментальное мертвое пространство, как правило, фиксировано. Однако, если пациент вентилируется с небольшими дыхательными объемами, то большая часть каждого вдоха будет тратиться на вентиляцию мертвого пространства. Следовательно, при стратегии частых вдохов с низким дыхательным объемом будет меньший клиренс CO2 при данной общей минутной вентиляции.
- Альвеолярное мертвое пространство увеличено при большинстве типов заболеваний легких (отражающих дисфункцию на уровне альвеол, сосудов или дыхательных путей). Например, увеличенное мертвое пространство наблюдается при эмболии легочной артерии, пневмонии или других паренхиматозных заболеваниях легких, таких как аспирация, или при обструктивных заболеваниях легких, таких как астма. Количество альвеолярного мертвого пространства может изменяться с течением времени по мере улучшения или ухудшения состояния легких.
Взаимосвязь между EtCO2 и артериальным уровнем CO2 (PaCO2)
- Лучший способ концептуализировать это - представить газ, поступающий из высоко функционирующей альвеолы в аппарат ИВЛ.
#1) В высокофункциональной альвеоле давление CO2 будет равно артериальному давлению CO2.
#2) Газ вытекающий из альвеолы будет разбавлен газом мертвого пространства, который будет иметь более низкую концентрацию CO2 (поскольку этот газ мертвого пространства не поглощает CO2 из крови).
#3) К тому времени, когда газ достигнет эндотрахеальной трубки, концентрация CO2 в конце выдоха будет ниже, чем СO2 в артерии.
- Это приводит к двум основополагающим принципам EtCO2:
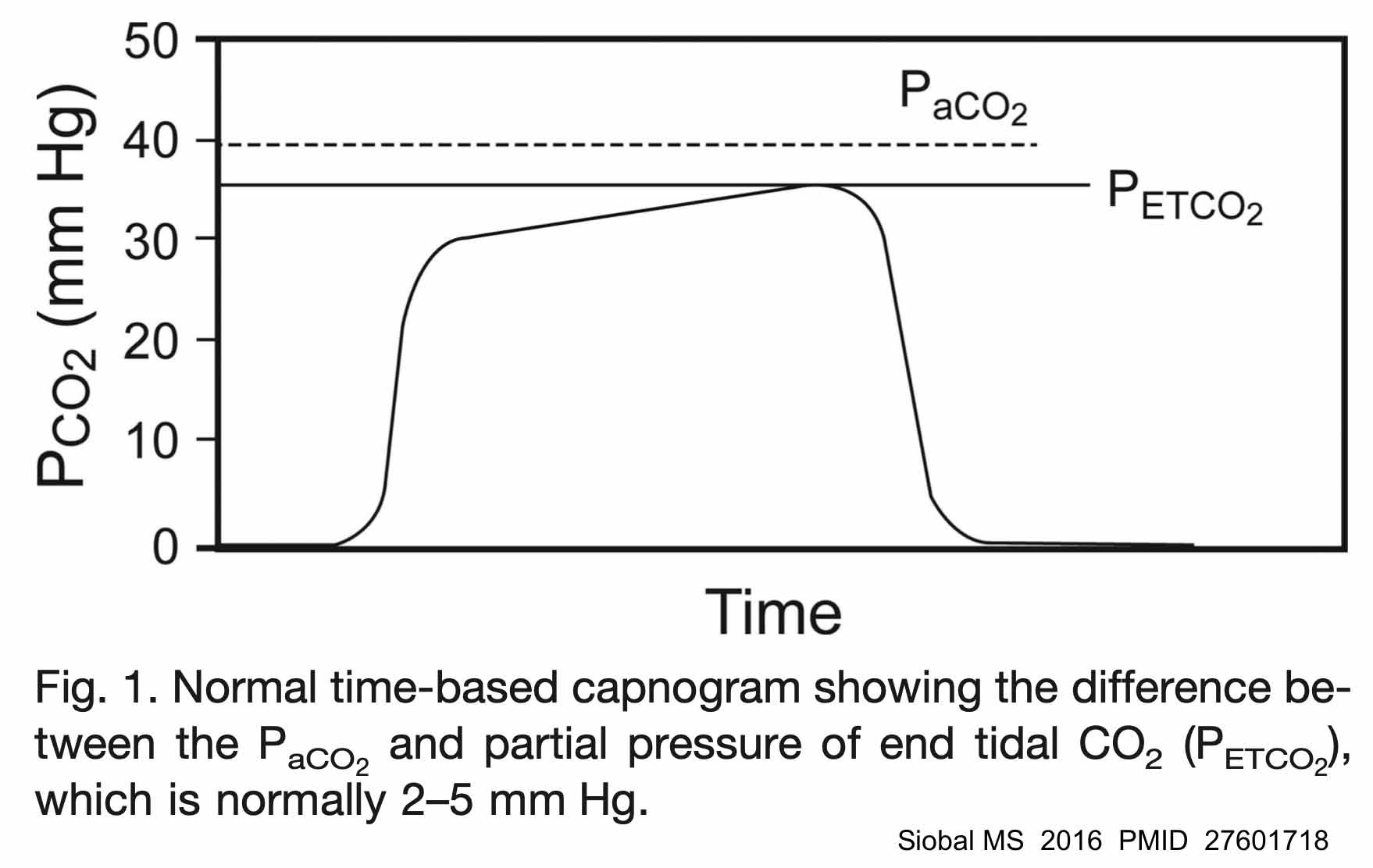
(1) CO2 в артерии должен быть выше, чем EtCO2. Чрезвычайно редко EtCO2 может быть немного выше, чем артериальный CO2 у беременных пациенток с нормальными в целом легкими.🌊 Для повседневной практики интенсивной терапии разумно предположить, что PaCO2 выше EtCO2.
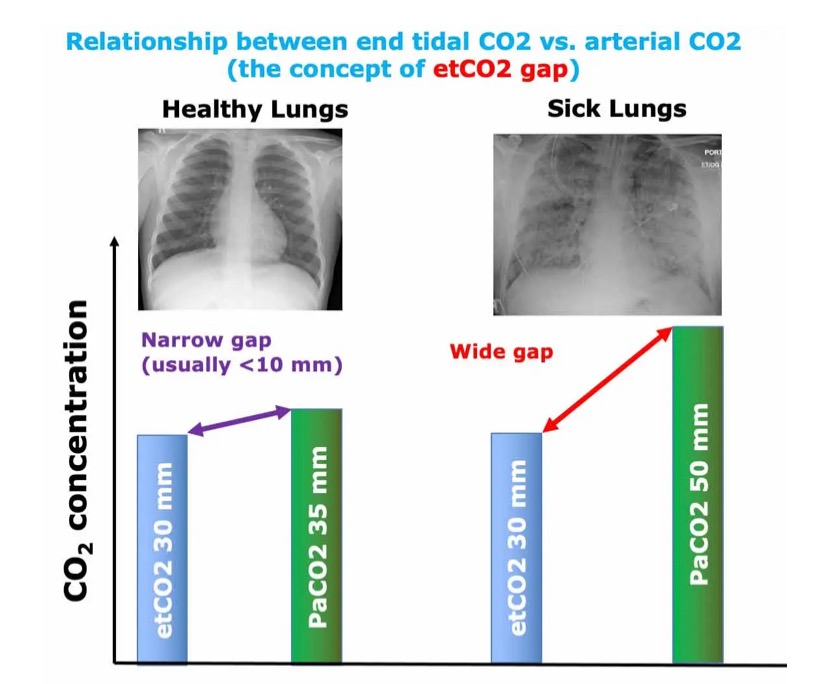
(2) Разница между EtCO2 и PaCO2 является отражением количества мертвого пространства. Любое увеличение мертвого пространства (например, из-за тяжелого повреждения легких) увеличит этот разрыв. У пациентов с нормальными легкими разница обычно составляет ~3-10 мм. Для пациентов с тяжелыми заболеваниями легких разница может быть намного больше.
🔑 Ключевые принципы
- PaCO2 выше, чем EtCO2.
- Разница между EtCO2 и PaCO2 увеличивается при более тяжелом поражении легких (из-за большего количества мертвого пространства).
EtCO2 и сердечный выброс
Здесь мы можем руководствоваться двумя главными принципами:
#1) в устойчивом состоянии сердечный выброс не влияет на EtCO2
- В равновесном состоянии количество CO2, вырабатываемого тканями организма, должно быть элиминировано легкими.(26447854) Поэтому,
(a) Количество выделенного CO2 в легких всегда будет равно произведённому организмом CO2 .
(b) Концентрация CO2 в выдыхаемом газе зависит только от выработки организмом CO2 и объема выдыхаемого газа в минуту (минутная вентиляция).
(c) Сердечный выброс не влияет на CO2 в конце выдоха.
- С клинической точки зрения это действительно полезно, потому что упрощает дело. Для пациента, находящегося в стабильном состоянии, EtCO2 отражает исключительно метаболические параметры (т. е. выработку CO2 организмом) и параметры дыхания (т. е. мертвое пространство и минутная вентиляция). В устойчивом состоянии сердечный выброс не влияет на EtCO2.
а) Это удобно, потому что если бы равновесие EtCO2 отражало дыхательные, сердечные и метаболические параметры, то это был бы очень запутанный параметр.
б) Для стабильных пациентов, находящихся на ИВЛ, сердечный выброс не должен влиять на EtCO2.
#2) динамические изменения сердечного выброса могут вызвать транзиторные изменения в EtCO2
- Быстрые изменения сердечного выброса могут вызвать временные колебания EtCO2.
- Чтобы проиллюстрировать это, давайте представим, что произойдет, если сердечный выброс внезапно упадет с 5 литров в минуту до 3 литров в минуту:
а) Сразу же произойдет снижение поступления CO2 в легкие. Это привело бы к падению EtCO2.
б) Со временем в тканях будет накапливаться CO2. Это увеличило бы напряжение CO2 в венозной крови, в конечном итоге повысив EtCO2 до прежнего уровня.
в) После восстановления равновесия падение сердечного выброса не окажет длительного влияния на EtCO2.
- Примеры изменений сердечного выброса, влияющих на EtCO2, включают следующее:
а) Сердечно-легочная реанимация является примером неравновесного состояния, когда EtCO2 сильно зависит от сердечного выброса. Таким образом, более качественная СЛР улучшит сердечный выброс и увеличит EtCO2. Возвращение спонтанной циркуляции вызовет резкий скачок EtCO2. (подробнее об этом ниже)
б) Маневр пассивного поднятия ног может вызвать временное увеличение сердечного выброса у пациентов, которые реагируют на преднагрузку. Это приведет к временному увеличению EtCO2. (подробнее об этом ниже).
Доказательство – точность EtCO2 в прогнозировании pCO2
Точность EtCO2 в прогнозировании PaCO2 зависит от того, насколько хорошо функционируют легкие пациента. Различные исследования часто приходят к противоположным выводам относительно полезности измерения EtCO2. Исследования с участием пациентов с заболеваниями легких, как правило, приводят к выводу, что EtCO2 недостаточно точно для определения PaCO2. В качестве альтернативы, исследования с участием групп пациентов с нормальной функцией легких, как правило, приводят к выводу, что EtCO2 хорошо подходит для определения PaCO2 пациента. В целом, большинство исследований пациентов без заболеваний легких показывают, что PaCO2 обычно на ~3-5 мм выше EtCO2 и почти всегда в пределах <10-15 мм EtCO2. (28993038, 27601718)
Даже у стабильных пациентов, находящихся на искусственной вентиляции легких, PaCO2 обычно колеблется случайным образом со стандартным отклонением /- 3 мм CO2. (1583545, 6407807, 8020270, 19091262)Следовательно, PaCO2 сам по себе является нестабильным параметром. У пациента может быть определенный PaCO2 в течение одного мгновения, затем он может проснуться, больше дышать и сбросить свой PaCO2. Продолжающееся изменение PaCO2 естественным образом с течением времени предполагает, что бесполезно пытаться быть предельно точным в отношении значений PaCO2. Дополнительная причина не беспокоиться о точных значениях PaCO2 у большинства пациентов заключается в том, что никто не знает оптимальных значений PaCO2 для интубированных пациентов (например, некоторые авторы предполагают, что гиперкапния может быть защитной для легких и, следовательно, полезной). (27060535)
EtCO2 менее точен при мониторинге пациентов с заболеваниями легких (с увеличением погрешности у самых тяжёлых пациентов). Изменения в настройках вентилятора могут изменить количество мертвого пространства и разницу между EtCO2 и PaCO2 (например, увеличение частоты дыхания может привести к аутоРЕЕР, что приведет к недостаточной перфузии некоторых альвеол; эти неперфузированные альвеолы функционируют как мертвое пространство). Таким образом, нельзя предположить, что EtCO2 идеально для отслеживания PaCO2 у самых тяжёлых пациентов с дыхательной недостаточностью.(26447854) Тем не менее EtCO2, может быть полезным для таких пациентов, существенные изменения трендов могут отражать изменение в состоянии пациента, которое требует дальнейшего обследования .
Какова цель pCO2 для интубированного пациента?
Мы делаем тысячи измерений газов крови у интубированных пациентов, чтобы отрегулировать настройки их вентиляторов. Зачем мы это делаем? Нас учили этому. От нас ожидают, что мы это сделаем. Но, на самом деле, нет высококачественных доказательств в поддержку этой практики. Отсутствие доказательств не означает, что мы не должны проверять параметры газов крови. Однако отсутствие доказательств должно умерить наше рвение в проведении этого мониторинга. В частности, давайте рассмотрим следующие моменты.
#1) Нет никаких доказательств в поддержку регулярного мониторинга газов крови у интубированных пациентов.
- Никогда не проводилось высококачественное РКИ, сравнивающее мониторинг параметров газов крови и отсутствие мониторинга параметров газов крови среди интубированных пациентов.
- Мониторинг показателей газов крови сопряжен с расходами, болью и кровопотерей. Однако эта практика никогда не подвергалась тщательному исследованию для определения надлежащей интенсивности мониторинга газов крови. Это аналогично практике рутинного рентгеновского исследования грудной клетки в отделении интенсивной терапии - практике, которая считалась необходимой в течение десятилетий, пока не было доказано, что на самом деле это не так.
а) Необходимо исследование, сравнивающее рутинное измерение газов крови с измерением газов крови, при клинической необходимости (для получения ответа на конкретный клинический вопрос).
#2) Целевой PaCO2 для интубированных пациентов, как правило, неизвестен.
- Помимо нескольких конкретных ситуаций (например, повышение внутричерепного давления), очень мало известно о целевом PaCO2 среди интубированных пациентов.
- Широко распространено мнение, что ориентирование на “нормальные” показатели газов крови улучшит результаты, но имеющиеся данные свидетельствуют о том, что это на самом деле неверно. В частности, литература по ОРДС демонстрирует, что большинство пациентов прекрасно переносят респираторный ацидоз (пермиссивная гиперкапния) – и попытка снизить PaCO2 до “нормального” уровня может фактически нанести ятрогенный вред.
- Некоторые данные свидетельствуют о том, что гиперкапния может быть защитной для легких. Поэтому вполне возможно, что для некоторых пациентов гиперкапния может быть желательной.
- В целом, для интубированных пациентов мало убедительных доказательств того, что изменение рутинных настроек аппарата ИВЛ улучшают исходы пациента.
Итак, на какие значения PaCO2 мы должны ориентироваться? Мы не должны выбрасывать ребенка вместе с водой – некоторый контроль над PaCO2, вероятно, разумен. В отсутствие высококачественных данных могут быть разумными следующие целевые показатели.
а) пациенты, которым требуется более жесткий контроль над PaCO2
- Некоторые пациенты могут требовать более тщательного мониторинга, например, следующие группы:
(1) Неврологические пациенты с повышенным внутричерепным давлением.
(2) Пациенты с правосторонней сердечной недостаточностью из-за легочной гипертензии (гиперкапния и ацидоз увеличивают сопротивление легочных сосудов).
(3) Беременные пациентки.
- Ориентирование на “нормальные” значения PaCO2 у этих пациентов (например, 35-45 мм) представляется разумным.
- Иногда другим пациентам с определенными патологиями могут потребоваться особые стратегии регулирования рН (например, пациентам с тяжелой салицилатной интоксикацией, требующим подщелачивания).
б) пациенты, которым не требуется жесткий контроль над PaCO2
- Среди большинства интубированных пациентов, вероятно, нет необходимости ориентироваться на такой узкий диапазон значений PaCO2.
- Оптимальная стратегия титрования PaCO2 у этих пациентов неизвестна, поэтому любые цели по определению будут произвольными.
- Одной из разумных стратегий может быть корректировка PaCO2 для достижения рН примерно 7,2-7,5. Обоснование этого заключается в следующем:
а) рН, по-видимому, является более важной физиологической переменной, чем PaCO2. Нормальная физиология, по-видимому, предназначена больше для защиты рН, чем для защита PaCO2 (например, дыхательная компенсация метаболических нарушений кислотно-щелочного обмена демонстрирует, что эволюция больше заботится о рН, чем о PaCO2). Функция ферментов и белков зависит от рН, а не от PaCO2, что объясняет, почему рН важнее.
б) Алкалемия, как правило, плохо переносится, но 7,50 представляет собой лишь очень легкую степень алкалемии.
в) Ацидемия, как правило, переносится гораздо лучше, чем алкалемия. Нижний уровень “безопасного” рН неизвестен и может варьироваться у разных пациентов. Тем не менее, 7.2, по-видимому, находится в пределах безопасного диапазона (например, как установлено общепринятой практикой, касающейся пермиссивной гиперкапнии).
- Для пациентов с заболеваниями легких (например, ОРДС, тяжелой астмой, бронхоплевральной фистулой) может быть лучше пермиссивная гиперкапния (например, нацеленная на pH > 7,15 или 7,10). Однако целевой показатель рН 7,2-7,5 может быть разумным для большинства интубированных пациентов.
Продолжение следует…