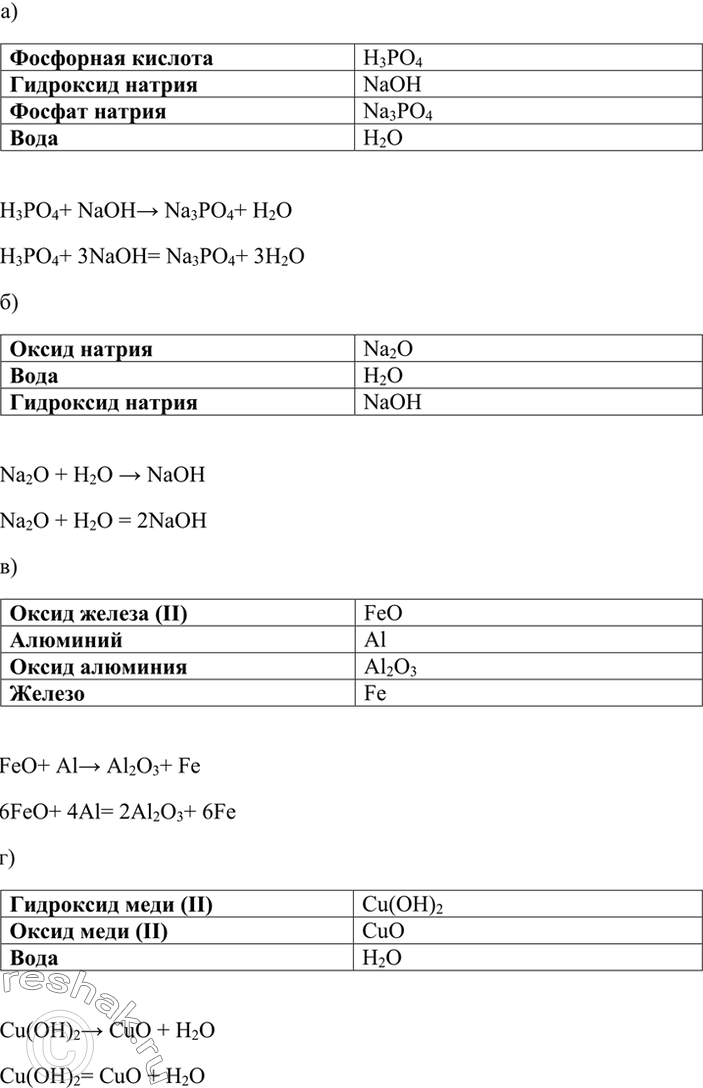
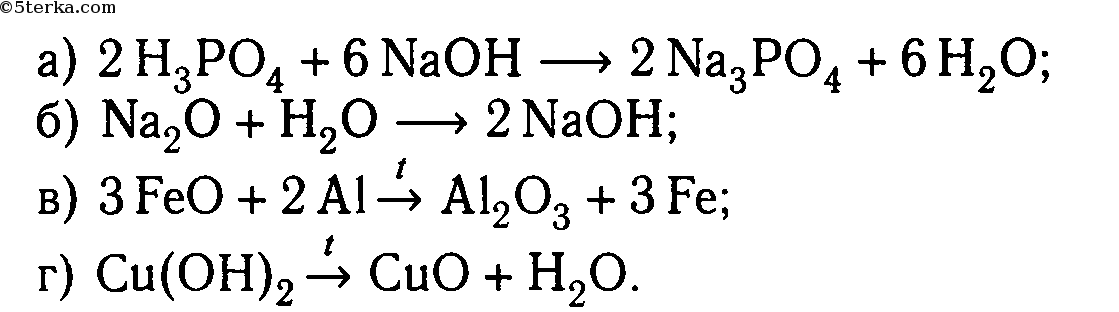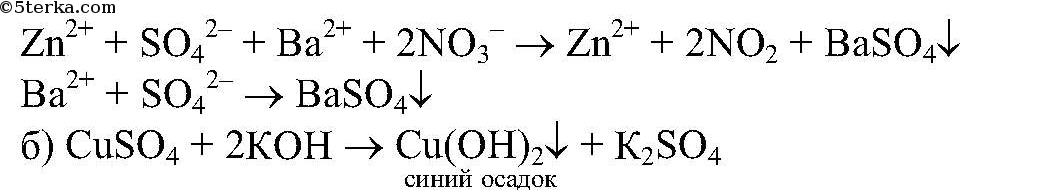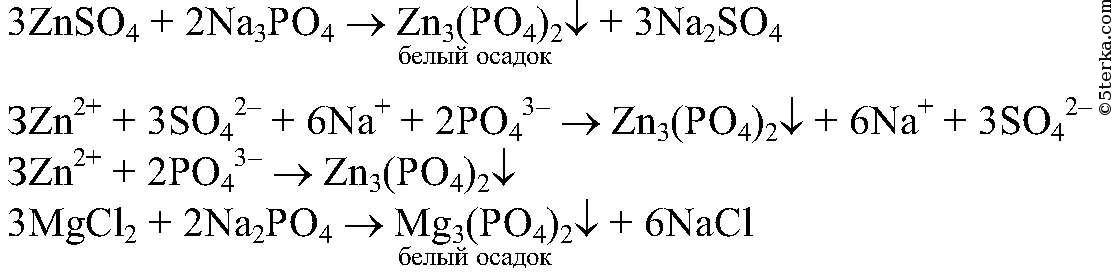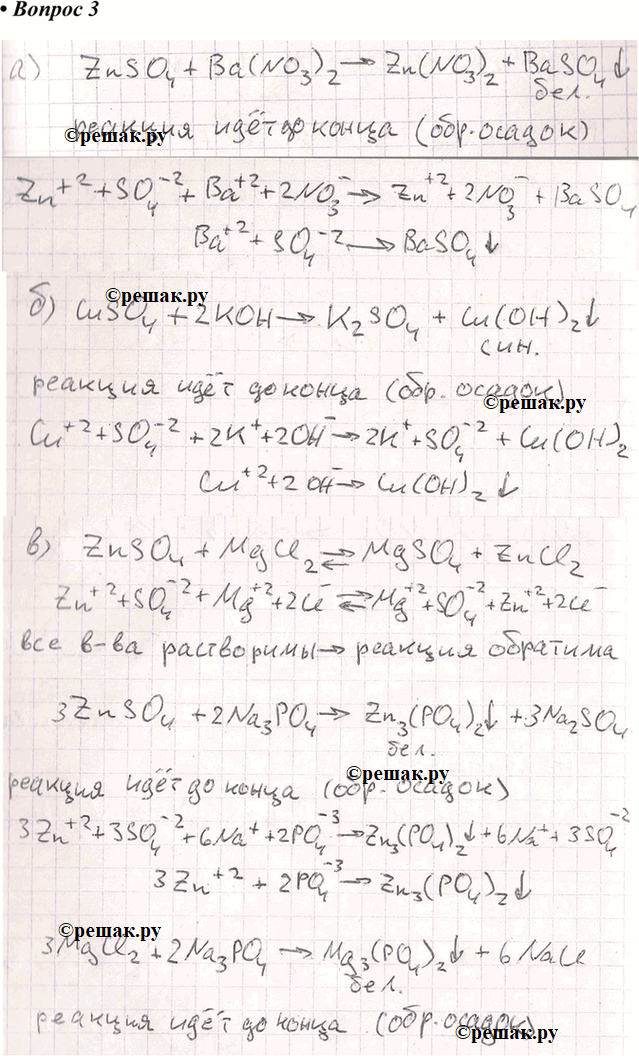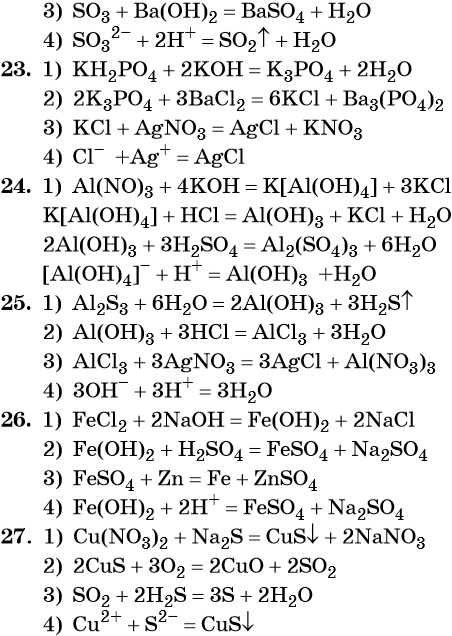Фосфат Железа И Гидроксид Натрия

⚡ 👉🏻👉🏻👉🏻 ВСЯ ИНФОРМАЦИЯ ДОСТУПНА ЗДЕСЬ, КЛИКАЙ 👈🏻👈🏻👈🏻
Реакция фосфата железа (ii) и гидроксида натрия . . .
Реакция гидрофосфата железа (ii) и гидроксида натрия . . .
Фосфат Железа (Iii)
Некоторые соли ортофосфорной кислоты: фосфат кальция . . .
Гидроксид Железа (Ii), Характеристика, Свойства И . . .
Окислительно-восстановительные реакции . Часть 1
Пероксид водорода фосфат магния бром карбонат кальция . . .
Хлорид железа фосфат кальция гидроксид натрия медь оксид серы
Гидроксид Железа (Iii) = Оксид Железа (Iii) + Вода
1) Как распознать карбонат, хлорид, фосфат и гидроксид . . .
Мидокалм При Грыже Поясничного Отдела Позвоночника
Маннит Доставка
Лекарство От Тромбов Ксарелто Цена
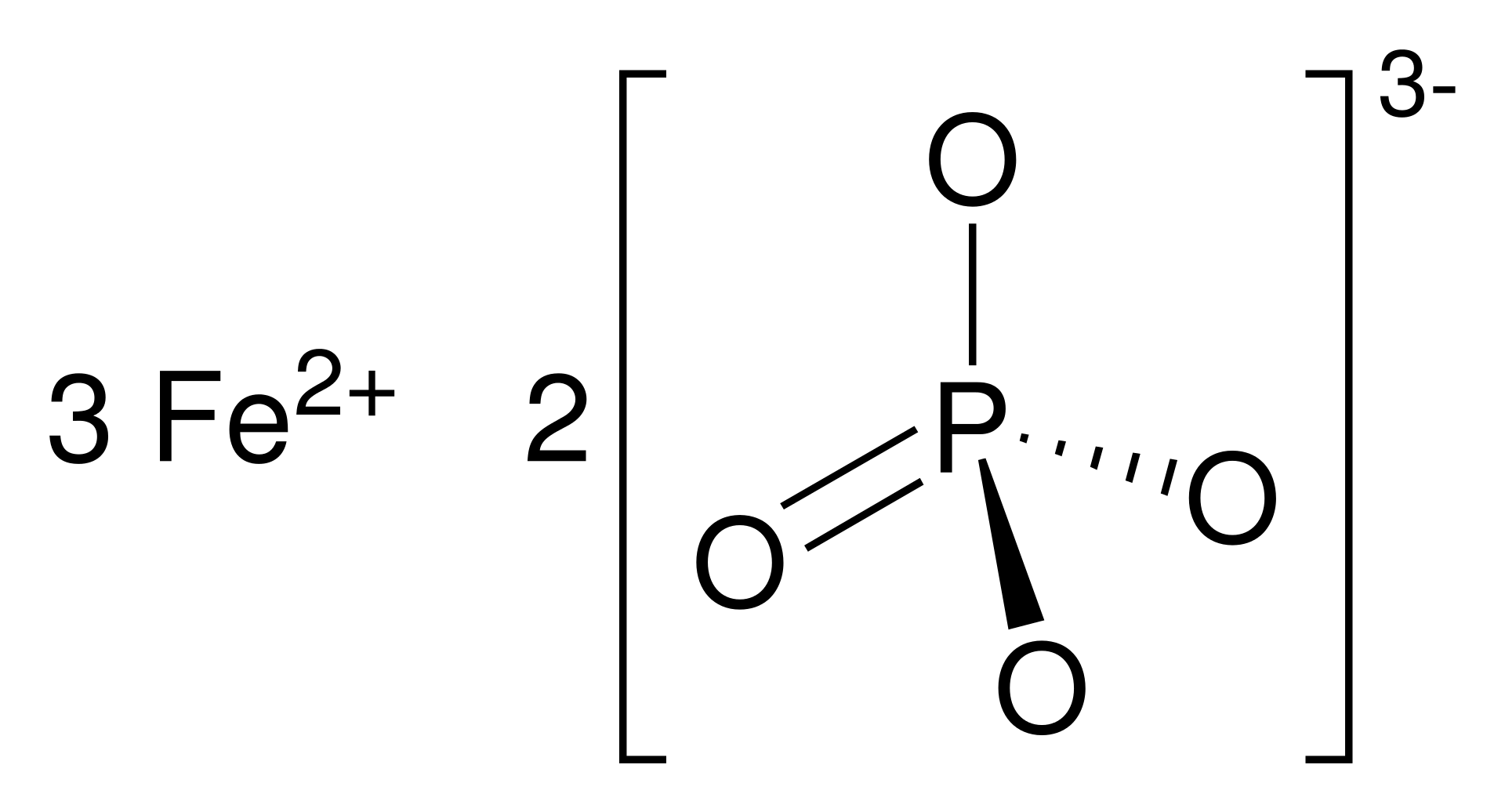
Реакция фосфата железа (ii) и гидроксида натрия Fe 3 (PO 4 ) 2 + 6NaOH → 3Fe(OH) 2 + 2Na 3 PO 4 В результате реакции фосфата железа (ii) (Fe 3 (PO 4 ) 2 ) и гидроксида натрия (NaOH) образуется гидроксид железа (ii) (Fe(OH) 2 ), ортофосфат натрия (Na 3 PO 4 )
3FeHPO 4 + 3NaOH → Na 3 PO 4 + 3H 2 O + Fe 3 (PO 4) 2 . В результате реакции гидрофосфата железа (ii) (FeHPO 4) и гидроксида натрия (NaOH) образуется ортофосфат натрия (Na 3 PO 4 ), вода (H 2 O), фосфат железа (ii) (Fe 3 (PO 4) 2) FeHPO 4 . соль . Гидрофосфат железа (II)
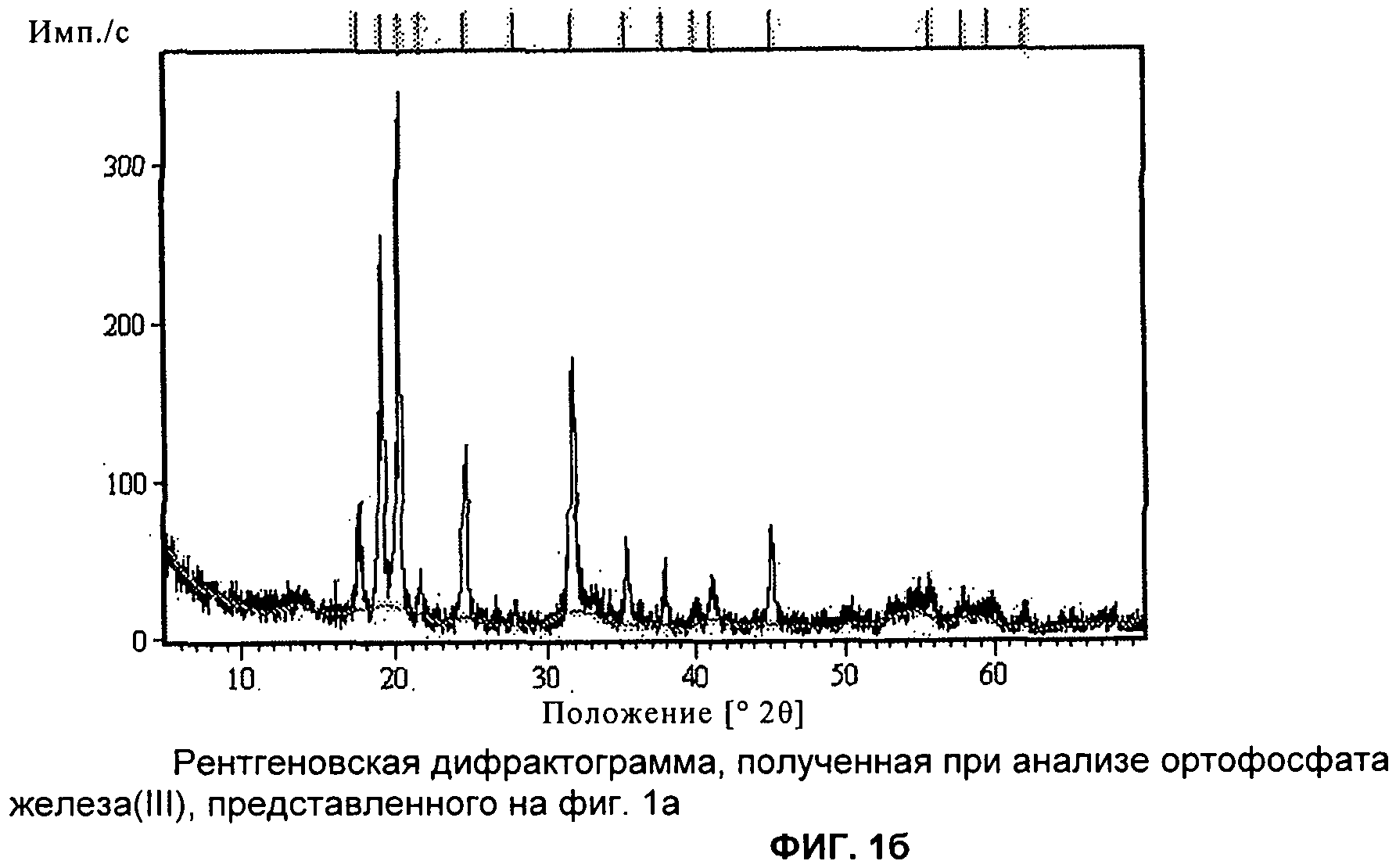
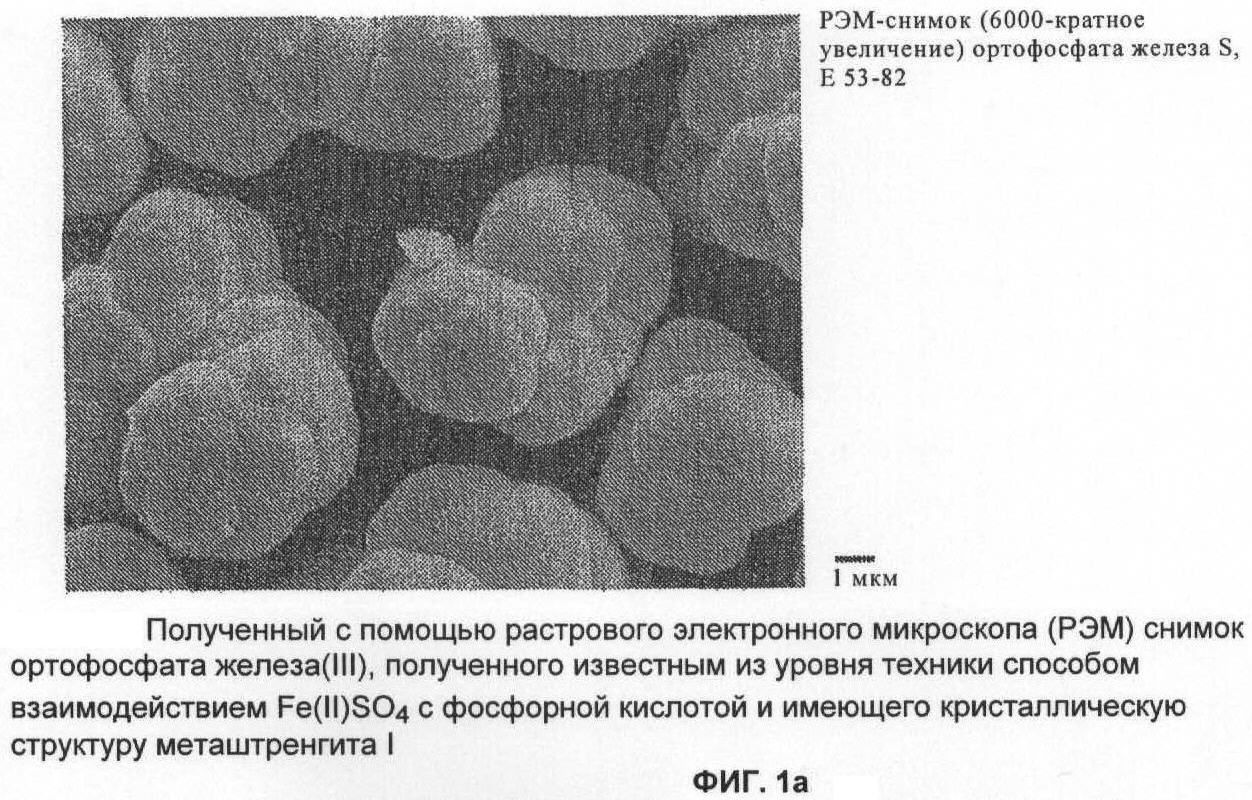
Обработка растворов солей железа (III) гидрофосфатом натрия в присутствии ацетата натрия: FeCl3 + Na2HPO4 + NaCH3COO → FePO4↓ + 3NaCl + CH3COOH Fe 2 (SO 4) 3 +2K 3 PO 4 =2FePO 4 +3K 2 SO 4 Физические свойства Фосфат железа (III) образует жёлтые кристаллы тетрагональной сингонии, параметры ячейки a = 0,5035 нм, c = 0,5589 нм .
Фосфат железа (iii): получение . Его можно получить, смешав растворы солей железа с гидрофосфатом и ацетатом натрия . Продукты реакции - фосфат железа, хлорид натрия и уксусная кислота . Применение
Гидроксид железа (II) встречается в природе в виде минерала амакинита . Данный минерал содержит примеси магния и марганца (эмпирическая формула амакинита Fe 0,7 Mg 0,2 Mn 0,1 (OH) 2 ) . Цвет минерала амакинита жёлто-зелёный или светло-зелёный, твёрдость по Моосу 3,5-4, плотность 2,925 . . .
Допустимо использование водных растворов этих веществ . Возможные варианты ответа: 2NH 3 + 2KMnO 4 = N 2 + 2MnO 2 + 2KOH + 2H 2 O . 1 2N -3 — 6 ē → N 20 (восстановитель) 2 Mn +7 + 3 ē → Mn +4 (окислитель) 2NaMnO 4 + 16HCl = 2MnCl 2 + 5Cl 2 + 2NaCl + 8H 2 O . 5 . 2Cl -1 - 2 ē → Cl 20 (восстановитель) 2 .
Гидроксид железа(II), гидроксид натрия, хлор, гидрофосфат натрия, карбонат меди(II) . 3Cl 2 + 6NaOH → NaClO 3 + 5NaCl + 3H 2 O (при нагревании) Cl 0 + 1e = Cl -1 5 окислитель . Cl 0 - 5e = Cl +5 1 восстановитель . Возможен другой . . .
Хлорид железа фосфат кальция гидроксид натрия медь оксид серы . Для выполнения задания используйте следующий перечень веществ: хлорид железа (iii), фосфат кальция, гидроксид натрия, медь, оксид серы (iv) .
Гидроксид железа (III) = оксид железа (III) + вода . Нитрат алюминия + фосфат натрия = фосфат алюминия + нитрат натрия . Серная кислота + гидроксид натрия = сульфат натрия + вода . Напишите уравнения реакций по следующим схемам:
Барий + вода = гидроксид бария + водород