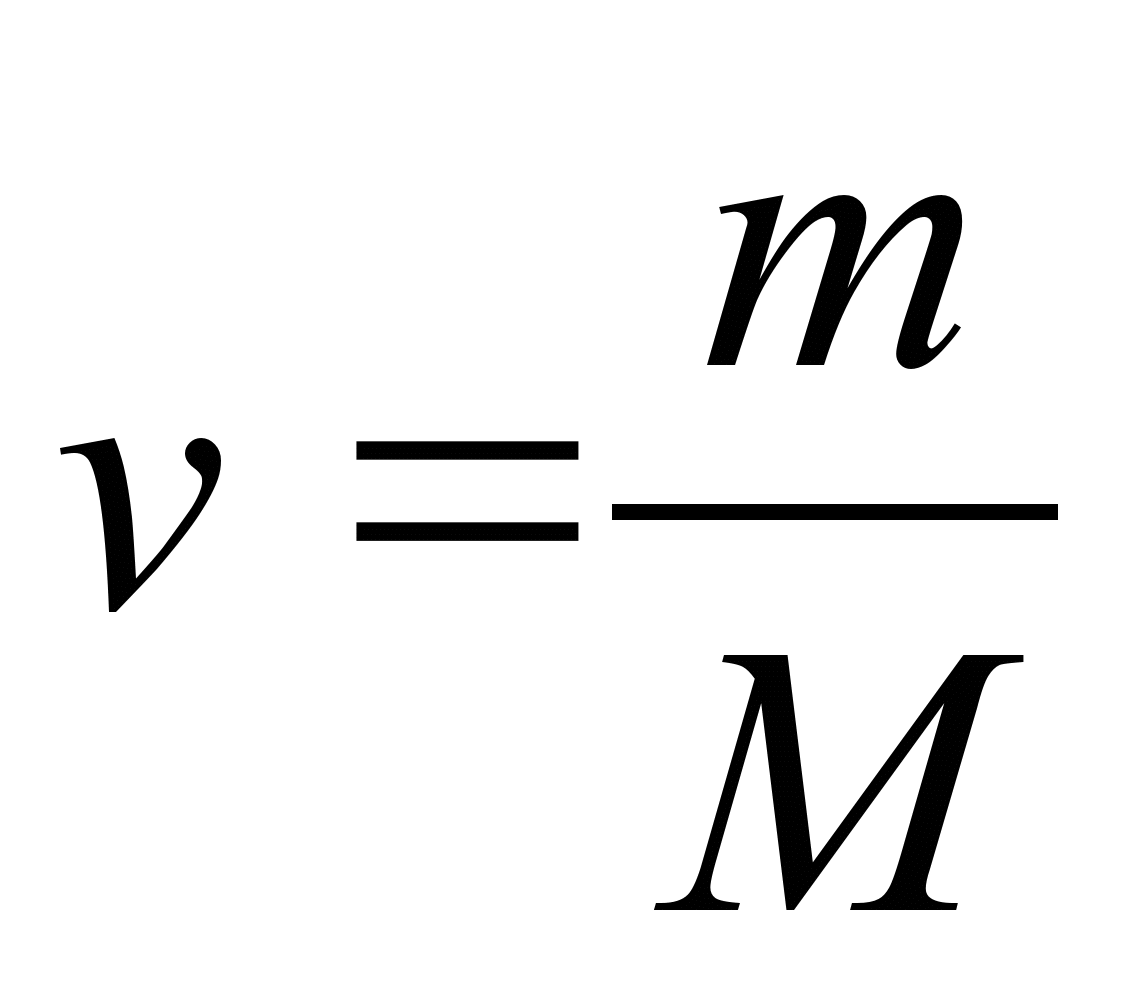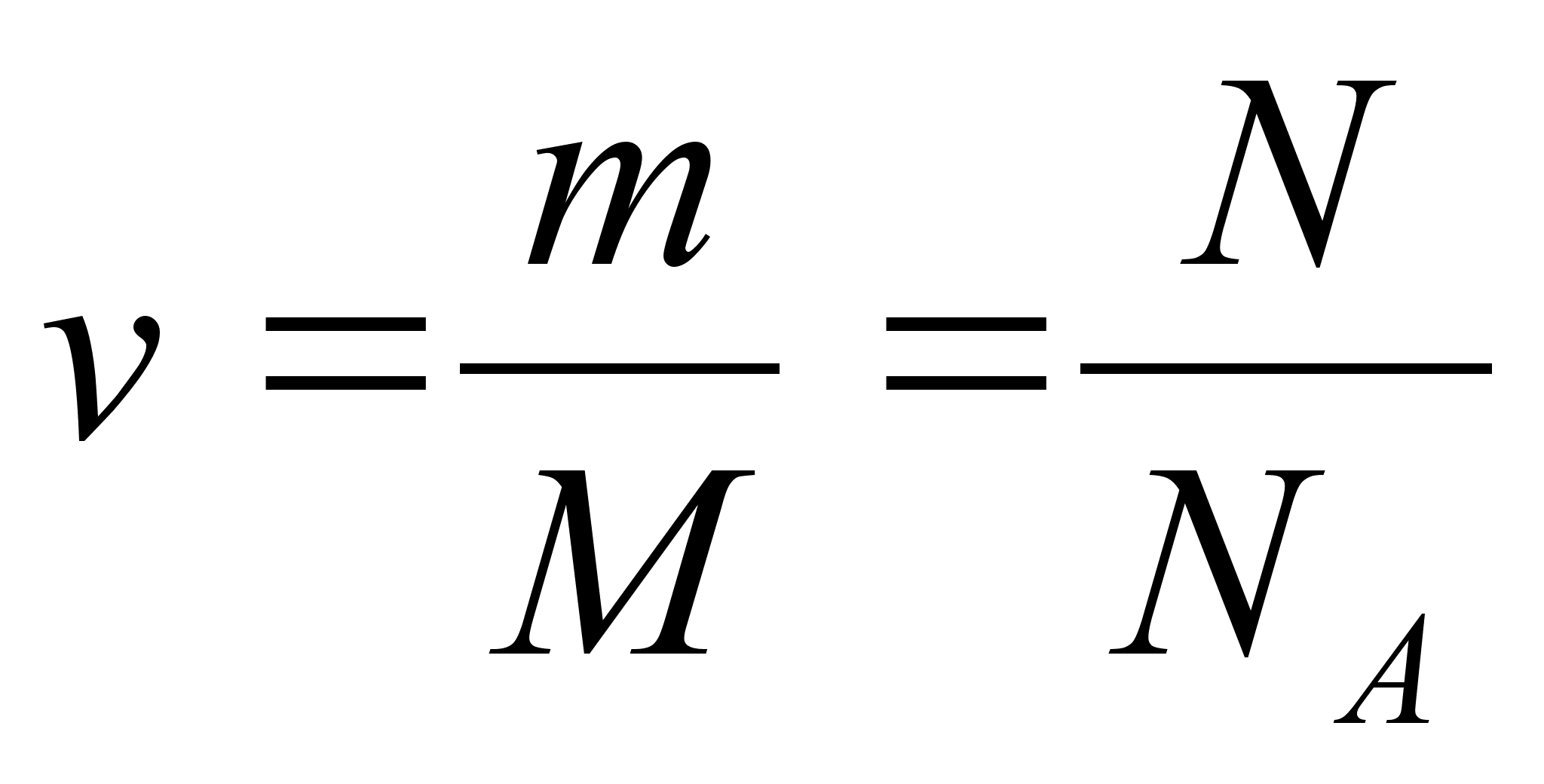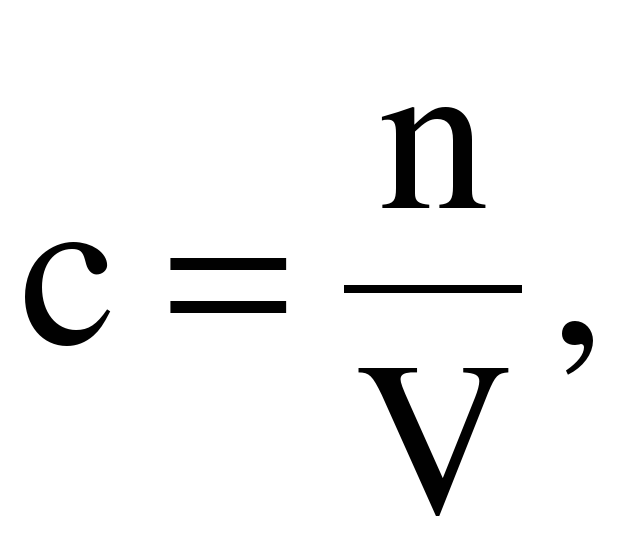Формула Ню Химия
⚡ 👉🏻👉🏻👉🏻 ИНФОРМАЦИЯ ДОСТУПНА ЗДЕСЬ ЖМИТЕ 👈🏻👈🏻👈🏻
Формула Ню Химия
Материал из Википедии — свободной энциклопедии
{\displaystyle \ n}
,
{\displaystyle \ \nu }
Коли́чество вещества́ — физическая величина, характеризующая количество однотипных структурных единиц, содержащихся в веществе. Под структурными единицами понимаются любые частицы, из которых состоит вещество (атомы, молекулы, ионы, электроны или любые другие частицы)[1]. Единица измерения количества вещества в Международной системе единиц (СИ) и в системе СГС — моль[2]. Без конкретизации объекта рассмотрения термин «количество вещества» не используют[K 1].
Эта физическая величина используется для измерения макроскопических количеств веществ в тех случаях, когда для численного описания изучаемых процессов необходимо принимать во внимание микроскопическое строение вещества, например, в химии, при изучении процессов электролиза, или в термодинамике, при описании уравнений состояния идеального газа.
При описании химических реакций, количество вещества является более удобной величиной, чем масса, так как молекулы взаимодействуют независимо от их массы в количествах, кратных целым числам.
Например, для реакции горения водорода (2H2 + O2 → 2H2O) требуется в два раза большее количество вещества водорода, чем кислорода. При этом масса водорода, участвующего в реакции, примерно в 8 раз меньше массы кислорода (так как атомная масса водорода примерно в 16 раз меньше атомной массы кислорода). Таким образом, использование количества вещества облегчает интерпретацию уравнений реакций: соотношение между количествами реагирующих веществ непосредственно отражается коэффициентами в уравнениях.
Так как использовать в расчётах непосредственно количество молекул неудобно, потому что это число в реальных опытах слишком велико, вместо измерения количества молекул в единицах «штука», их измеряют в молях. Фактическое количество единиц "штука" в 1 моле вещества называется числом Авогадро (NA = 6,02214076⋅1023 "штука"/моль[4]).
Количество вещества обозначается латинской
{\displaystyle n}
(эн) и не рекомендуется обозначать греческой буквой
{\displaystyle \nu }
(ню), поскольку этой буквой в химической термодинамике обозначается стехиометрический коэффициент вещества в реакции, а он, по определению, положителен для продуктов реакции и отрицателен для реагентов[5]. Однако в школьном курсе широко используется именно греческая буква
{\displaystyle \nu }
(ню).
Для вычисления количества вещества на основании его массы пользуются понятием молярная масса:
{\displaystyle n=m/M}
, где m — масса вещества, M — молярная масса вещества. Молярная масса — это масса, которая приходится на один моль данного вещества. Молярная масса вещества может быть получена произведением молекулярной массы этого вещества на количество молекул в 1 моле — на число Авогадро. Молярная масса (измеренная в г/моль) численно совпадает с относительной молекулярной массой.
По закону Авогадро, количество газообразного вещества можно также определить на основании его объёма:
{\displaystyle n}
= V / Vm, где V — объём газа при нормальных условиях, а Vm — молярный объём газа при тех же условиях, равный 22,4 л/моль.
Таким образом, справедлива формула, объединяющая основные расчёты с количеством вещества:
↑ Можно говорить о количестве вещества для молекул (формульных единиц) водорода
{\displaystyle {\ce {H2}}}
, можно говорить о числе молей атомов водорода
{\displaystyle {\ce {H}}}
, но словосочетание «один моль водорода» без конкретизации объекта обсуждения лишено смысла[3].
↑ [dic.academic.ru/dic.nsf/polytechnic/4077/КОЛИЧЕСТВО Количество вещества]. Большой энциклопедический политехнический словарь (2004). Дата обращения: 31 января 2014.
↑ Деньгуб В. М., Смирнов В. Г. Единицы величин. Словарь-справочник. — М.: Издательство стандартов, 1990. — С. 85. — 240 с. — ISBN 5-7050-0118-5.
↑ Пресс И. А., Основы общей химии, 2017, с. 119.
↑ Avogadro constant (англ.). Physical Measurement Laboratory. National Institute of Standards and Technology. Дата обращения: 7 февраля 2017.
↑
{\displaystyle {\mathsf {5B+4{,}5H_{2}\ {\xrightarrow {}}\ B_{5}H_{9}}},~\Delta H_{298}^{\circ }=+62{,}8~\mathrm {kJ} }
Когда теплота реакции записывается так, как это сделано в данном уравнении, подразумевается, что она выражена в килоджоулях на стехиометрическую единицу («моль») реакции по записанному уравнению. В рассматриваемом случае теплота реакции равна 62,8 кДж на моль (+62,8 кДж · моль−1) B5H9 (газообразного), но составляет только 12,56 кДж на моль израсходованного бора (твёрдого кристаллического) или 62,8 кДж на каждые 4,5 моля газообразного водорода. Теплоты реакций всегда табулируются в расчете на моль образующегося соединения.
Это заготовка статьи по химии. Вы можете помочь проекту, дополнив её.
Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена.
Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники.
Эта отметка установлена 13 мая 2011 года.
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист.
Секретная шпаргалка по химии . 2.3 Количество вещества (моль). | Яндекс Дзен
🎦 Количество вещества. Совершенно та же Википедия. Только лучше. // WIKI 2
Урок 8. Химическое количество вещества и моль – HIMI4KA
Основные формулы для решения задач по химии | Дистанционные уроки
Химическое количество вещества . Постоянная... — урок. Химия, 8–9 класс.
В сентябре, когда я начинаю работать с новыми учениками, всегда волнуюсь. Первые занятия - самые важные, поскольку происходит построение "призмы", через которую я буду передавать знания и опыт, а ученик - воспринимать информацию и учиться работать с ней.
Я преподаю химию как точный предмет, в основе которого лежит строгая математическая логика. Я учу строить систему в любой поступающей информации, видеть главные узлы системы и связи между ними. Только так можно изучить такой сложный предмет, каким является химия. Ребята учатся грамотно учиться, затем свои знания и опыт работы они переносят в высшую школу, изучая более сложные медицинские предметы.
Не все проходит гладко. Накопление информации и опыта всегда индивидуально и связано с формированием сложной системы условных рефлексов. Но даже в самых тяжелых и запущенных случаях я не опускаю руки, использую современные технологии нейрофизиологии для ускорения процесса образования и повышения его качества.
Вспоминаю 2008 год. Это был последний год без ЕГЭ. Тяжелые задания на письменных вступительных экзаменах подразумевали серьезную подготовку, особенно по решению сложных задач. В тот год у меня были очень сильные ученики. Все как на подбор, быстро схватывали материал, набирались опыта и решали сложные задачи. И только Дима резко отставал от всех остальных. На занятиях он работал отлично, но как только покидал стены кабинета, весь изученный материал и накопленный опыт исчезали бесследно. На следующем занятии приходилось начинать все с начала. Так продолжалось несколько месяцев. Я понимала, что это не вина, а беда мальчика, а ключ к решению проблемы спрятан в индивидуальных особенностях физиологии высшей нервной деятельности. Пришлось обратиться за советом к своим бывшим ученикам, профессиональным нейрофизиологам. Как решилась проблема Димы и кем он стал теперь, я расскажу позже. А мы продолжим изучать химию. Тема сегодняшней статьи - количество вещества (моль).
Количество вещества (моль) - важная расчетная величина в химии. Это именно тот золотой ключик, которым открывают любую, даже самую потайную дверь химической задачи. Термины "моль" и "молекула" - однокоренные, они произошли от латинского слова "moles". В XVII в. появился термин "молекула" ("маленькая масса"). Понятие "моль" ("большая масса", "порция") появилось в начале XX века. Автор термина "моль" - немецкий химик и физик Вильгельм Оствальд.
Количество вещества определяется числом частиц, из которых состоит данное вещество (атомов, молекул, ионов), и обозначается греческой буквой "ню". Для характеристики количества вещества в химии используют особую единицу измерения - моль.
Моль - это количество вещества, которое содержит столько структурных единиц (атомов, молекул, ионов), сколько атомов углерода содержится в 12 г изотопа углерода 12С. Экспериментально установлено, что один моль любого вещества содержит число Авогадро структурных единиц. В настоящее время известно более 60 независимых экспериментальных методов определения значения числа Авогадро.
Молярная масса - это масса 1 моля вещества, то есть отношение массы вещества к его количеству, выраженное в г/моль.
Абсолютная масса одной молекулы (атома) определяется делением молярной массы на число Авогадро
Итак, мы освоили первые математические формулы для химических расчетов. Попробуем закрепить наши знания и умение пользоваться этими формулами на решении простейших задач по химии.
Определите массу карбоната натрия и воды, которые содержатся в 0,8 моль кристаллической соды
Вычислите абсолютную массу одной молекулы углекислого газа в граммах
Образец вещества, массой 5,6 г содержит десятую часть числа Авогадро молекул. Определите молярную массу вещества
Эквимолярная смесь оксида фосфора (V) и диоксида кремния имеет массу 60,6 г. Определите массу оксида фосфора (V)
Вот мы и освоили первые, самые важные расчетные величины и поучились с ними работать. Но это еще не все. С количеством вещества можно вытворять такие замечательные трюки, которые вы даже представить не можете! Об этом скоро в следующих статьях.
А теперь о Диме и его проблеме с изучением химии. Тайна лежала в индивидуальных особенностях бета-тета активности головного мозга. Мои бывшие ученики, а теперь - ведущие нейрофизиологи МГУ работают с ритмами мозга. Они определили, что бета-тета ритмы мозга находится под влиянием гиппокампа, который играет ключевую роль в ускоренной переработке информации и активации долговременной памяти. Стимуляция бета-тета волновой активности способствует изучению иностранных языков, усвоению новых терминов, более быстрому и конструктивному получению фундаментальных знаний. Дима прошел курс БОС терапии по стимуляции мозговой активности в одной из лабораторий МГУ. Уже через месяц он не только достиг уровня своих товарищей, но и даже превзошел их. Как показали исследования, после трех часов решения задач по химии также происходил невероятный всплеск бета-тета волн, а через три месяца регулярных занятий формировался высокий уровень бета-тета потенциала! Дима блестяще сдал вступительные экзамены и в 2008 году поступил в РГМУ им. Н.И.Пирогова (РНИМУ им. Н.И. Пирогова). Сегодня Дима работает врачом-педиатром в одной из центральных клиник Москвы.
Вы готовитесь к ЕГЭ и хотите поступить в медицинский? Обязательно посетите мой сайт Репетитор по химии и биологии http://repetitor-him.ru. Здесь вы найдете огромное количество задач, заданий и теоретического материала, познакомитесь с моими учениками, многие из которых уже давно работают врачами. Звоните мне +7(903) 186-74-55. Приходите ко мне на курс, на Мастер-классы "Решение задач по химии" - и вы сдадите ЕГЭ с высочайшими баллами, и станете студентом престижного ВУЗа!
PS! Если вы не можете со мной связаться из-за большого количества звонков от моих читателей, пишите мне в личку ВКонтакте, или на Facebook. Я обязательно отвечу вам.
Репетитор по химии и биологии кбн В.Богунова
Частные Фото Свинг Пар
Порно Фото Тетя И Малыш
Фильм Порно Эротика 70 80ых
Древний Способ Увеличения Груди
Порнушка У Гинеколога