Эфедрин - общие сведения
MacondoRCМы в телеграмм:
💡 Получите все необходимое вместе с Macondo. Стать членом сообщества можно через Macondo Shop (ссылка в шапке профиля).
У нас вы найдете:
🟢 Рецепты синтеза:🔹Мефедрон🔹A-PVP🔹МДМА🔹Амфетамин🔹Метамфетамин🔸Рецепты других веществ
🟠 Товары:🔹Реактивы и прекурсоры🔹Лабораторная посуда и оборудование🔹Конструкторы почтой🔹Конструкторы кладом
🟡 Услуги:🔹Консультации для новичков🔹Консультации для магазинов🔸 Справочник WIKI
🟣 Прочее:🔹 Правила🔹 Контакты
Введение:
Эфедрин, природный алкалоид, имеет богатую историю, тесно переплетенную с традиционной медициной и современной фармакологией. Эфедрин был впервые выделен в 1885 году и поступил в коммерческое использование в 1926 году. Он включен в Список основных лекарственных средств Всемирной организации здравоохранения. Он доступен в виде непатентованного лекарства. Это соединение, полученное из таких растений, как Ephedra sinica, нашло применение в самых разных областях: от противоотечных средств до средств для снижения веса. Это исчерпывающее руководство призвано пролить свет на эфедрин, изучить его физические и химические свойства, методы синтеза, применение, правовой статус, хранение, утилизацию, токсичность, а также правила обращения с ним.

Химические свойства эфедрина:
Эфедрин, классифицируемый как симпатомиметический амин и замещенный амфетамин , имеет сходство молекулярной структуры с фенилпропаноламином, метамфетамином и адреналином (адреналином). По химическому составу этот алкалоид с фенетиламиновым скелетом обычно встречается в различных растениях рода Ephedra семейства Ephedraceae. Его основной механизм действия заключается в усилении активности норадреналина (норадреналина) на адренергических рецепторах. Обычно он продается в форме гидрохлорида или сульфатной соли.
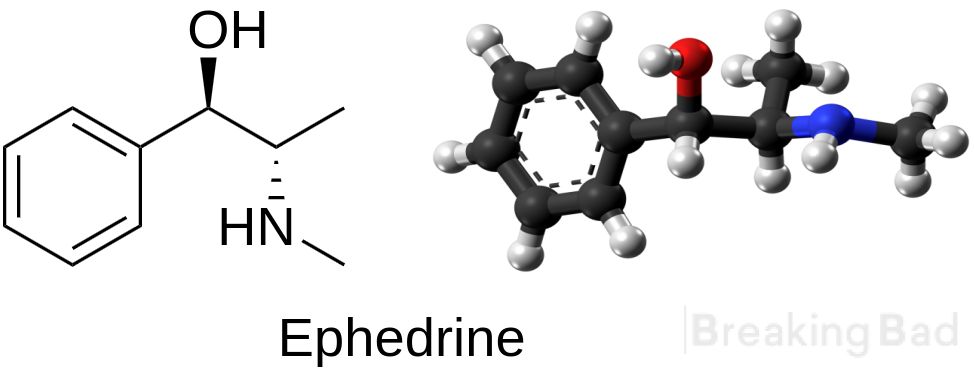
Обладая оптической изомерией и обладая двумя хиральными центрами, эфедрин дает четыре стереоизомера. Соглашение обозначает пару энантиомеров со стереохимией (1R,2S) и (1S,2R) как эфедрин, а пару энантиомеров со стереохимией (1R,2R) и (1S,2S) называют псевдоэфедрином. Функционально эфедрин является замещенным амфетамином и структурно аналогичен метамфетамину , отличающемуся только наличием гидроксильной группы (-ОН).
Коммерчески доступным изомером является, в частности, (-)-(1R,2S)-эфедрин. В устаревшей системе D/L (+)-эфедрин обозначается как D-эфедрин, а (-)-эфедрин обозначается как L-эфедрин, с фенильным кольцом, расположенным внизу в проекции Фишера.
Важно отметить, что часто возникает путаница между системой D/L (с маленькой буквой) и системой d/l (с строчными буквами), что приводит к неправильным названиям. В этом сценарии левовращающий L-эфедрин ошибочно называют L-эфедрином, а правовращающий d-псевдоэфедрин (его диастереомер) ошибочно называют D-псевдоэфедрином. Названия IUPAC для двух энантиомеров:
- (1R,2S)-2-метиламино-1-фенилпропан-1-ол
- (1S,2R)-2-метиламино-1-фенилпропан-1-ол, синонимом является эритро- эфедрин.
Физические свойства эфедрина:
Эфедрин представляет собой кристаллический порошок белоснежного цвета, без запаха или с легким ароматом. Имеет характерный горьковатый вкус. По форме эфедрин имеет кристаллическую структуру с четко выраженными геометрическими узорами. Примечательно, что эфедрин демонстрирует заметную растворимость в воде, что влияет на его состав в фармацевтических препаратах и медицинских препаратах.
В теплую погоду он медленно испаряется. Безводное вещество плавится при 36°С, а полугидрат плавится при 42°С. Это слабое основание с pKa = 9,6. Эфедрин разлагается под действием света. Растворы в масле могут иметь чесночный запах. Он растворим в воде (1 из 20), а также в спирте, хлороформе, эфире, глицерине, оливковом масле и жидком парафине (Windholz, 1983). Практически нерастворим в петролейном эфире при охлаждении.
Будучи сильным основанием, эфедрин вытесняет аммиак из своих солей. Растворы солей в воде с концентрацией от 1 до 10 процентов оказались чрезвычайно устойчивыми. Никаких изменений в прочности не произошло после 6 месяцев хранения при комнатной температуре. Растворы вполне работоспособны при температуре кипения.
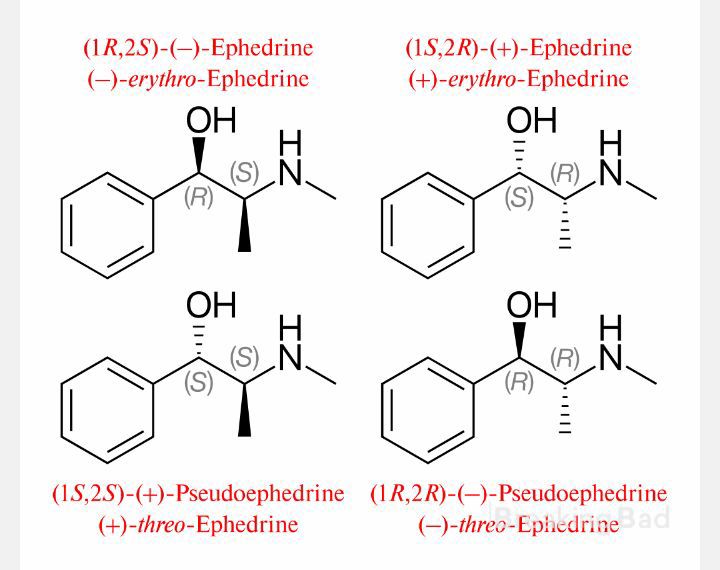
Свободное основание эфедрина (см. рис. 2):
- Молекулярная формула: C10H15NO
- Молекулярная масса: 165,2 г/моль
- Структурное название: (1R,2S)-2-метиламино-1-фенилпропан-1-ол
Эфедрина гидрохлорид:
- Молекулярная формула: C10H15ON·HCl.
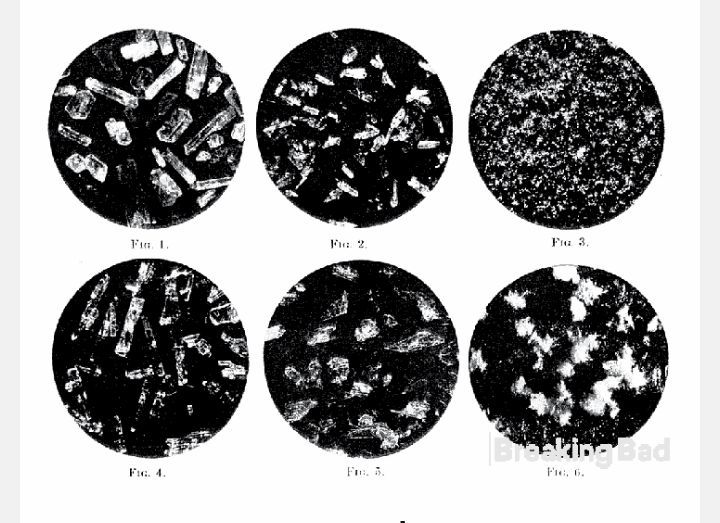
- Призматические иглы, т. пл. 216°C. Легко растворяется в спирте и воде. Его водный раствор стабилен при температуре кипения (см. рис. 1).
Сульфат эфедрина:
- Молекулярная формула: C10H15ON·H2SO4
- Шестиугольные пластины; Т.пл. 257°С. Трудно растворим в спирте, легко растворим в воде, нейтральен к лакмусам.
Эфедрина оксалат:
- Молекулярная формула: 2C10H15ON·C2H2O4.
- Призматические иглы из. вода; Т.пл. 245°С. с разложением; нейтральный по отношению к лакмусу; лишь очень мало растворим в холодной воде (см. рис. 3).
Эфедринфосфат:
- Молекулярная формула: C10H15ON·H3PO4.
- Кристаллизуется из спирта в длинные шелковистые иглы; т. пл. 178°С; кислота в лакмус.
Псевдоэфедрин:
- Чистый псевдоэфедрин кристаллизовался из спирта в ромбических призмах, т. пл. 118°С (см. рис. 4) . В отличие от эфедрина он лишь незначительно растворялся в воде. Его соли были получены и дали следующие физические константы.
Псевдоэфедрина гидрохлорид:
- Молекулярная формула: C10H15ON·HCl.
- Кристаллизуется из спирта в толстых иголках; т. пл. 179-181°С; очень растворим в воде и спирте (см. рис. 5).
Сульфат псевдоэфедрина:
- Молекулярная формула: C10H15ON·H2SO4.
- Призматические иглы; нет резкого МП; легко растворим в воде и спирте.
Оксалат псевдоэфедрина:
- Молекулярная формула: 2C10H15ON·C2H2O4
- Иглы; т. пл. 218°С с разложением; трудно растворим в спирте; очень растворим в холодной H2O; нейтрально к лакмусу (см. рис. 6).
Способы синтеза эфедрина:
Одним из основных способов получения эфедрина являются традиционные методы экстракции из растений рода Ephedra, особенно Ephedra sinica. Этот естественный подход использует богатое алкалоидами содержание этих растений, требуя тщательных процессов экстракции и очистки для выделения эфедрина из сложной матрицы.
Также существуют различные способы синтеза эфедрина.
Выбор между естественной экстракцией и химическим синтезом зависит от таких факторов, как стоимость, масштабируемость и желаемая стереохимия конечного продукта. Каждый метод представляет собой свой набор проблем и требует глубоких знаний принципов органической химии.
Применение эфедрина:
Эфедрин, стимулятор центральной нервной системы (ЦНС), обычно используется для предотвращения гипотонии во время анестезии. Хотя в прошлом он применялся при таких заболеваниях, как астма, нарколепсия и ожирение, он не является предпочтительным средством лечения этих заболеваний. Его эффективность в облегчении заложенности носа остается неясной. Способы введения включают пероральный прием или инъекцию в мышцу, вену или подкожно. Внутривенное применение приводит к быстрому началу действия, тогда как мышечная инъекция может занять около 20 минут, а пероральное употребление может занять до часа для достижения заметного эффекта. Продолжительность действия составляет примерно один час при инъекциях и до четырех часов при приеме внутрь. Эфедрин оказывает свое действие путем увеличения активности α- и β-адренергических рецепторов.

Первоначально выделенный в 1885 году, эфедрин начал коммерческое использование в 1926 году и занимает место в Списке основных лекарственных средств Всемирной организации здравоохранения. Он доступен в виде непатентованного лекарства и в природе встречается в растениях рода Эфедра. В Соединенных Штатах пищевые добавки, содержащие эфедрин, обычно запрещены, за исключением традиционной китайской медицины, где он известен как ма хуанг.
В медицинской сфере сердечно-сосудистые эффекты эфедрина аналогичны эффектам адреналина, вызывая повышение артериального давления, частоты сердечных сокращений и сократимости. Он действует как бронходилататор, аналогичный псевдоэфедрину, хотя и с меньшей эффективностью. Эфедрин исследовался для смягчения укачивания и противодействия седативному эффекту, вызываемому другими лекарствами от укачивания. Кроме того, его быстрая и устойчивая эффективность наблюдалась при врожденном миастеническом синдроме как у детей раннего возраста, так и у взрослых с новой мутацией COLQ.
Что касается потери веса, эфедрин способствует умеренной краткосрочной потере веса, особенно жира, но его долгосрочное влияние остается неопределенным. Соединение стимулирует термогенез в бурой жировой ткани, преимущественно встречающейся у мышей, и уменьшает опорожнение желудка. В сочетании с метилксантинами, такими как кофеин и теофиллин, эфедрин образует сложные продукты, такие как комплекс ЭКА, популярный среди бодибилдеров, стремящихся уменьшить жировые отложения. Систематический обзор 2021 года отметил потерю веса на 2 кг (4,4 фунта) при приеме эфедрина по сравнению с плацебо, что сопровождалось учащением сердечного ритма, снижением ЛПНП, повышением ЛПВП и отсутствием статистически значимой разницы в артериальном давлении.

Из-за структурного сходства с амфетаминами эфедрин может быть использован не по назначению для синтеза метамфетамина. Химическое восстановление эфедрина с удалением его гидроксильной группы является известным методом производства метамфетамина. Таким образом, эфедрин классифицируется как прекурсор.
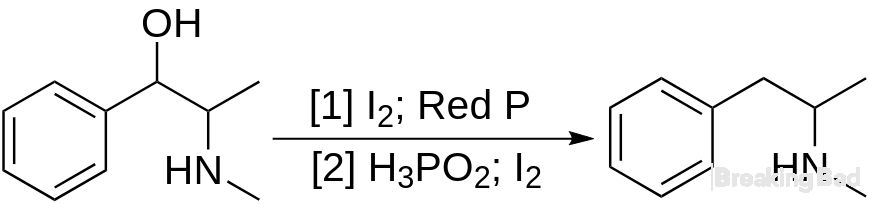
Синтез метамфетамина в форме эфедрина.
Правовой статус эфедрина:
Правовой статус эфедрина представляет собой сложную картину, сформированную различными юрисдикциями и опасениями по поводу возможности его неправильного использования. Его классификация варьируется по всему миру, что отражает многогранную природу этого соединения.
В фармацевтической сфере эфедрин известен своими терапевтическими применениями и часто доступен для медицинского применения в контролируемых условиях. Регулирующие органы могут устанавливать строгие правила относительно его назначения и применения, обеспечивая его ответственное использование в клинических условиях. Однако правовая ситуация становится более сложной, когда рассматривается вопрос о включении эфедрина в безрецептурные продукты, особенно в пищевые добавки.
Во многих регионах, включая США, введены строгие правила, регулирующие пищевые добавки, содержащие эфедрин. Из соображений безопасности, связанных с неправильным использованием эфедрина для снижения веса и улучшения спортивных результатов, несколько стран запретили или ограничили включение эфедрина в эти добавки. Однако существуют исключения, особенно в традиционной китайской медицине, где признаны и разрешены препараты, содержащие эфедрин, такие как ма хуанг.
Канада: Эфедрин может продаваться без рецепта для дыхательных целей в дозах по 8 миллиграммов.
Швеция: Эфедрин отпускается только по рецепту.
Хранение:
Храните это лекарство при комнатной температуре, от 59 до 77 ° F (от 15 до 25 ° C). Храните вдали от источников тепла, влаги и света. Не хранить в ванной. Храните эфедрин в недоступном для детей и от домашних животных.
Фармакология и токсикология:
Токсикодинамика:
Эфедрин может вызывать стимуляцию адренергических рецепторов и высвобождение норадреналина в нейронах (Kelley 1998).
Фармакодинамика:
Эфедрин обладает как альфа-, так и бета-адренергической активностью, а также прямым и косвенным действием на рецепторы. Он повышает кровяное давление как за счет увеличения сердечного выброса, так и за счет индукции периферической вазоконстрикции (Shufman et al., 1994; Parfitt, 1999). Это может вызвать бронходилятацию. При местном применении вызывает расширение зрачков. Основными метаболическими эффектами при передозировке являются гипергликемия и гипокалиемия. Эфедрин является стимулятором дыхания центрального действия и может повышать двигательную активность.
Токсичность:
Концентрация эфедрина у трех погибших составила 3,49, 7,85 и 20,5 мг/л (Kelley 1998). Однако сообщалось о выживаемости при уровнях 23 мг/л (Basalt and Cravey 1995).
Заключение:
В заключение, это исследование углубилось в сложные аспекты эфедрина, от его исторических корней до современного значения. Кристаллическая природа эфедрина, методы синтеза, разнообразные применения и юридические соображения были тщательно изучены.