Drug Discovery vs PharmDev, pt.2
επ.Pharm
Начало фармацевтической разработки
Итак, ранняя разработка позади. Вас уже выкупила биг фарма или её представители активно подкатывают к вашему CEO, ожидая результаты хотя бы I фазы и планируя разогнать всех сотрудников к чертям собачьим для реализации новых идей.
- Что у компании на руках после drug discovery?
Лучшая молекула, приблизительное понимание дозировки препарата и от чего он будет лечить. Если разработчик был умен, то молекула уже давно защищена патентом описывающим маркуш формулу и о конкурентах можно не беспокоиться. Если нет, ну штош.
- Что впереди?
Доклиническая разработка и 3 фазы клинических исследований, сбор документов и регистрация в соответствующим органе (МинЗдрав в РФ). Ничего нового
- В чем сложность?
Вопрос риторический🤷♂️ Свободный полет мысли ранней разработки начинает встречаться с суровой правдой фармацевтической разработки. С этого момента все активности по дизайну клиники и разработке препарата, должны быть зафиксированы и быть прозрачны, чтобы лет через 5-15 у регулятора (МинЗдрав) не было вопросов, а почему так вот поступили. Казалось бы чего тут сложного, но бизнес суров и начав свой жизненный цикл в компании №1, потаскавшись по компаниям, продукт в итоге может быть зарегистрирован компанией №5, понятно что сохранить целостность данных при этом сложновато.
Стримы в разработке
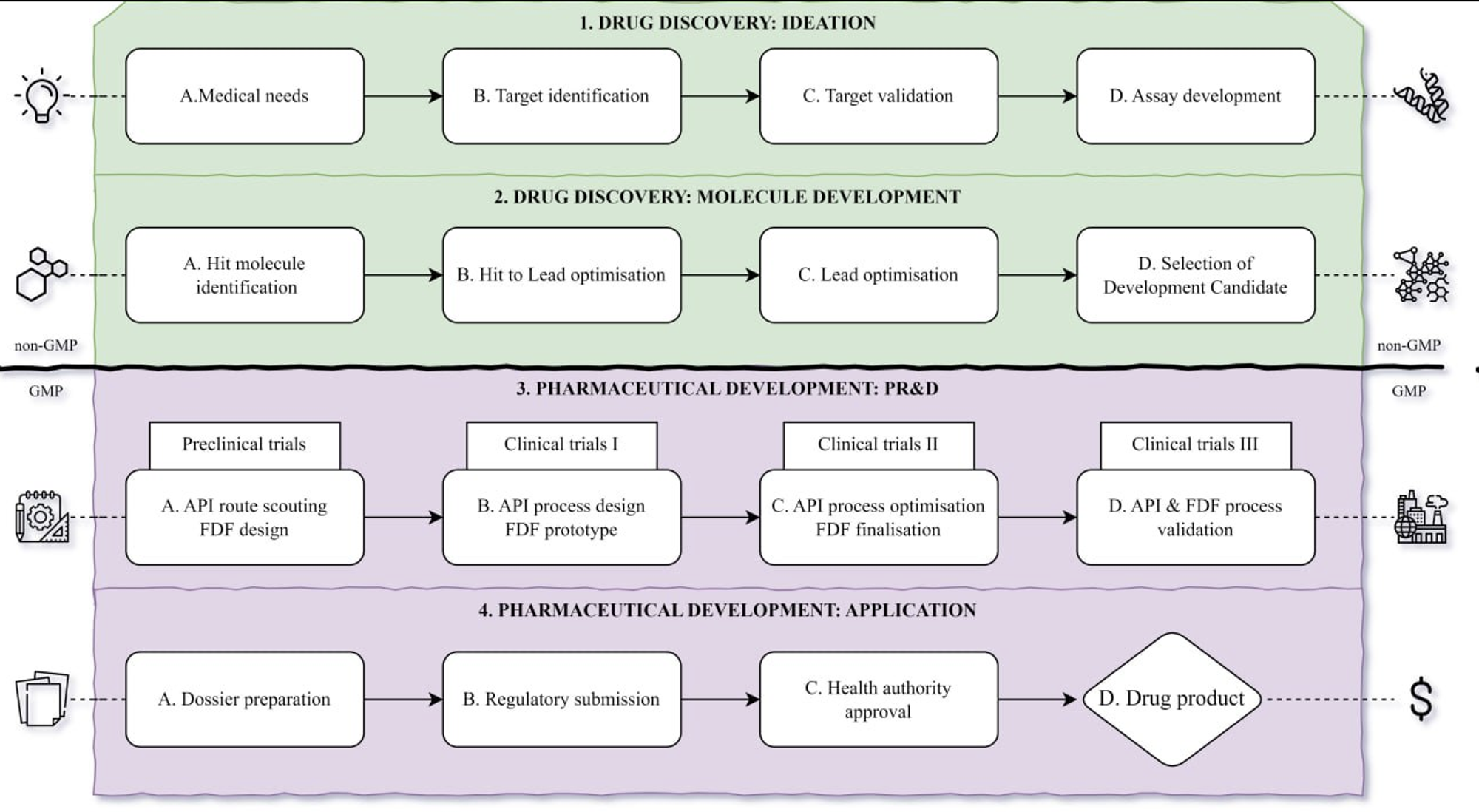
И опять я приведу общую схему. Как уже можно было догадаться сейчас мы говорим об этапах 3A-4D. То есть на выходе после этапа 2D у нас еще молекула и идея, а на 4D у нас уже проверенная таблетка или шприц готовый лечить людей за $$$. Нетрудно догадаться, что такая метаморфоза является результатом работы не 1-2 людей и поэтому можно пока верхнеуровнево пробежаться по основным стримам, которые происходят параллельно на этапах фармацевтической разработки.
Стримы придуманы и использованы автором для простоты, это понятие не принятое повсеместно.
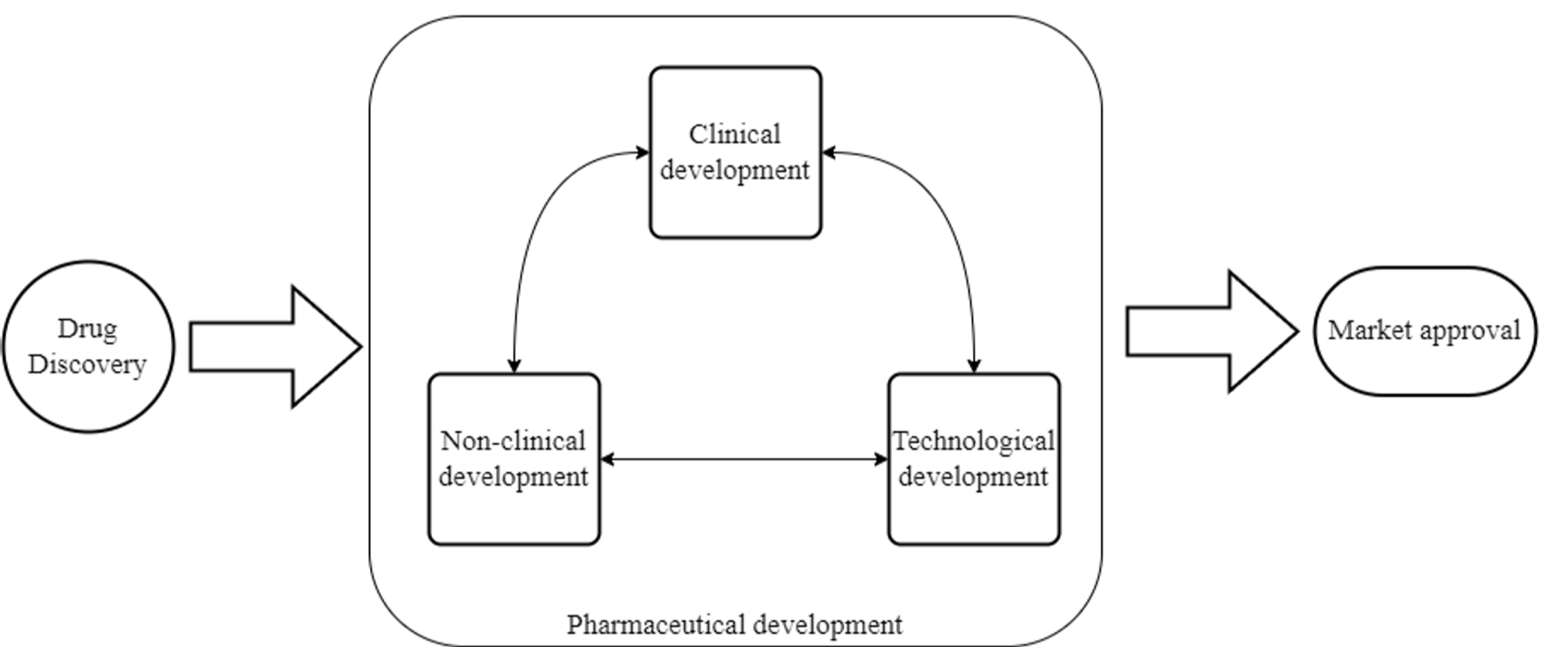
Стрим №1 - клиническая разработка (3B → 3D).
Ну название говорит само за себя. Когда говорят про “разработку препаратов” то обычно все дискуссии крутятся именно вокруг drug discovery и клинических исследований.
В данном стриме изучается эффективность и безопасность препарата в рамках показаний, которые сформулированы стейкхолдерами бизнеса. Несмотря на кажущуюся простоту финального результата, этот стрим является наиболее дорогой активностью. Именно на клинику уходят большая часть бюджета в сотни миллионов $.
Кто работает?
- Непосредственно специалисты-организаторы КИ / Clinical Research Associates
- Мониторы КИ / Medical Monitors
- Проджект менеджеры КИ / Clinical Project Managers
- Клинические дата менеджеры / Clinical Data Managers
- Биостатистические специалисты / Biostatisticians
- Клинические фармакологи / Clinical Pharmacologists
- Медицинские писатели / Regulatory and Clinical Document Writers
- Специалисты по качеству / Quality Assurance (QA) Specialists
- Представители этического комитета / Ethics Committees Review Boards
- Специалисты по фармаконадзору / Pharmacovigilance Teams
- И конечно специалисты по работе с регуляторными документам / Regulatory Affairs Specialists

Вроде никого не забыл и извиняюсь за возможно корявый перевод. Не стал расписывать функционал умышленно, потому что список и так большой, да и гугл пока еще работает и вообще организация клинических работ это отдельное искусство, требующее отдельного поста. Ну и из-за объемности работ эти активности всегда уходят на аутсорс в CRO.
Но чувствуется, что чего-то тут не хватает - изучения механизма действия препарата.
Стрим №2 - неклиническая разработка (3A→3D)
Рискну выделить как отдельный пласт работ немного отличающейся от клинической разработки.
Самые опытные сейчас скажут. “Так это же оно это, то самое, доклиника!”. Как бы да и как бы не совсем да. Что под собой подразумевает неклиническая разработка: исследование механизма действия изучаемой молекулы. То есть доклинические исследования являются началом и частью неклинической разработки, но неклиническая разработка при этом продолжается даже при окончании доклинических исследований.

Суть в том, что перед тем как давать субстанцию/препарат людям необходимо конечно изучить токсичность (острую/хроническую), подобрать дозировку, собрать данные по фармакологии, но при этом еще нужно изучить механизм действия. Поэтому, после доклиники, если все хорошо, то параллельно клинической разработке, часть испытаний на животных может продолжаться, чтобы понять, а как точно препарат работает.
Я акцентирую внимание на этом аспекте, потому что изучение механизма действия весьма захватывающая область разработки, которая при этом еще имеет академические вайбы. Необходимо разобраться и доказать как оно там работает в этих ваших организмах, на что разлагается и каким образом всё-таки реально оказывает действие, а не гипотетически.
Бывают случаи когда механизм действия так и остается под вопросом, это влияет на дизайн клинических исследований, где упор ставиться на терапевтическую эффективность, ввиду отсутствия биомаркеров.
Все гипотезы по механизму действия препарата описываются и заявляются при подаче разрешения на КИ и затем подтверждаются или опровергаются во время первых фаз клинических исследований.
Кто работает?
- Токсикологи / toxicologist
- Фармакологи (зачатую совмещают с ФК/ФД специалистами, очень модно нынче говорить о DMPK специалистах) / Pharmacologist or DMPK specialist
- Биохимики + Молекулярные биологи / Molecular biologist
- Специалисты по метаболомике / Metabolomics Scientists
В принципе из названий более менее понятно что происходит, просто отдельно выделю метаболомику - активности, когда специалисты вооружившись супер точными инструментами (пинцет и лупа) ищут в крови и других биологических жидкостях остатки препарата, идентифицируя во что он мог там превратиться, подкидывая инсайты фармакологам. Очень сложно и захватывающе на мой скромный взгляд.

Это у нас было все вокруг изучения препарата, как он именно работает, на ком именно, работает ли вообще или больше калечит. Теперь встает вопрос, а откуда собственно препарат берется?
Стрим №3 - технологический
Производится на заводах. Расходимся.
Но если всё-таки разбираться, то для удовлетворения потребностей всех этапов клинических исследований требуются килограммы и под конец уже, иногда, тонны субстанции. Из субстанции в свою очередь необходимо получить препарат, то есть таблетку, капсулу, ампулу. Для любителей разных ценностей может быть даже свечку. Чтобы было что за здравие поставить.
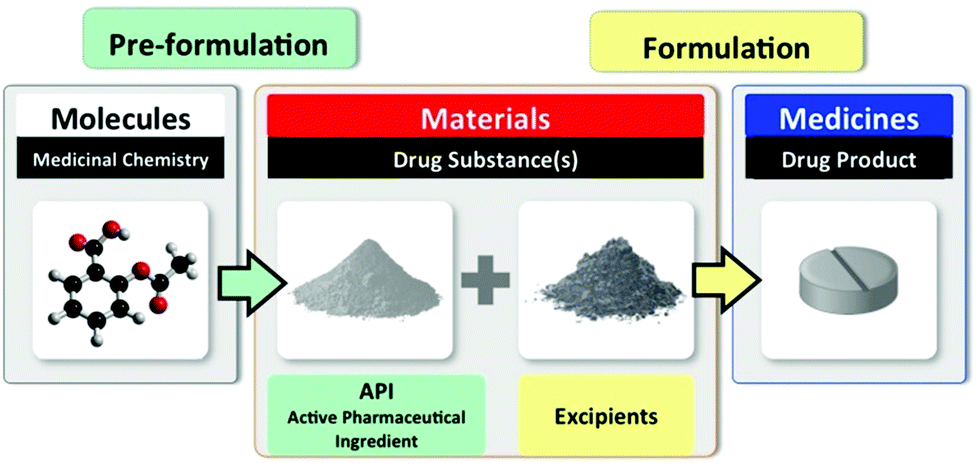
“Не ну а что, раз молекулу разработали, значит просто надо наварить её побольше, чтобы всем хватило.” - цитаты великих менеджеров в фармацевтике. Понятно что такой подход не работает, но почему именно - попробуем накидать на вентилятор конструктивно.
Все описываемые ниже активности в рамках технологического стрима происходят параллельно стримам упомянутым выше.
Требуемые количества
- На ранних этапах разработки молекулы (до этапа 2D), исследуемые количества ограничивались десятками миллиграмм субстанции, в худшем случае ну 1 грамм нужно было. Для таких количеств химики используют оборудование в виде колбочек и мензурок небольшого объема, всё это прекрасно умещается в вытяжном шкафу, легко обрабатывается и требует минимальной документации.

- Когда молекулярная разработка заканчивается, начинается уже серьезное дерьмо⚗️. Требуемые количества взлетают до сотен грамм. Всё это нужно скармливать мышам, отдавать на разработку аналитических методик, разработку препарата и DMPK исследования. То есть мы еще говорим о доклинике, но аппетиты уже неплохие (этап 3A).
Химикам уже надо суетится и придумывать более оптимальные подходы по получению целевой субстанции. Химия, которая хорошо работает на малые количества, обычно очень плохо работает на большие объемы. Поэтому тут подключаются процессные химики и разрабатывают новую технологию для молекулы, которую разработали медицинские химики. Это необходимо так как подходы к синтезу на ранних этапах были нацелены на максимальное разнообразие, но когда целевая молекула одна, то там уже необходимо увеличить эффективность по максимуму. В общем, как обычно, diversity vs based.
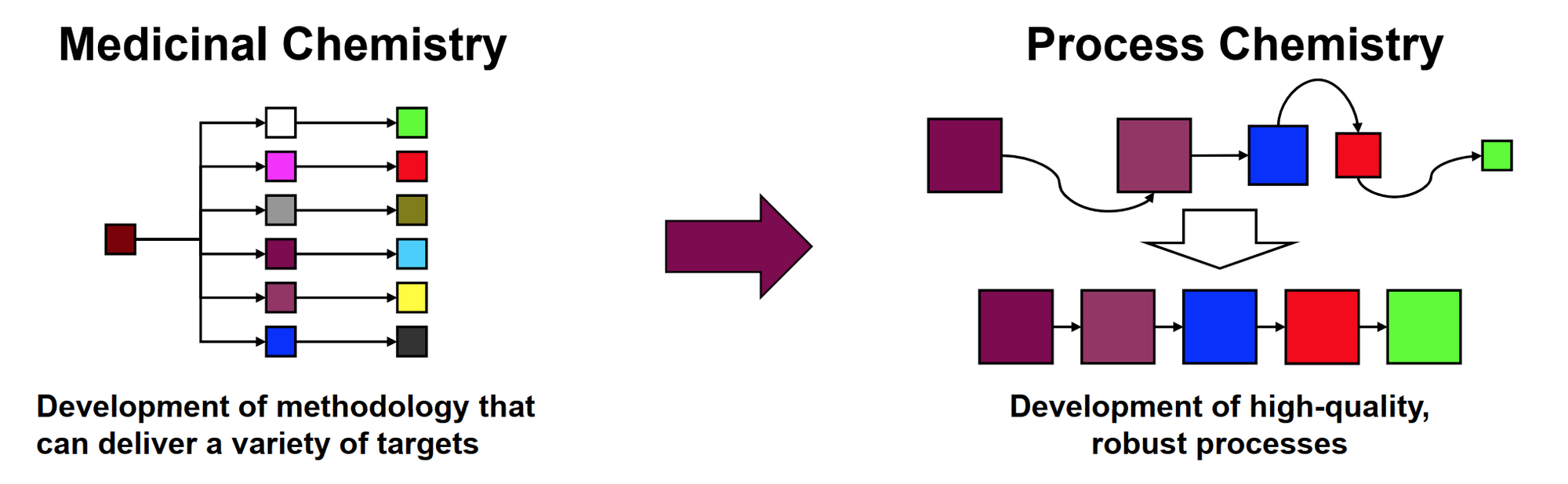
- Говоря про лекарственный препарат 💊, он тоже не появляется из ниоткуда, но при этом его надо тоже как-то разработать. Какую форму выбрать? Какую дозировку субстанции засунуть? А с чем оно вообще совместимо? Какую технологию вообще применить? Весь этот вал вопросов начинает решаться параллельно разработке и наработки тех самых сотен грамм субстанции. Подробностями буду грузить потом, но если нужен спойлер. Этим занимаются специалисты по разработке формуляций (formulation scientist), причем у них есть под специализации по ранней разработке (early formulation) и поздней разработке и конечно по типам формуляции.
- После того как доблестные мыши, кролики, поросята, собачки, хорьки, обезьяны (выбираем по вкусовым предпочтениям) отдали свои жизни ради блага не очень доблестного человечества, потребности в субстанции (АФС) и препарата (ГЛФ или ЛП) потребности опять резко возрастают уже до нескольких килограмм или тонн на этапах 3B-3D. Все процессы уже происходят в суровых стальных (эмалированных) реакторах.

Время о@уительных аналогий - вчера вы сварили борщ на одну порцию в ковшике на 300 мл из готового бульона и уже нарезанных овощей, получилось вкусно. И вам семья говорит - “Ну здорово вышло, давай-ка нам такого же борща на всю неделю, но подешевле, а то бюджет нерезиновый”, а семья у вас дружная, крепкая и большая. В итоге вы бегаете по кухне с 10 литровыми кастрюлями с придыханием “ух, бля” пытаясь сделать всё с нуля, потому что готовые ингредиенты уже дорого выходят на такое количество. И надо еще успеть всё сделать до того, как приедет дорогая тётя с борщем не хуже вашего.
Целевое качество
Куда мы без качества. Мы говорим о фармацевтике, тут всё серьезно, это вам не криптоинвестиции. Из общего стоит отметить, что все требования берутся не из воздуха, они прописаны максимально детально в соответствущих документах. Кто их придумал и откуда, это отдельный момент, пока оставим это за кадром.
Если фармацевтический продукт (лекарственное средство) было произведено не в соответствующих условиях (привет GMP), по качеству не соответствует требованиям (привет фармакопея), было исследовано в разрез с необходимыми условиями (привет уже GCP, GLP), то он не может считаться фармацевтическим.
То есть если была наварена тонна субстанции и она не прошла по одному из показателей, то скорее всего продукт отправиться в утиль (читатели из ООК не пинайте, я упрощаю же), т.к. не будет соответствовать грейду фармацевтического качества. Именно поэтому БАДы “хороши” тем, что там этой возни с качеством нет, что получилось то и зафасовали. И так сойдет.
Требования к качеству препарата и субстанции начинаются формироваться сразу же на этапе доклинических испытаний (3A) и неуклонно суровеют к 3 фазе клинических испытаний, когда менять уже что-то в процессе достаточно сложно. При этом все изменения в технологии фиксируются, документируются и вносятся в финальное досье. Этим занимаются специалисты CMC (chemistry manufacturing control) вместе со специалистами RA. Да это разные люди, а не вот это всё как обычно.
И тут мы вспоминаем про стримы №1 и №2. Зачем? А потому что от качества субстанции и препарата зависит эффективность и токсичность. Процессы получения еще не стабильны, сроки сжаты и возможности изучить химические аспекты препарата не так много, а это важно.
Например, для доклиники АФС нарабатывают по определенной технологии, что дает определенный профиль примесей - совокупный набор веществ, которые остаются в АФС. А для клиники процесс оптимизируют (количества же увеличиваются) и профиль примесей меняется. Так вот даже одна из новых примесей может давать токсический эффект. К сожалению никто не идеален и такое уже случалось и случится еще не раз.
Само же качество обеспечивается непосредственным производственным процессом, который изначально разрабатывается учеными, которые уже понимают регуляторные особенности. Следовательно от компетенций разработчиков, процессных химиков, их умению контактировать с производством и компетенций самого производства напрямую зависит качество продукта.
И в итоге что получается по качеству - следим за руками:
- Нужно провести клинические исследования, для этого нужно произвести препарат
- Для производства препарата его надо разработать и передать на производственную площадку
- Для разработки препарата надо произвести субстанцию
- Дла производства субстанции надо разработать технологию и передать её не площадку
- Для разработки субстанции нужно понимать какими целевыми характеристиками качества она должна обладать
- В лучшем случае это понимание будет прилетать через систематические обзоры по клинике, а в худшем случае (обычная ситуация) - разработчикам будет пофиг куда там надо будет субстанцию использовать.
Ладно вот для легкости чтения диаграмка:
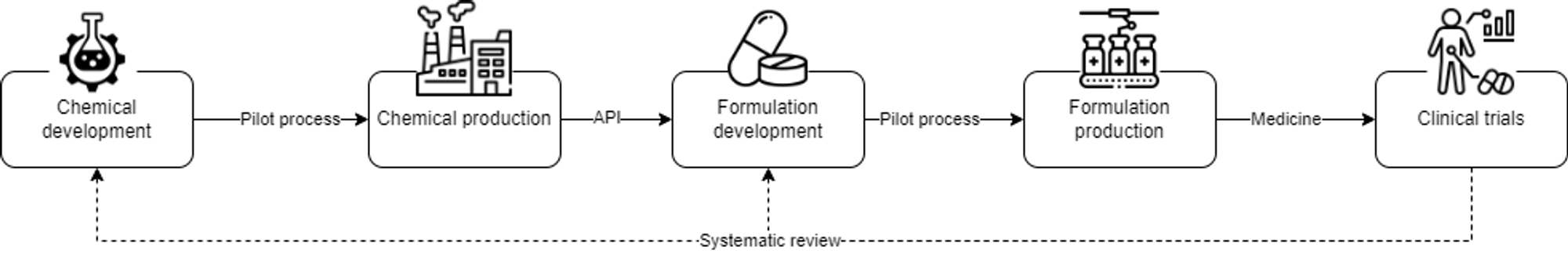
То есть, даже самые незначительные изменения в качестве на любом из этапов разработки, могут повлиять на результаты клинических исследований. А учитывая, что разработку АФС могут вести в одной стране, производство во второй, а разработку формуляции с производством в третей, то можно представить как непросто держать под контролем качество продукта через все упомянутые этапы.
Кто работает:
- Процессные химики / Process chemist
- Технологи ГЛФ / Formulation scientist
- Химики-аналитики / Analytical chemist
- Химические инженеры / Chemical engineer
- CMC специалисты / CMC specialist
- Специалисты по регуляторике / RA specialist
- ООК / Quality Assurance
- Менеджеры по трансферу / Technological transfer lead
- Менеджеры по проекту / Project lead
Суровый пул специалистов занимающихся продуктовой разработкой. От их компетенций, а самое главное умению общаться друг с другом зависит упомянутое качество продукта, а следовательно эффективность клинических исследований. Ну и вспоминаем про бюрократию. Все этапы должны быть описаны и зафиксированы, поэтому если по каким-то причинам схему синтеза было решено поменять посередине 1 или 2 фазы, то разработчик обязан оформить необходимые дополнения, переоценить риски по QbD, исследовать стабильность субстанции, препарата и т.д.
Как эти стримы работают вместе
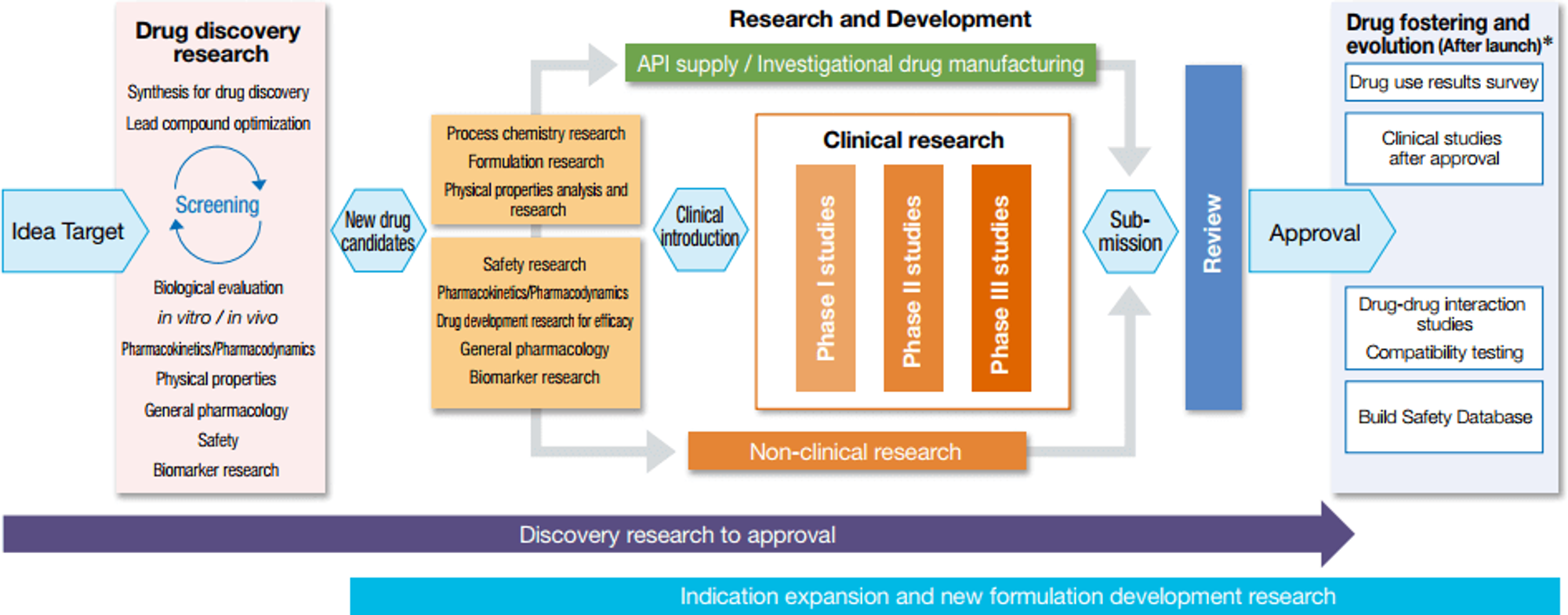
После этапа успешной номинации молекулярного кандидата встает вопрос организации доклинических и затем клинических исследований. Если компания большая, то молекулу просто передают в специальный департамент, который занимается фармацевтической разработкой. Ранняя разработка умывает руки и идет творить дальше.
Если же это стартап или компания небольшая, то те же самые химики начинают корпеть над наработкой десятков-сотен грамм веществ, а менеджмент пухнет над организацией доклинических испытаний и над подготовкой документов. Начинается бюрократический ад, который уже не закончится. Так что если у компании нет опыта и денег на внешних консультантов, то весь путь проходит через пробы и ошибки.
Поэтому не стоит удивляться после новости о перспективной молекуле, разработанной в стенах “ВладХимИнноСуперКластера”, что она так и не дошла даже до клиники, через N лет.
Ввиду тщательной разработки молекул начало доклиники это обычно не условный вопрос, а мероприятия, которые могут быть проведены в любом случае. А вот переход с доклиники на клинику будет уже зависеть от результатов самой доклиники.
Ну а если всё хорошо, есть ресурсы, компетенции и желание, то после номинации кандидата потихоньку запускаются все вышеперечисленные активности в параллельном режиме, в надежде не запутаться с организацией и успеть сделать всё в срок - конкуренты не дремлют
От связки экспертов сопровождающих клиническую, неклиническую разработку и технологической команды зависит скорость принятия решений и возможность оперативно подработать моменты с качеством препарата. Для этого обычно существуют проектные менеджеры, которые могут увидеть затык клинической команды и оперативно её связать с технологической. Это конечно при условии наличия менеджера вообще и его достаточной мотивации для работы.
Итого

От исходного дизайна молекулы и предполагаемой индикации (от чего лечим собственно) зависят активности фармацевтической разаработки. Если молекула оказалась сложна или предполгаемая индикация не сработала на клинике, то шансов на успех обычно не остается. Нет ТЗ, результат ХЗ.
Хотелось бы вы выдать в итоге идеальный рецепт разработки препаратов от идеи до рынка, но его не существует. Думаю теперь понятно, что исследования всегда очень легко завести в тупик из-за попыток сэкономить на экспертах, можно тупо запутаться в организации, документах или потратить весь бюджет до получения каких-то результатов, которые позволят привлечь инвесторов.
Экспертиза и опыт сотрудников сильно повышают шансы на успех, при условии что молекула добралась до 3 фазы клинических испытаний, но до этого приходится уповать еще и на везучесть (обычно используют термин serendepity).
Страшно представить сколько денег и усилий было потрачено ради того, чтобы в итоге запнуться на фиговом дизайне клинических исследований или неквалифицированной разработке препарата/субстанции.
Конечно фармацевтическая область продолжает развиваться, каждый месяц разрабатывают новые мишени, развиваются новые технологии, появляется шанс излечения самых суровых заблолеваний, но шансы на успех остаются всё теми же, потому что основной фактор остается неизменным - люди и их умение здраво и систематизированно подходить к принятию решений.