Drug Discovery vs PharmDev, pt.1
επ.Pharm
В чем же главное отличие drug discovery и почему он не считается этапом фармацевтической разработки как таковой? Потому что всем безразлично. То есть регулятору и другим бюрократам в длинной цепочке фармы в принципе все равно откуда молекула появилась, хоть форточкой надуло, хоть пророк нашептал - не имеет значения.
Легальное и контролируемое поле исследований молекулы начинается с этапа доклинических исследований (не путаем с ФК/ФД на животных моделях) где уже изучают можно ли давать АФС и прототип ГЛФ обезьянам поумнее (т.е. людям) на более поздних этапах.
Все работы и активности на этапе молекулярного дизайна, от идеи до номинации молекулы на доклинику, не освещаются в финальном CTD на продукт.
А это значит что? Правильно - тотальная анархия на ранних этапах разработки абсолютно легитимна. При отсутствии адекватного контроля и метрик весь процесс drug discovery (DD) превращается в некоторого рода искусство. Да компании активно работают над KPI, но всегда же можно сказать менеджменту, что мишень просто undruggable и спокойно умыть руки. В принципе от этого страдает большая часть стартапов в фарме.
В итоге мы имеем шанс того что молекула, которую мы синтезировали и отдали на панель in vitro тестов дойдет до коммерции примерно 1 к 30,000. Если что шанс выиграть в рулетке 1 к 37. То есть разработка молекул это лотерея для умных и богатых😅 Ну может не все так и плохо и стоит добавить, что если рассматривать молекулы с этапа номинации на доклинические исследования то шанс успеха составляет в среднем 15%, что уже конечно чуть лучше. Другими словами в процессе DD мы повышаем наши шансы с 0.003% до 15% - до сих пор сомнительно, ну о’кей.
С шансами разобрались, а почему они такие низкие в итоге все равно? - раздутость процессов и тяга к фундаментальной науке. Вернемся к схеме, сшакалю её сюда для простоты.
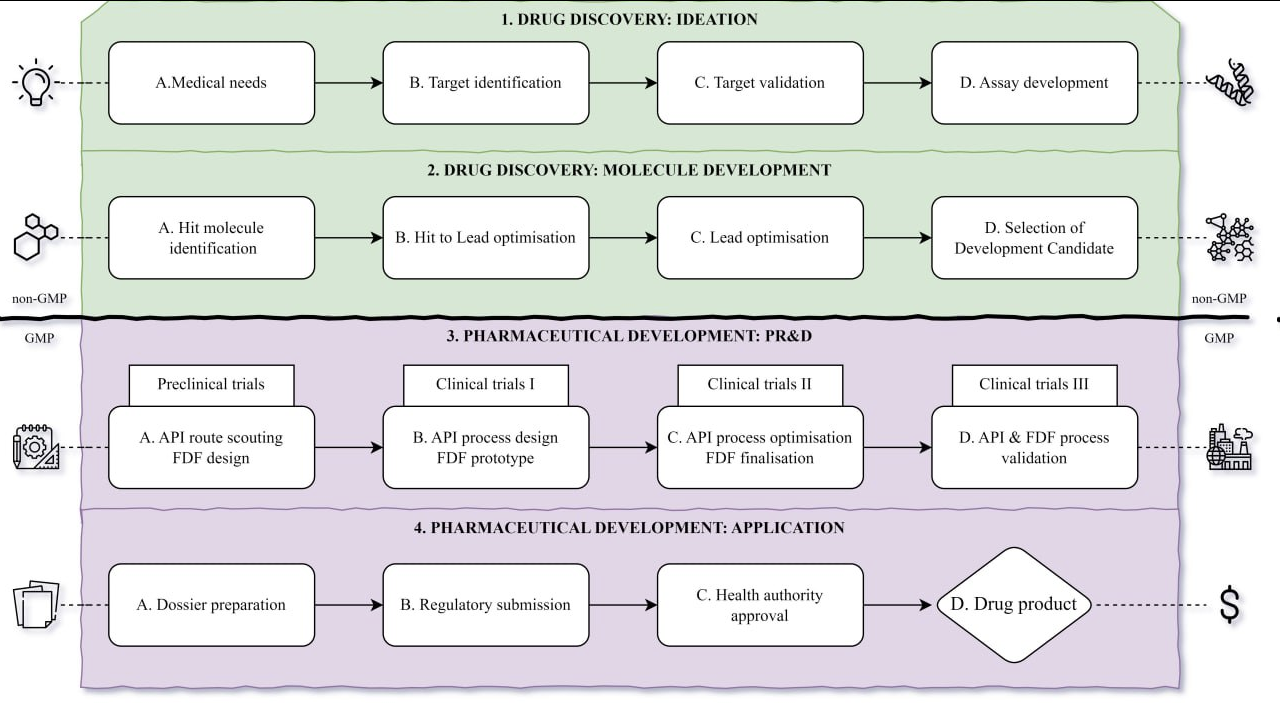
Этап 1B-1С: поиск мишени
Максимально важная веха в разработке препарата. Исследователи должны найти целевой белок который отвечает за непосредственный патогенез (вот хороший материал, если интересно). Обычно это не является прямой бизнес задачей фармацевтических компаний - это слишком дорого и долго, поэтому это падает на плечи ученых в институтах, которые в свою очередь волнуются за публикации в Q1-Q2 журналах, чтобы методы и результаты подходили под критерии уважаемого (или не очень) издания. К сожалению, журнальные требования к методам не всегда обеспечивают необходимое GxP качество данных и мишень криво валидируется, делаются поспешные выводы, что приводит к тому что весь цикл разработки запускается с прицелом на неверную мишень.

Время о@уительных аналогий - надо было стрелять в дерево, а наводчик оказалсятупнедобюджетирован и обойма зарядов спускается в песок или воздух.
Почему же не дождаться перепроверки данных по мишени другими исследователями парочку лет? Если мишень перспективная и давно ожидаемая, то компании или другие группы исследователей сразу же начинают разрабатывать потенциальные first-in-class препараты обильно патентуя химическое пространство.
В итоге можно не успеть на банкет и тогда останутся объедки с химического стола и придется ковыряться оптимизацией по me-too подходу, аккуратно обходя все патентные ограничения. Да, можно еще не угадать с индикацией, потенциальными дозировками и путями введения, что тоже важно при оформлении патента. Уже все очень сложно, а что дальше?
Этап 1D: In Vitro Тесты.
Допустим с мишенью всё ок, никто не накосячил и все говорит о том, что именно выделенный белок ответственен за пролиферацию (рост) клеточек рака или другой патогенез. Доблестные молекулярные биологи разрабатывают тест, который говорит в какой концентрации происходит 50% ингибирование (ну или деактивация) целевого белка - IC50. Меньше лучше - обычно цель это наномолярные концентрации - nM, но это уже мелочи.
Так вот in vitro тест это анализ, а любой анализ выполняется по методике. Все кто хоть как-то соприкасался с фармой знает, что для того, чтобы можно было верить результатам методика должна быть квалифицирована хотя бы частично. Но я напомню, что на данном этапе интереса регулятора нет, то есть вся ответственность лежит на компании и это только в её интересах вложить чуть больше денег в разработку тестов, чтобы обеспечить их правильность. Но тяга к экономии всегда побеждает здравый смысл. Было бы неправильно говорить, что все подряд игнорируют эти требования, но практика показывает, что зачастую команды исследователей недооценивают важность, например, точности метода и в итоге разработка полнится ложноположительными или ложнонегативными данными.

И почему же так происходит - зачастую никто, начиная от лаборантов и заканчивая менеджментом, не задается этими метрологическими вопросами просто из-за фундаментально научного уклона самих работ, полученного образования и ограниченности временных ресурсов. Особенно печально то, что иногда правда так и не вскрывается и разработка заканчивается с “нерабочими” молекулами на руках. Публикуется статья по типу - мы все сделали правильно, но что-то недоглядели, we are very sorry. Вспоминаем пример с Семагацестатом и забываем сотни миллионов $ спущенных в карманы причастных. И это мы еще про ADMET тесты молчим, ну это потом.
Ладно всё хорошо - мишень есть, тест допустим разработан и команда готова тестировать 300к молекул в секунду. Где взять молекулы?
Этапы 2A-2D: Поиск Молекулы
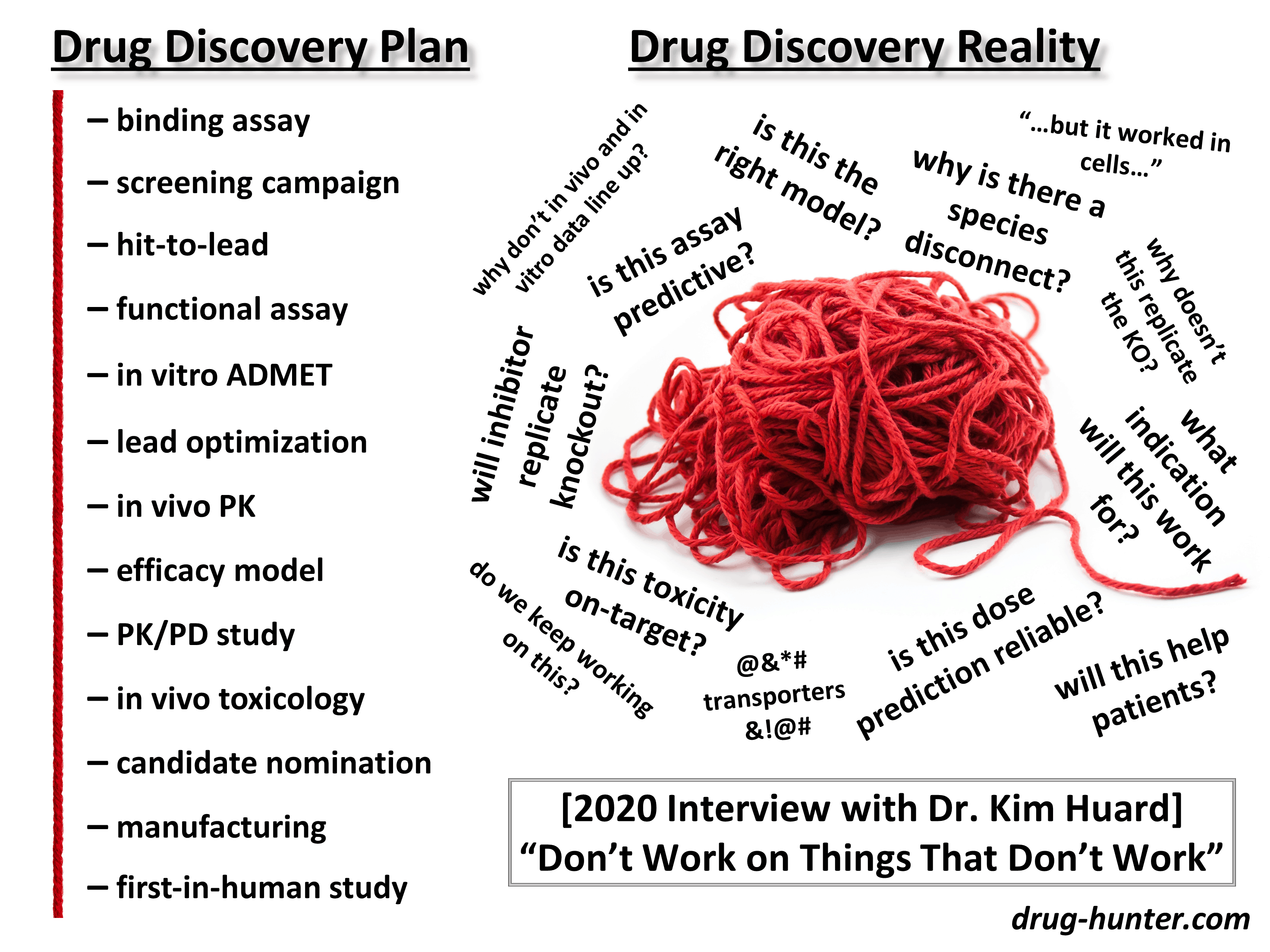
Это моя любимая веха в ранней разработке молекул. Обычно мне сразу вспоминается эта картинка:

Подходы к поиску “той самой” молекулы очень разнообразны, но сейчас суть можно сжать в пять пунктов:
- HTS (high throughput screening) - скрининг наиболее оптимального молекулярного ядра из имеющихся молекул с помощью мокрого или компьютерного скрининга. Тут проверяется только целевая активность к мишени. Сами молекулы берутся из внешних или внутренних каталогов уже синтезированных веществ или из теоретических списков молекул, которые можно будет в теории быстро сварить.
- H2L (hit-to-lead) оптимизация выбранного ядра с целью увеличения активности молекулы. Тут химики навешивают на это ядро различные функциональные группы (как на елочку игрушки). Цель - максимально увеличить аффинность (целевую активность)
- Lead Optimisation - работа с лучшими молекулами, чтобы они худо-бедно проходили целевые показатели in vitro ADMET тестов. То есть, чтобы хотя бы в колбочке они походили на молекулы, которые можно дать животным (просто напоминаю что люди не животные).
- Номинация кандидата - это как выбор Чаши Грааля. Из 10-20 молекул надо выбрать 5-6 штук, чтобы отправить их на съедение мышкам и проверить биодоступность с помощью фармакокинетических исследований. Все in vivo тесты не бесплатны, поэтому команде исследователей надо хорошо подумать прежде чем отправлять конкретную молекулу на фармакокинетику и ФД модель.
- В случае успешных скрининговых ФК/ФД исследований лучшая молекула уходит в фармацевтическую разработку на радость разработчиков, инвесторов и бизнеса, но мы помним что шанс того что молекула пройдет все следующие этапы до регистрации всего лишь 15%. Шампанское открывать еще рано.
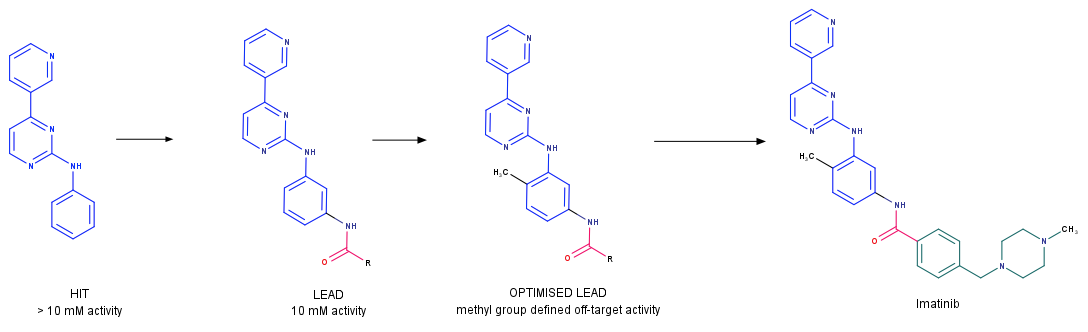
В итоге с точки зрения химии это выглядит так, на примере Иматиниба. Да выглядит просто, бабушка в гараже сварит на изи, но вот такая разработка заняла >10 лет, где пришлось перебрать 400,000 молекул.
Организация работ
В разработке молекул обычно участвуют несколько классов персонажей (вся жизнь это DnD, только на руках обычно всего лишь кость 1d1):
- Химики-синтетики (a.k.a. медицинские химики) - боги и элита. Занимаются синтезом и возможных идей по модификации молекул. Без них никакого драг дизайна в принципе быть не может. От их способностей зависит продуктивность всего процесса, чем больше молекул будет произведено, тем больше шансов попасть в цель. Обычно это кандидаты наук (PhD) или магистры в области орг. химии.
А дальше идет всякая челядь (автор иронизирует если что) - Хемоинформатики - максимально саппортят синтетикам (чем вызывают раздражение у последних) и пытаются оцифровать все возможные идеи. Считают возможную активность у предполагаемых молекул, дизайнят наиболее оптимальные молекулы и пытаются предсказать ADMET свойства. В современной команде по разработке находятся по умолчанию, иначе за конкурентами не поспеть. Обычно это переученные синтетики, но в последние 5 лет количество магистратур и PhD на эту тему астрономически выросло, поэтому компании предпочитают набирать готовых PhD-хемоинформатиков из ВУЗов.
- Молекулярные биологи - те про кого обычно забывают. Усердно прогоняют все что наварили синтетики на ADMET свойства. От качества их данных как раз зависит какие будут приняты в дальнейшем решения. То есть когда мы видим предложение - "наша супер модель была обучена на in vitro данных и мы предсказали лучшую молекулярную структуру", то вот эти данные это результат работы биологов. Естественно это тоже база - какой DD без in vitro тестов. Говоря о специалистах - это магистры или PhD в области биологии.
- Технический Менеджер - человек из поля, кто понимает что происходит и по идее должен быть ответственен за весь процесс разработки. Даже после PhD из крутых групп, на такие должности обычно не назначают сразу и нужно 3-4 года опыта работы, чтобы попасть на такую позицию. И говоря про опыт мы имеем в виду кого-нибудь из вышеперечисленных специалистов.
- И еще до кучи нужны - патентоведы, DMPK специалисты ну и конечно бизнес девелопмент, чтобы держать руку ну пульсе, gate review сам себя не сделает.
Звучит как солидный пул специалистов. Что их всех объединяет? - Отсутствие индустриального GxP опыта разработки препаратов, что не равно молекулы. При этом у рынка нет внешнего запроса на внедрение таких компетенций на этапе ранней разработки, потому что цель фармацевтической разработки это изучение эффективности, токсичности и возможных химических свойств разработанной молекулы - то есть всё что важно пациенту и всё к чему только идут на этапе drug discovery. И гипотетическому потребителю не очень важно как удалось перейти от этапа hit к этапу номинации молекулы.
Можно подумать, что автор сетует - "регуляторики на ваш drug discovery не хватает", но это не так. Гибкость молекулярной разработки, позволяет сэкономить хоть какое-то количество денег и не быть зажатым регуляторными рамками, чтобы успевать принимать решения и выводить лекарства чуточку быстрее. Тем более в данном случае риски несет только кошелек компании, а не гипотетический пациент.
Конечно каждый из этапов drug discovery занимает кучу времени, сил, денег и не гарантирует правильность выбора. В любой момент можно принять неверное решение и пойти по пути оптимизации не того молекулярного ядра из-за ложноположительных результатов, личных предпочтений хемоинформатиков или синтетиков, неверной интерпретации или передачи данных и т.д. Есть вероятность уйти в неправильную ветвь решений и в итоге потратить 1-3 года копаясь не с тем хемотипом, израсходовав весь возможный бюджет.
В дополнение к упомянутым трудностям, стоит добавить, что ввиду бизнес особенностей, молекулы или идеи по их дизайну, нередко передаются в другие лаборатории или компании посередине любого из вышеупомянутых этапов, что обычно не улучшает качество и скорость разработки. Мы же все сталкивались с тем, что часть данных остается в голове у ответственного и уходит в небытие вместе с ним же. Это все является следствием того, что область ранней разработки не регулируема и происходит хаотично.
Как все эти мины ранней разработки отражаются на фармацевтической разработке, а именно про этапы 3A-3D, напишу в следующей части.