Диета При Кишечной Метаплазии Желудка

⚡ 👉🏻👉🏻👉🏻 ИНФОРМАЦИЯ ДОСТУПНА ЗДЕСЬ ЖМИТЕ 👈🏻👈🏻👈🏻
Вопрос для защиты от спама. Введите ответ с большой буквы:
Отправляя персональные данные из этой формы, Вы подтверждаете свое согласие на обработку персональных данных и соглашаетесь с политикой конфиденциальности .
(c) 2017 - 2021. Андрей Горковцов. Врач-эндоскопист. Все права защищены. Копирование материалов сайта допускается только со ссылкой на источник.
Кишечная метаплазия желудка является предраковым изменением слизистой оболочки желудка и связана с повышенным риском дисплазии и рака. В патогенезе прогрессирования от предраковых состояний к аденокарциноме желудка кишечного типа, согласно предложенного каскада Correa, считают переход от нормального эпителия желудка через воспаление, атрофию, внутрислизистую карциному, и наконец, к инвазивной карциноме. Множественные факторы риска были связаны с развитием взаимосвязи кишечной метаплазии желудка, включая инфекцию желудка H. pylori, генетических факторов, экологической среды, ревматических болезней, табакокурения, питания, желчного рефлюкса и кишечной микробиоты. Во всем мире в странах с высоким уровнем заболеваемости разработаны руководящие принципы скрининга.
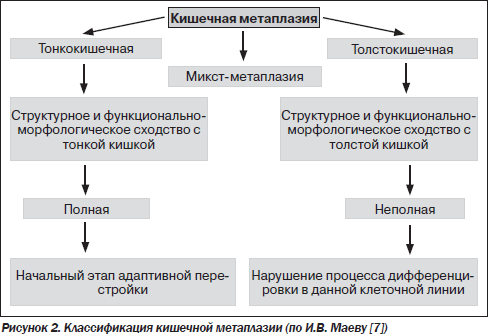
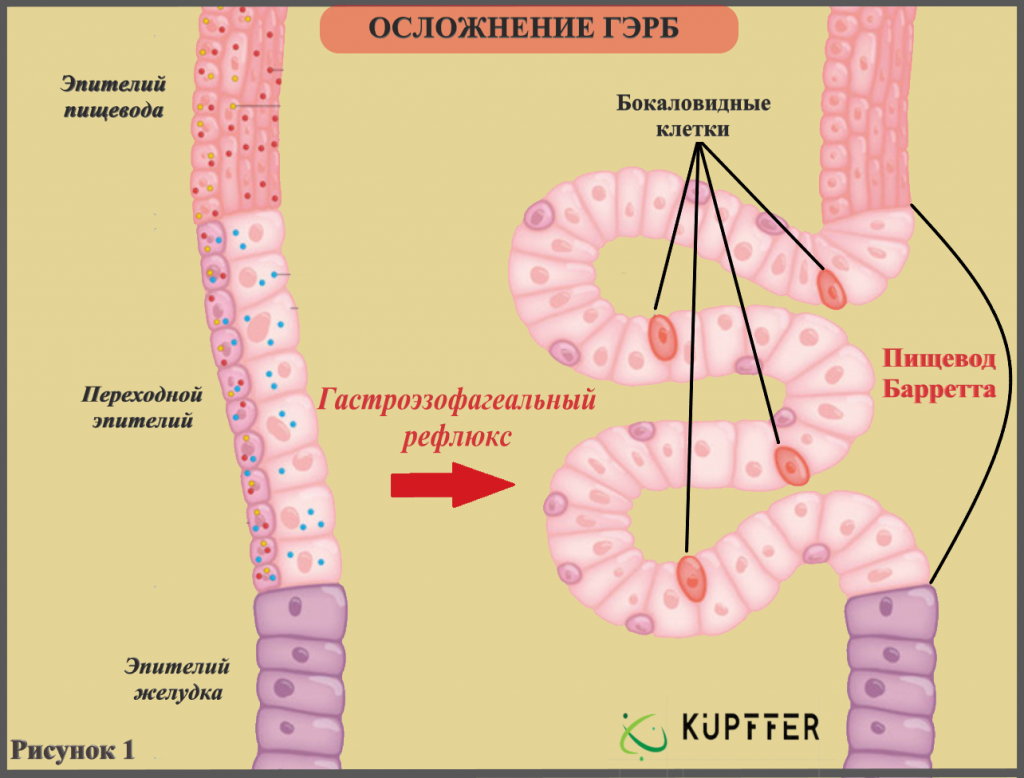
Кишечная метаплазия желудка определяется как замена поверхностного, фовеолярного, и/или железистого эпителия кислотопродуцирующей или антральной слизистой желудка кишечным эпителием. Кишечная метаплазия желудка характеризуется анатомически как ограниченный процесс, если он находится в одной области желудка или как обширный, если вовлечены две области желудка. Гистологически кишечная метаплазия желудка считается либо полной, либо неполной. Полный (I тип) кишечная метаплазия определяется слизистой оболочкой тонкой кишки со зрелыми абсорбирующими клетками, бокаловидными клетками (Гоблета) и щеточной каймой. Неполная (II тип) кишечная метаплазия секретирует сиаломуцины и сходна с толстокишечным эпителием с цилиндрическими “промежуточными” клетками на различных стадиях дифференцировки, неравномерными каплями муцина и отсутствием щеточной каймы.
Самый высокий риск развития рака желудка связан с неполным и/или обширной кишечной метаплазией желудка. Систематический обзор, который включал 10 наблюдательных исследований по всей Европе, Азии и Латинской Америке в диапазоне от 10 месяцев до 19 лет наблюдения, показал, что риск рака желудка составляет в 4-11 раз выше при наличии неполной метаплазии по сравнению с ее отсутствием.
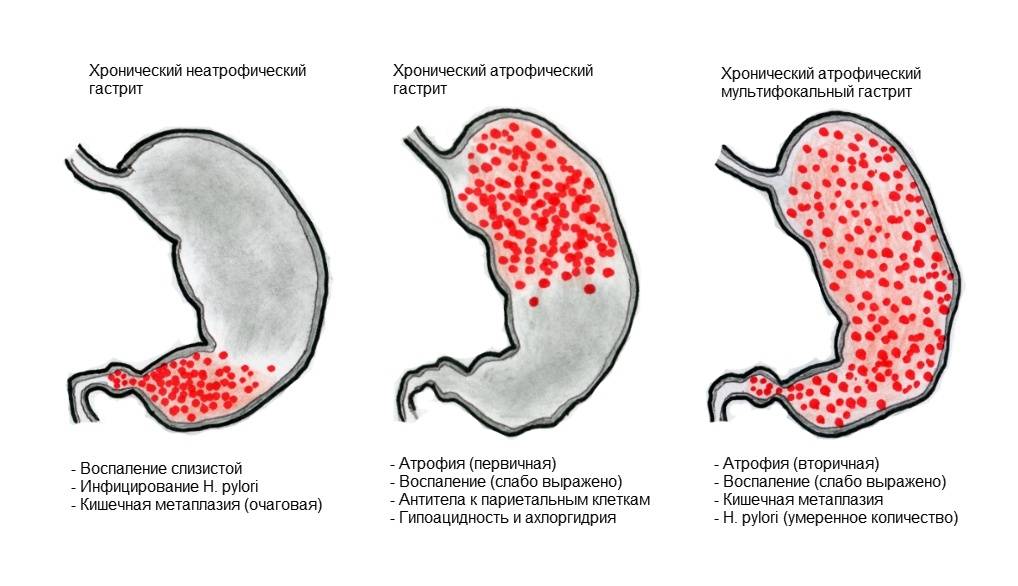
Первым изменением в гистологическом каскаде является либо активное хроническое воспаление неатрофического хронического гастрита, характеризующегося наличием желез, либо мультифокальный атрофический гастрит. Последующие гистологические изменения прогрессируют через появление полной метаплазии, неполной метаплазии, дисплазии низкой и высокой степени с последующей карциномой. В Нидерландах было проведено общенациональное когортное исследование для оценки риска развития рака желудка, связанного с различными предраковыми поражениями желудка. Атрофический гастрит, кишечная метаплазия, умеренно выраженная дисплазия, и высокая дисплазия были связаны с ежегодной заболеваемостью рака желудка в 0,1%, 0,25%, 0,6%, и 6,0%, соответственно. Заболеваемость раком желудка, ассоциированным с кишечной метаплазией желудка, в систематических обзорах колеблется от 0% до 10%, причем переменный диапазон обусловлен различными размерами выборки и периодами наблюдения.
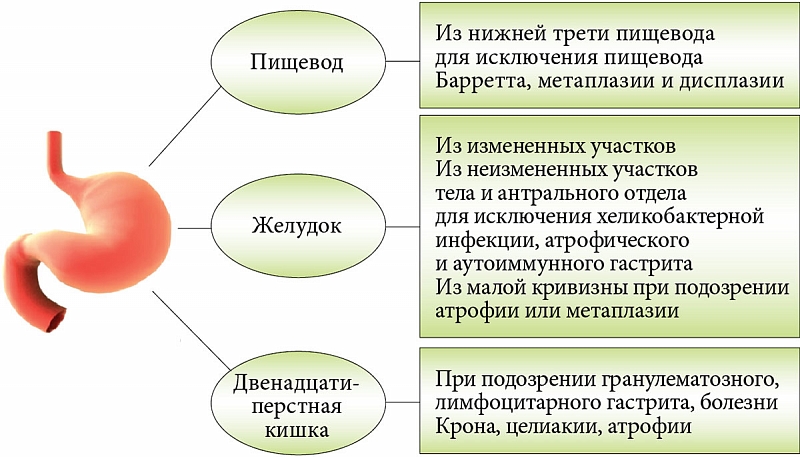
Пациентам с высоким риском рекомендовано пройти эндоскопическое обследование с картированием биопсий по модифицированной Сиднейской системе (MSS) из 5 точек – антрального отдела (большая кривизна, малая кривизна), угол желудка и тело желудка (большая кривизна, малая кривизна). Следует отметить, что биопсии тела особенно ценны после длительного лечения ингибиторами протонной помпы, так как кислотопродуцирующая слизистая оболочка может быть изолировано инфицирована H. pylori. Биопсии с угла желудка также особенно важны, так как они, скорее всего, выявят максимальную атрофию, кишечную метаплазию и предраковую дисплазию. De Vries и его коллеги провели проспективное многоцентровое исследование в 2010 году. Золотым стандартом считалось получение 12 биопсий. На основе MSS (5 биопсий) выявили 90% пациентов с кишечной метаплазией желудка и 50% пациентов с дисплазией, в отличие от 97% и 100%, соответственно, когда было получено не менее 7 биопсий. De Vries и его коллеги пришли к выводу, что по крайней мере 9 биопсий, в том числе из кардии, необходимы для адекватного наблюдения предраковых поражений в популяции с низкой частотой рака желудка, к которым относятся европеоиды и белые американцы не испанского, африканского или восточноазиатского происхождения.
В настоящее время ASGE не рекомендуют общее наблюдение за людьми с кишечной метаплазией желудка, если не присутствуют другие факторы риска рака желудка, например, семейного анамнеза рака желудка и азиатского происхождения. Однако, европейский партнер, ESGE, рекомендует лечение H. pylori, если установлено, что пациент заражен бактериями, с последующим картированием биопсий по выявлению дисплазии каждые 3 года. Если слабая дисплазии (LGD) обнаруживается у пациента с кишечной метаплазией желудка, то ЭГДС с картированием необходима в течение 1 года для оценки эндоскопически видимых поражений. Пациентам с подтвержденной дисплазией высокой степени (HGD) при отсутствии эндоскопически видимого поражения рекомендуется повторное ЭГДC через 6-12 месяцев для наблюдения видимых поражений. Эти пациенты с поражениями должны пройти надлежащее либо хирургическую, либо эндоскопическую резекцию из-за высокой вероятности сосуществования инвазивной аденокарциномы, так как 25% пациентов с дисплазией высокой степени могут спрогрессировать до аденокарциномы в течение 1 года.
David S. Jencks, Jason D. Adam, Marie L. Borum, Joyce M. Koh, Sindu Stephen, David B. Doman. Overview of Current Concepts in Gastric Intestinal Metaplasia and Gastric Cancer. Gastroenterol Hepatol (NY). 2018 Feb; 14(2): 92–101.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5866308/
*Цена указана за один эпизод диагностики болезни. Окончательная цена рассчитывается индивидуально исходя из количества эпизодов
Встречный бой – это ведь не на стрельбище, целится некогда. Попал, не попал…
«Итак во всем, как хотите, чтобы с вами поступали люди, так поступайте и вы с ними». Евангелие от Матфея (гл. 7, ст. 12)
Отправляя персональные данные из любой формы на сайте, Вы подтверждаете свое согласие на обработку персональных данных и соглашаетесь с политикой конфиденциальности .
Главная
Пациентам
Врачам
Литература
Справочник
Аппаратура
Фото
Видео
Исток-Система
Кишечная метаплазия слизистой оболочки желудка в практике гастроэнтеролога: современный взгляд на проблему
И.В. Маев, О.В. Зайратьянц, Ю.А. Кучерявый
Московский государственный медико-стоматологический университет
Понятие о нарушении клеточного обновления
Хронический гастрит и Helicobacter pylori
Хронический гастрит как предраковое заболевание
Типы кишечной метаплазии и риск развития рака желудка
Возможно ли обратное развитие атрофии и кишечной метаплазии?
Информация на сайте www.gastroscan.ru предназначена для образовательных и научных целей. Условия использования.
Главная
Пациентам
Врачам
Литература
Справочник
Аппаратура
Фото
Видео
Исток-Система
При любых повреждениях слизистой оболочки активируется пролиферация, ускоряется миграция клеток, что ведет к восстановлению структуры и возвращению клеточного обновления в исходное состояние. При хроническом гастрите процесс клеточного обновления в слизистой оболочке нарушается (дисрегенерация), что вызывает ускоренное перемещение клеток из генеративной зоны без полноценной дифференциации в зоны расположения зрелых специализированных эпителиоцитов. Следствием этого процесса является неспособность желудочных желез к полноценной функции [3].
К нарушениям клеточного обновления относят кишечную метаплазию и атрофию слизистой оболочки желудка. В настоящее время принято считать, что атрофия - это необратимая утрата желудочных желез с замещением метаплазированным эпителием или фиброзной тканью [61]. Однако в последние годы в научных кругах развернулась широкая дискуссия и многие ученые стали подвергать сомнению необратимость атрофии.
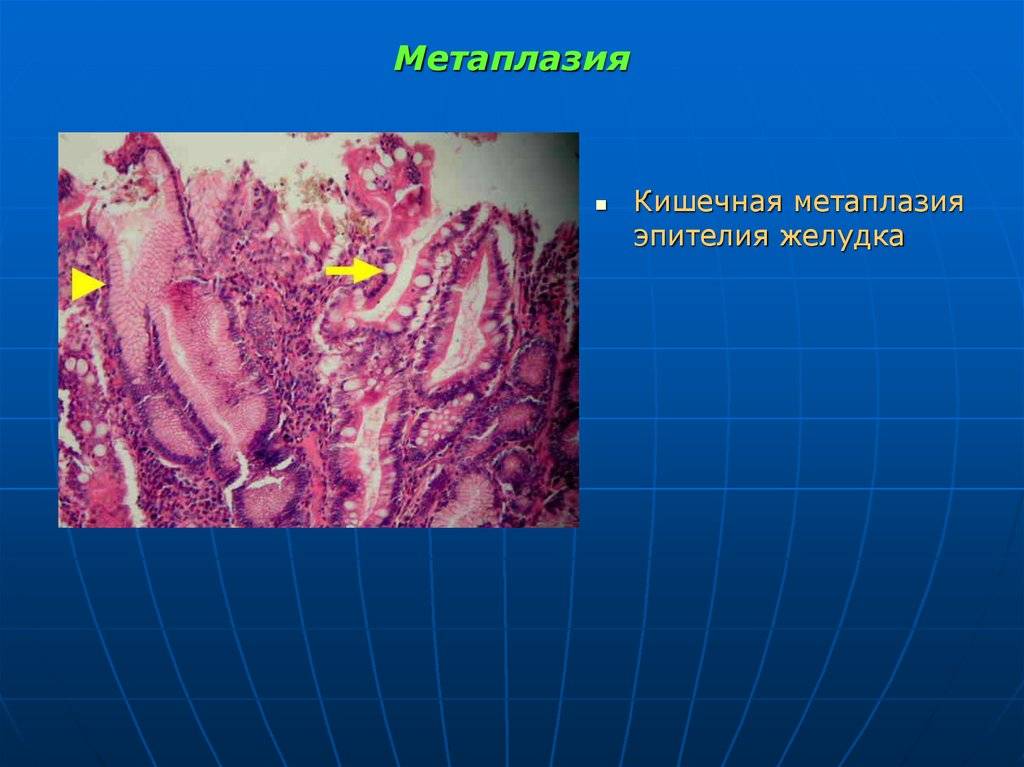
Под кишечной метаплазией в слизистой оболочке желудка принято понимать замещение желудочного эпителия кишечным [3,7]. Исходя из вышесказанного становится понятна взаимосвязь между атрофией и кишечной метаплазией в слизистой оболочке желудка. При этом кишечную метаплазию и атрофию желудочного эпителия можно рассматривать в качестве стадий эволюции хронического гастрита, поэтому представляется важным установление связи с наиболее частым возбудителем гастрита - Н. pylori.
Геликобактериоз является так называемой "медленной инфекцией", что обусловлено длительным, практически пожизненным, персистированием возбудителя в организме человека, его способностью взаимодействовать с иммунной системой и адаптироваться к ее изменениям. Несмотря на многообразие клинических форм геликобактериоза во всех случаях имеет место общий механизм - воспаление слизистой оболочки, развивающееся вслед за адгезией микроорганизма на желудочном эпителии. Морфологически такое воспаление характеризуется инфильтрацией собственной пластинки слизистой нейтрофильными лейкоцитами, лимфоцитами, макрофагами, плазматическими клетками, формированием лимфоидных фолликулов и повреждением эпителия различной степени выраженности.
Нейтрофильная инфильтрация эпителия и собственной пластинки слизистой оболочки индуцируется посредством реализации двух различных механизмов - непосредственно Н. pylori (за счет выделения растворимого белка, активирующего нейтрофилы) и опосредованно через экспрессию эпителиоцитами интерлейкина-8 (IL-8) с последующим запуском всего провоспалительного каскада. Белок, активирующий нейтрофилы, имеется у всех известных штаммов Н. pylori, что объясняет наличие нейтрофильной инфильтрации у 100% инфицированных. При этом вариабельность степени воспалительной инфильтрации, по всей видимости, вызвана различиями в степени адгезии и обсемененности Н. pylori, где на первый план может выступать iL-8-обусловленный механизм. Феномен хемотаксиса нейтрофилов после активации IL-8 цитокинового сигнального каскада более выражен у CagA-, VacA-позитивных штаммов, при этом выраженность воспалительной инфильтрации коррелирует со степенью обсеменения.
Одним из эффектов нейтрофильной инфильтрации является увеличение проницаемости эпителия для антигенов Н. pylori, вызывающих миграцию в собственную пластинку лимфоцитов, плазматических клеток и макрофагов. Важная особенность состоит в отсутствии эрадикации Н. pylori под воздействием антигеликобактерных антител, что, вероятно, объясняется "недоступностью" бактерии для антител в слое желудочной слизи, невозможностью выделения IgG в просвет желудка при относительном дефиците секреторных IgA, а также "антигенной мимикрией" Н. pylori. Таким образом, неэффективный гуморальный иммунный ответ на Н. pylori и его антигены вместо элиминации возбудителя становится одним из факторов патогенеза, формируя различные клинические варианты геликобактериоза. В результате прогрессирования воспаления закономерно возникают повреждения эпителия посредством индукции апоптоза или развития некрозов слизистой оболочки, опосредованных активными формами кислорода и оксидом азота нейтрофилов. Следует подчеркнуть, что для геликобактерного гастрита апоптоз является более характерной формой гибели клеток, чем некроз.
Хронический геликобактерный гастрит развивается более чем у 70% инфицированных Н. pylori уже в детском и подростковом возрасте; у взрослых инфицирование наступает значительно реже - около 2% в год [6]. Подтверждение трех постулатов Р. Коха, а также несомненная эффективность антигеликобактерной терапии у больных хроническим гастритом свидетельствует об этиологической роли данного микроорганизма в развитии большинства форм этого заболевания.
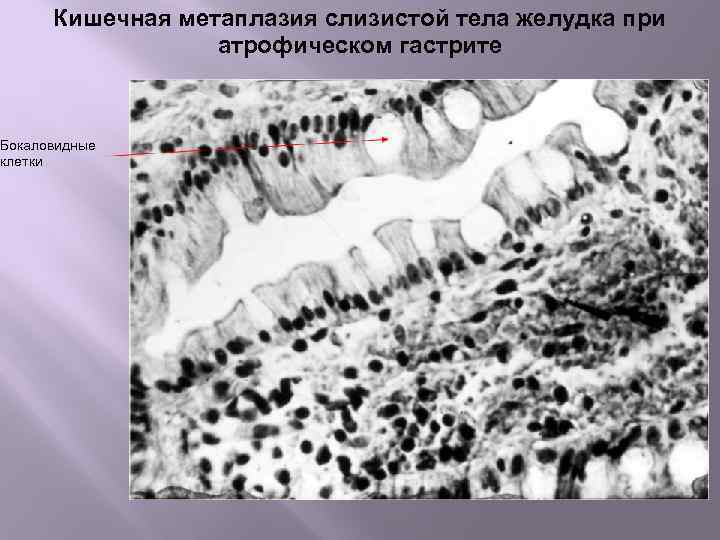
Н. pylori вызывает индукцию апоптоза клеток желудочного эпителия, что в последующем приводит к компенсаторному усилению пролиферативной активности в герминативных зонах слизистой оболочки [63]. Причем пролиферация стимулируется главным образом CagA-позитивными штаммами, а ее темпы коррелируют с выраженностью воспаления [48]. Это и объясняет высокую частоту нарушений клеточного обновления - атрофии и кишечной метаплазии при геликобактерном гастрите (рис. 2). По данным Л.И. Аруина и соавт. [3], ассоциация кишечной метаплазии и Н. pylori выявляется с частотой до 50%, атрофии Н. pylori - более чем в 80%, атрофии и кишечной метаплазии - до 100% случаев. Таким образом, в последние годы принято считать, что кишечная метаплазия - один из признаков геликобактерного гастрита. Этот тезис базируется на ряде фактов - при геликобактерном гастрите регистрируется высокая частота выявления кишечной метаплазии [32], установлена корреляционная взаимосвязь между степенью геликобактерного гастрита и выраженностью кишечной метаплазии [29], обратимость кишечной метаплазии возможна после успешной эрадикационной терапии [39].
При многих заболеваниях, характеризующихся хроническим воспалением (язвенный колит, болезнь Крона, хронический вирусный гепатит, хронический панкреатит и т. д.) существует высокий риск развития злокачественных новообразований. Наиболее вероятной причиной является клеточная пролиферация и/или повреждение генома, вызванное воспалением [49].
Как показал ряд исследований, такая взаимосвязь существует и в отношении рака желудка, развивающегося на фоне персистирующего хронического гастрита. Начиная с первого описания Н. pylori в слизистой оболочке желудка австралийскими учеными J. Warren и В. Marshall [59] значение данного открытия прогрессивно увеличивалось; в настоящее время эта инфекция признана в качестве главного этиопатогенетического фактора развития не только хронического гастрита и язвенной болезни, но и рака желудка.
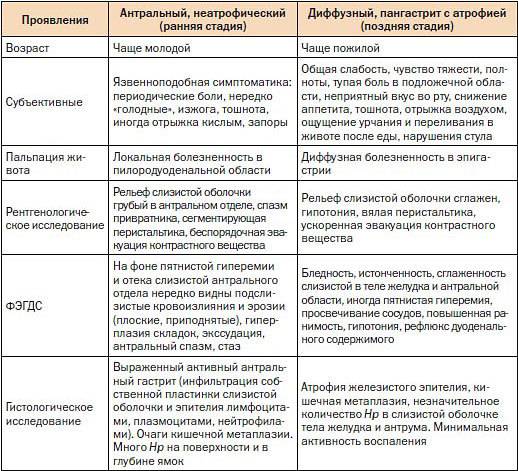
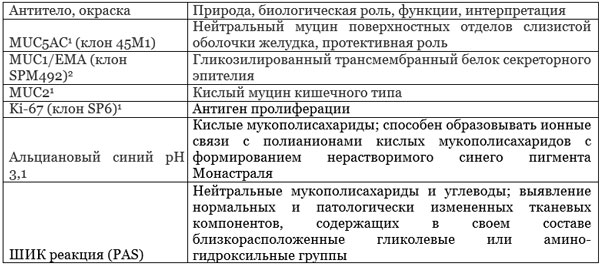
Так как в здоровой слизистой оболочке рак практически не возникает [8], в последние годы сформировалось представление о предраковой патологии желудка [4], в спектре которой Н. pylori-ассоциированный хронический гастрит занимает центральное место (табл. 1).
Взаимосвязь хронического гастрита и рака желудка была доказана рядом научных исследований как за рубежом, так и в России в 50-70-х годах прошлого века, т.е. до открытия Н. pylori. Еще в тот период было отмечено, что необходимыми условиями для возникновения рака являются нарушения клеточного обновления - кишечная метаплазия и атрофия слизистой оболочки, создающие предпосылки для дисплазии эпителия - практически облигатного предракового состояния [10]. Таким образом, Н. pylori, хронический гастрит, кишечная метаплазия, атрофия и рак желудка - звенья одной цепи, в которой инициирующую роль играет микроорганизм; в ответ на инвазию у человека развивается хронический воспалительный процесс в слизистой оболочке, сопровождающийся дисрегенеторными изменениями эпителия, создающими, в свою очередь, фон для развития рака желудка кишечного типа.
Данный каскад патологических явлений в качестве модели развития рака желудка предложил в 1988 г. Р. Соrrеа [21], однако в то время в этой модели не нашлось места для H. pylori. Только двумя годами позже автор ввел H. pylori а качестве этиологической причины гастрита [23,25] и соответственно рака желудка. Указанная последовательность патологических явлений в последние годы стала широко известна и получила название парадигмы желудочного канцерогенеза (рис. 3). Молекулярных изменений, которые возникают при инфекции H. pylori и способны привести к развитию рака желудка, не установлено. Действительно, сведений, достоверно подтверждающих синтез или секрецию Н. pylori мутагенных или канцерогенных субстанций нет. Имеются отдельные экспериментальные исследования, показывающие способность Н. pylori стимулировать in vitro рост культуры, опухолевых клеток [17], не имеющих к раку желудка никакого отношения. Поэтому современные представления состоят в том, что Н. pylori скорее действует в качестве промотора, чем инициатора желудочного канцерогенеза. При инфицировании Н. pylori возникает воспалительная реакция в слизистой оболочке желудка, наблюдается продукция нейтрофильными лейкоцитами реактивных кислородных метаболитов и происходит высвобождение цитокинов клетками воспалительного инфильтрата, что приводит к повреждению ДНК и стимуляции рецепторов, вызывающих пролиферацию клеток.
Развитие дистального рака желудка по времени может занять несколько десятилетий, в течение которых у большинства пациентов последовательно сменят друг друга указанные нами стадии желудочного канцерогенеза, включающие заражение Н. pylori, развитие хронического активного гастрита, возникновение атрофии слизистой и кишечной метаплазии, дисплазии эпителия с последующей трансформацией в рак [21,35,50].
Риск развития рака значительно повышается при сочетании предраковых состояний с предраковыми изменениями слизистой оболочки - в 26 и 132 раза при умеренной и тяжелой дисплазии желудочного эпителия соответственно [8].
Однако приведенные выше факты не отвечают на ряд важнейших вопросов: почему Н. pylori вызывает и другие заболевания (язвенную болезнь двенадцатиперстной кишки, MALT-лимфому), крайне редко сочетающиеся с раком желудка [12-14,19,28,46,57], почему только у небольшого числа больных (1-2%) с H. pilory-ассоциированным гастритом развивается дистальный рак желудка [1,2], а также почему кишечная метаплазия (дифференцированный эпителий, не способный к делению) является фоном для возникновения рака желудка.
Динамическое наблюдение за больными, инфицированными Н. pylori, позволило выделить две формы хронического гастрита - хронический поверхностный и хронический атрофический, являющиеся, по сути, последовательными этапами развития хронического геликобактерного гастрита. С другой стороны, большинством специалистов, занимающихся вопросами геликобактерноза, выделяются два фенотипа геликобактерного гастрита - классический антральный и фундальный (мультифокальный). Именно топографические особенности гастрита, а не выраженность воспаления определяют клинические последствия инфицирования Н. pylori [2]. Установлено, например, что у 1% больных антральным хроническим гастритом ежегодно возникают дуоденальные язвы, но у них не развивается рак желудка; при фундальном и мультифокальном гастритах у 1% пациентов ежегодно развивается рак желудка и практически не встречаются дуоденальные язвы ("язвенный" и "раковый" фенотипы хронического гастрита по P. Sipponen). Возможное объяснение этому кроется в том, что фенотип Н. pylori-accoцииpoванного гастрита влияет на секрецию соляной кислоты. Если ее уровень низкий, Н. pylori может колонизировать любой отдел желудка, при сохранной (повышенной) кислотности единственным местом, где может выжить микроорганизм, является антральный отдел, для которого характерны более высокие значения рН. В этом случае ведущую роль в развитии конкретного фенотипа будет играть возраст, в котором произошло заражение, поскольку для детей более характерно состояние гипоацидности, а для взрослых - нормацидности [12].
Вместе с тем антральный H
Кишечная метаплазия — 55 ответов врачей о лечении и опасности на...
Обзор современных концепций кишечной метаплазии желудка и рака желудка
Типы кишечной метаплазии и риск развития рака желудка
Помогите Пожалуйста, метаплазия Желудка , Очаговая толстокишечная метаплазия
Участки кишечной метаплазии - Гастроэнтерология - Здоровье Mail.ru
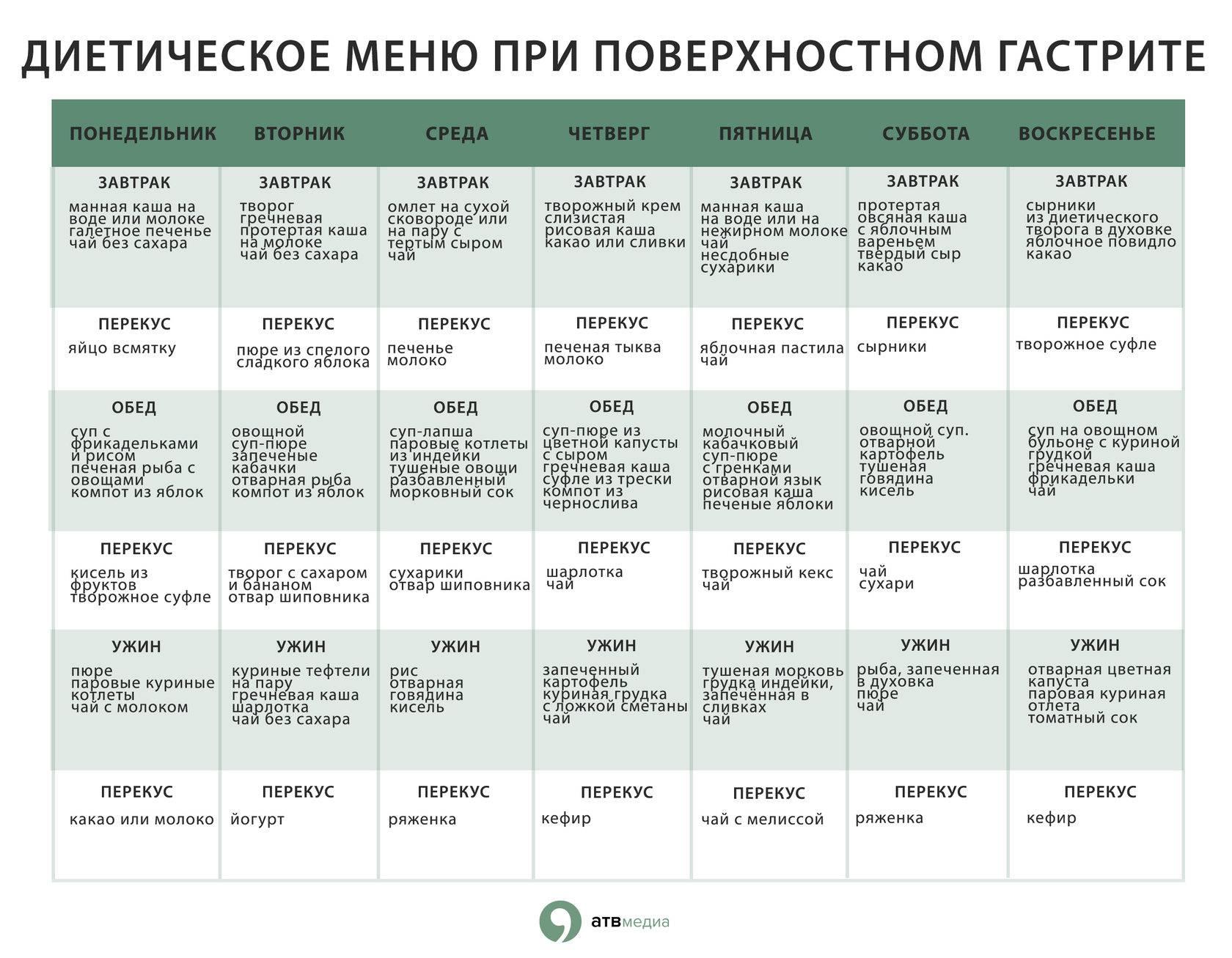
Лечебная Диета Номер
Лечение И Диета При Колите Кишечника
Диета При Гепатозе Беременных
Диета При Кишечной Метаплазии Желудка