Циклоалканы. Строение, свойства, получение
Органика с нуля | Stepenin.ruВ этой статье собраны все теоретические посты, опубликованные в период изучения циклоалканов на курсе 10 класса по органике в телеграм-канале "Органика с нуля". Если читать вайба нет, то держите запись вебинара 2025 года, в котором обсуждается все то, что написано ниже, но сильно подробнее и с разбором заданий:
— Все про циклоалканы за 1 урок
Качайте конспект PDF "Все про циклоалканы", нажав на его название. Подходит для печати и быстрого повторения. Рассказал обо всем, стартуем!
Строение и номенклатура циклоалканов
Циклоалканы — циклические углеводороды (алициклические углеводороды), содержащие только одинарные С-С связи. Все атомы углерода находятся в sp³-гибридизации.
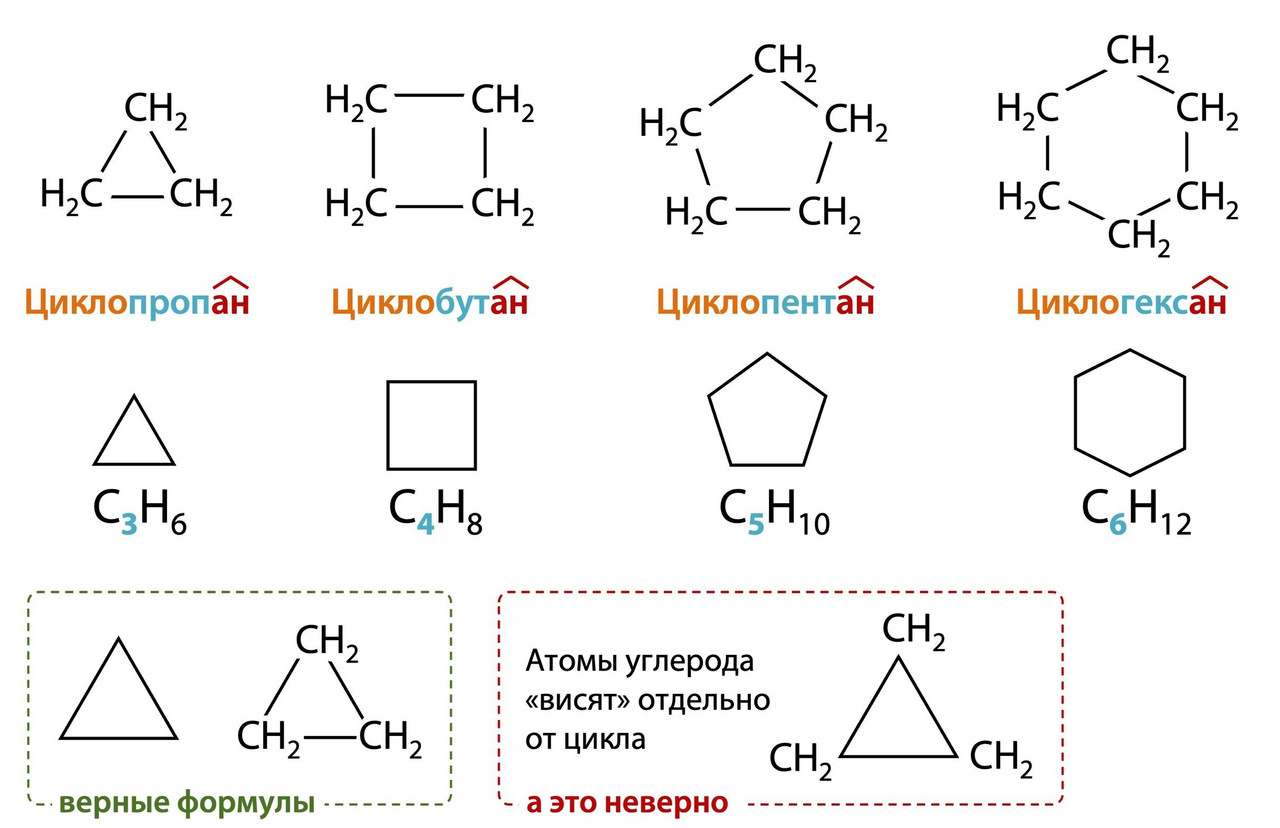
В циклопропане атомы углерода находятся в одной плоскости, т.к. через 3 точки можно провести одну плоскость. Более крупные циклоалканы "изогнуты" в пространстве, а значит ни углероды, ни водороды не находятся в одной плоскости:
Бесплатные тесты, видео и конспекты по органике для 10 класса и ЕГЭ: stepenin.ru/courses/organic10
🤔 Нужна ли химикам геометрия? Спойлер — да.
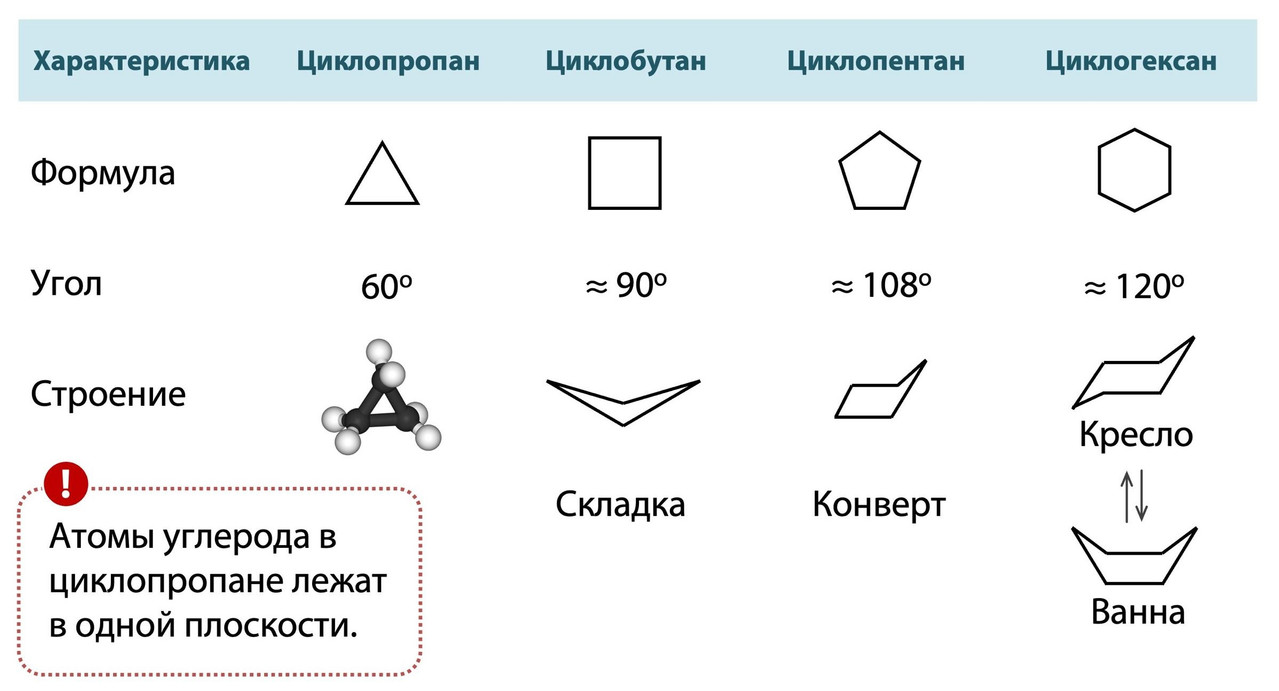
Каждый углерод в составе циклоалканов находится в sp³-гибридизации, а значит угол между любыми двумя его связями должен быть равен 109°28’. Но у циклопропана угол как в равностороннем треугольнике - 60°, а у циклобутана - примерно 90°. Такое сильное отклонение углов от тетраэдрического вызывает напряжение в цикле и делает эти молекулы менее устойчивыми по сравнению с более крупными циклоалканами. Поэтому для этих двух малышей будут характерны реакции с разрывом/раскрытием цикла. Им просто хочется снять напряжение!
Простая аналогия. Представьте, что вас на уроке физкультуры заставили сделать складку (сесть на пол и руками достать до пальцев ног). Если у вас нет хорошей растяжки, то вы будете «напряжены» и у вас будет большое желание «раскрыться». Циклы в циклопропане и циклобутане хотят сделать то же самое: раскрыться, чтобы увеличить свой угол с 60° и 90° до 109°28.
И, кстати, из-за «желания связей увеличить угол» будет происходить их выгибание наружу цикла. Такие выгнутые связи назвали «банановыми», уж очень сходится форма!
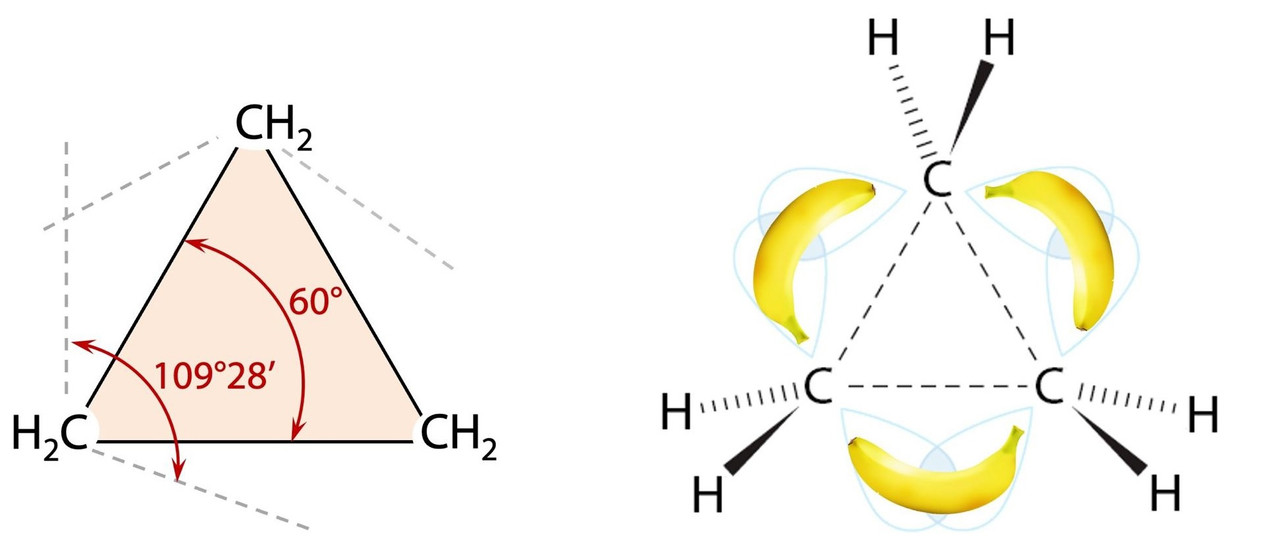
Подробнее про номенклатуру циклоалканов разветвленного строения читайте в этой главе электронного учебника по органике для 10 класса: stepenin.ru/tasks/ebook-10/test2263
Химические свойства циклоалканов
Гидрирование циклопропана и циклобутана протекает с разрывом «напряженного» цикла и образованием алканов. Вы помните, что угол в циклопропане сильнее отличается от тетраэдрического, чем угол в циклобутане? Это приводит к тому, что на одном и том же катализаторе (Ni) циклопропан гидрируется при 80°, а циклобутан только при 200°.
Таким образом, «легкость» реакции с водородом можно оценить так, возвращаясь еще и к предыдущему изученному классу алкенов:
пропен > циклопропан > циклобутан
Интересно, что циклопентан тоже можно гидрировать с разрывом цикла и образованием н-пентана. Но это происходит при еще более жестких условиях (>300°, Ni), чем у циклобутана.
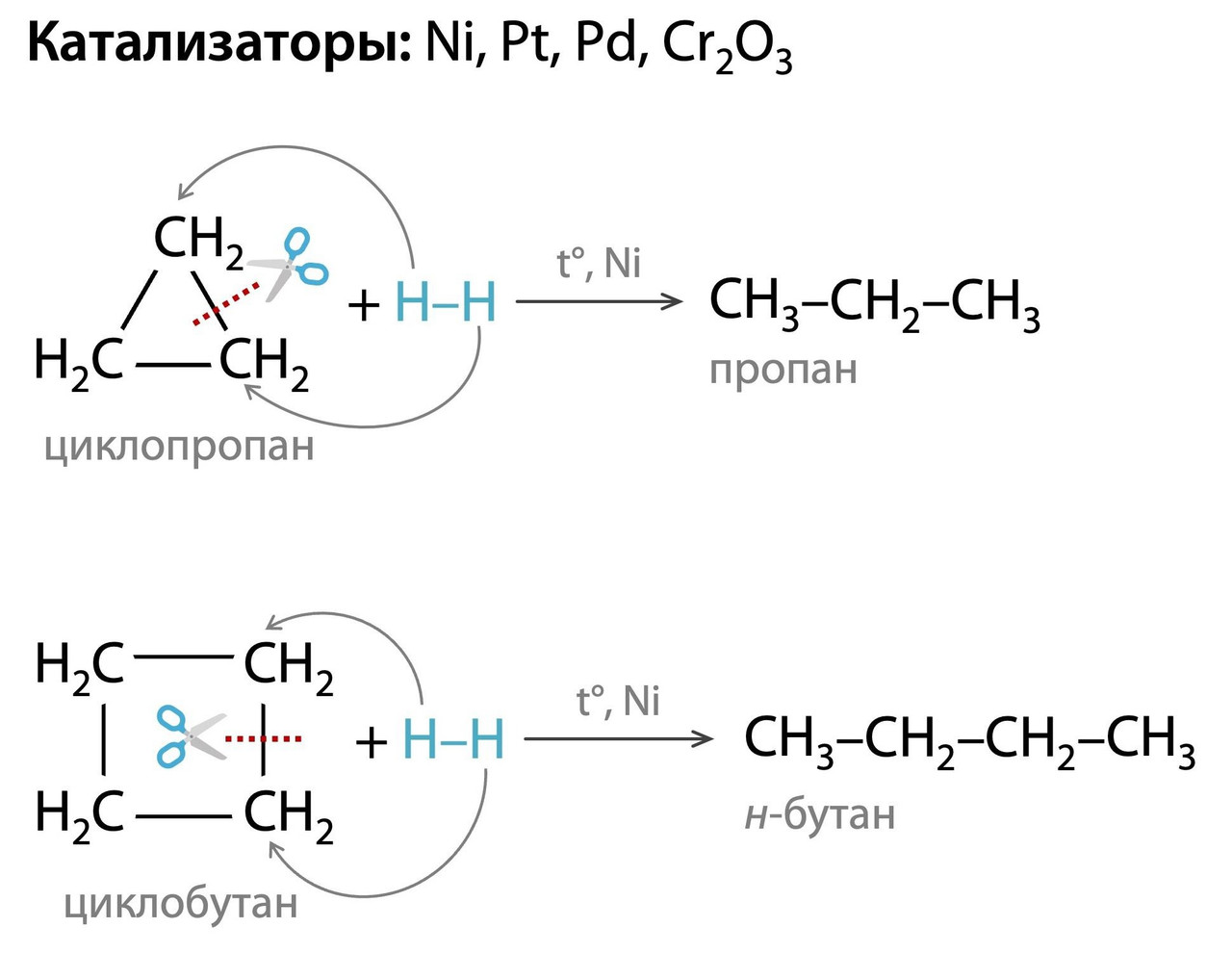
Вступать в реакцию галогенирования (+ Cl₂/Br₂) с разрывом цикла может только циклопропан. Циклобутан галогенами не раскрывается, но иногда в тестах встречается такая «бумажная реакция». Чтобы понять, почему в такой реакции галогены оказываются не при соседних атомах углерода как в случае алкенов, посмотрите как происходит присоединение. И, да, иногда в тесте можно встретить, что циклопропан реагирует с бромной водой и обесцвечивает ее, не пугайтесь!
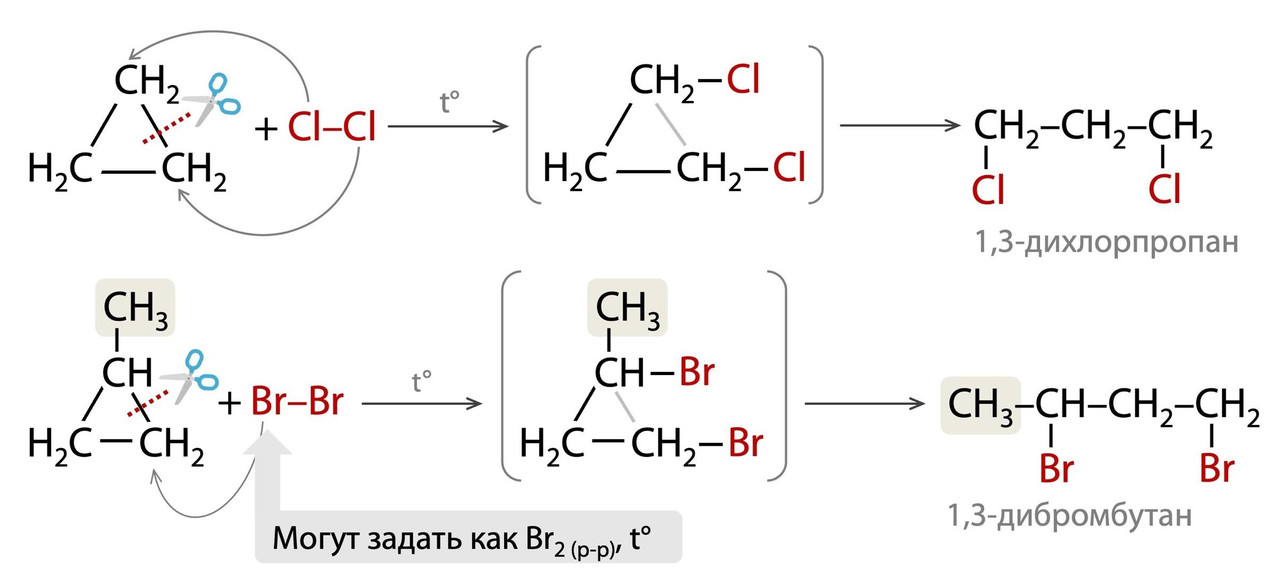
Присоединению галогеноводородов (+ HCl/HBr) с разрывом цикла также подвергается только циклопропан. Но в тестах вы все еще можете встретить «бумажную реакцию» с циклобутаном! Заметьте, что при разрыве кольца циклопропана без заместителей галоген в такой реакции оказывается на конце цепи:
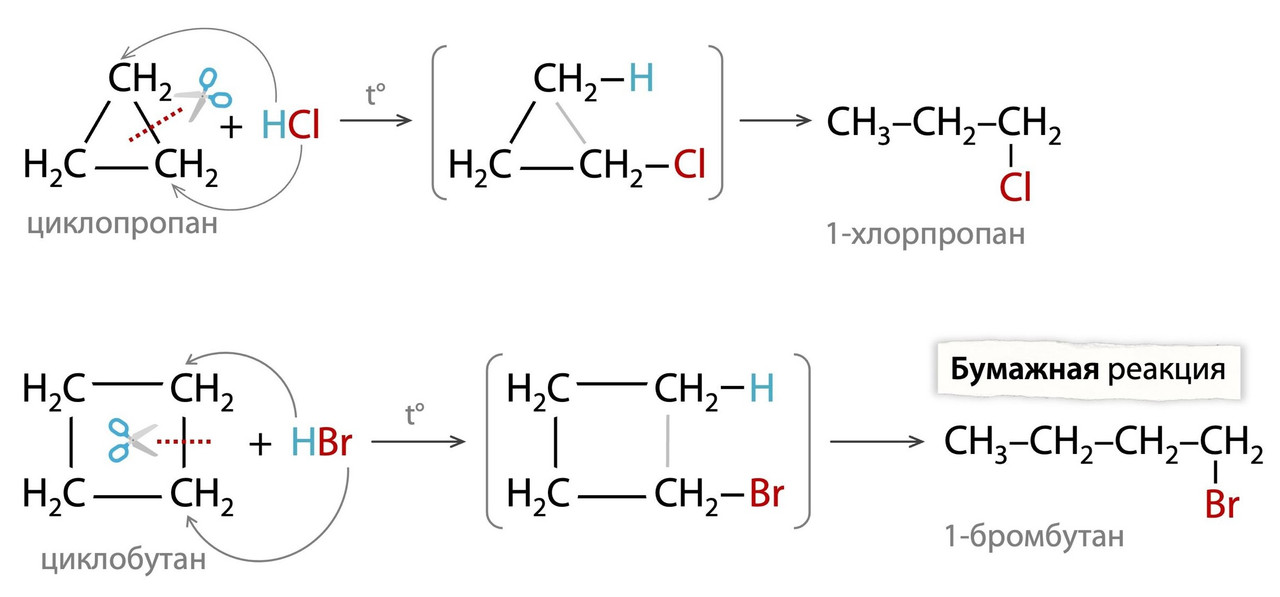
А если заместитель есть, то при вторичном атоме углерода. Все из-за того, что для удобства мы будем пользоваться и в таком присоединении "правилом Марковникова" и разрывать связь в кольце между углеродом с заместителем и его соседом:
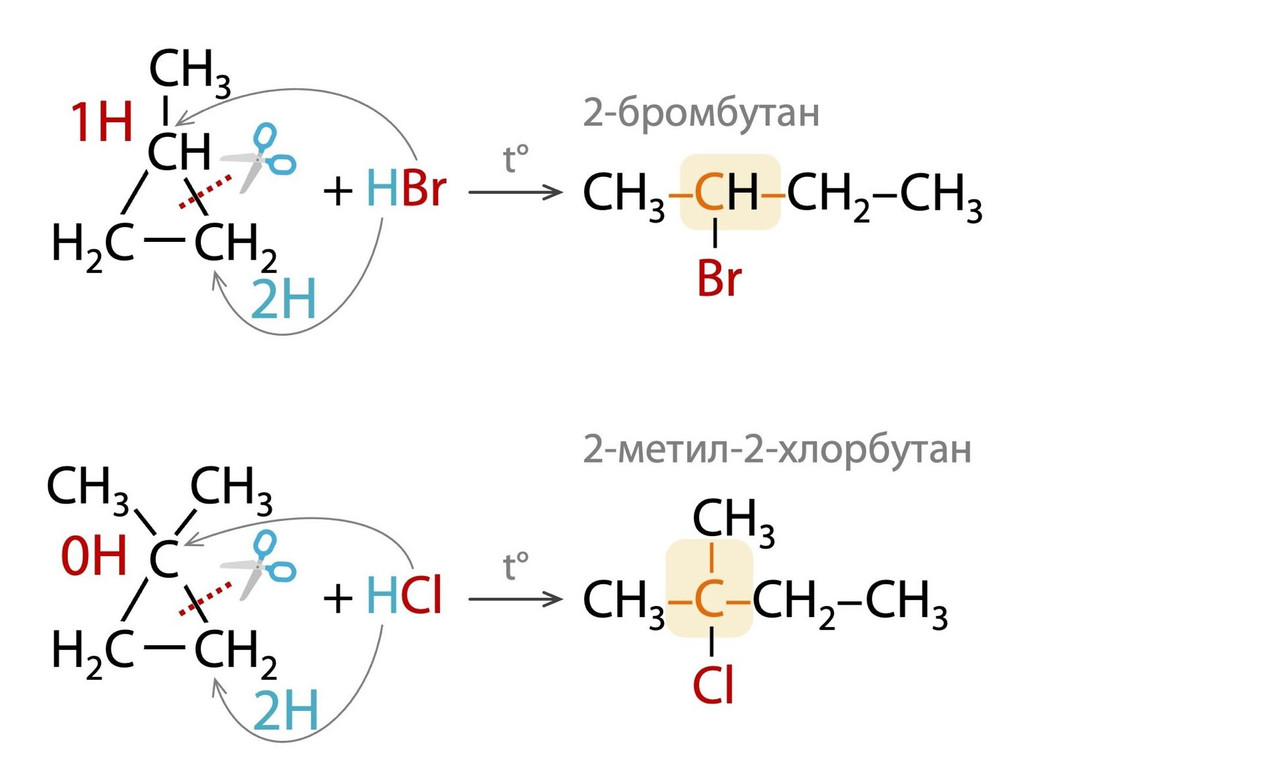
Кстати, В.В. Марковников же и выделил в 19 веке циклоалканы из нефти. Но он их тогда назвал нефтены (от греч. naphtha — нефть).
Циклопентан и циклогексан достаточно устойчивы к разрыву цикла и для них будут характерны реакции замещения как и для алканов.
Почему устойчивы? Угол между связями их цикла очень близок к тетраэдрическому, «напряженность» отсутствует и это позволяет им «не раскрываться».
Две реакции, которые вам нужно знать:
1. галогенирование Cl₂/Br₂ (не водными растворыми, а чистыми галогенами) с замещением водорода на атом галогена
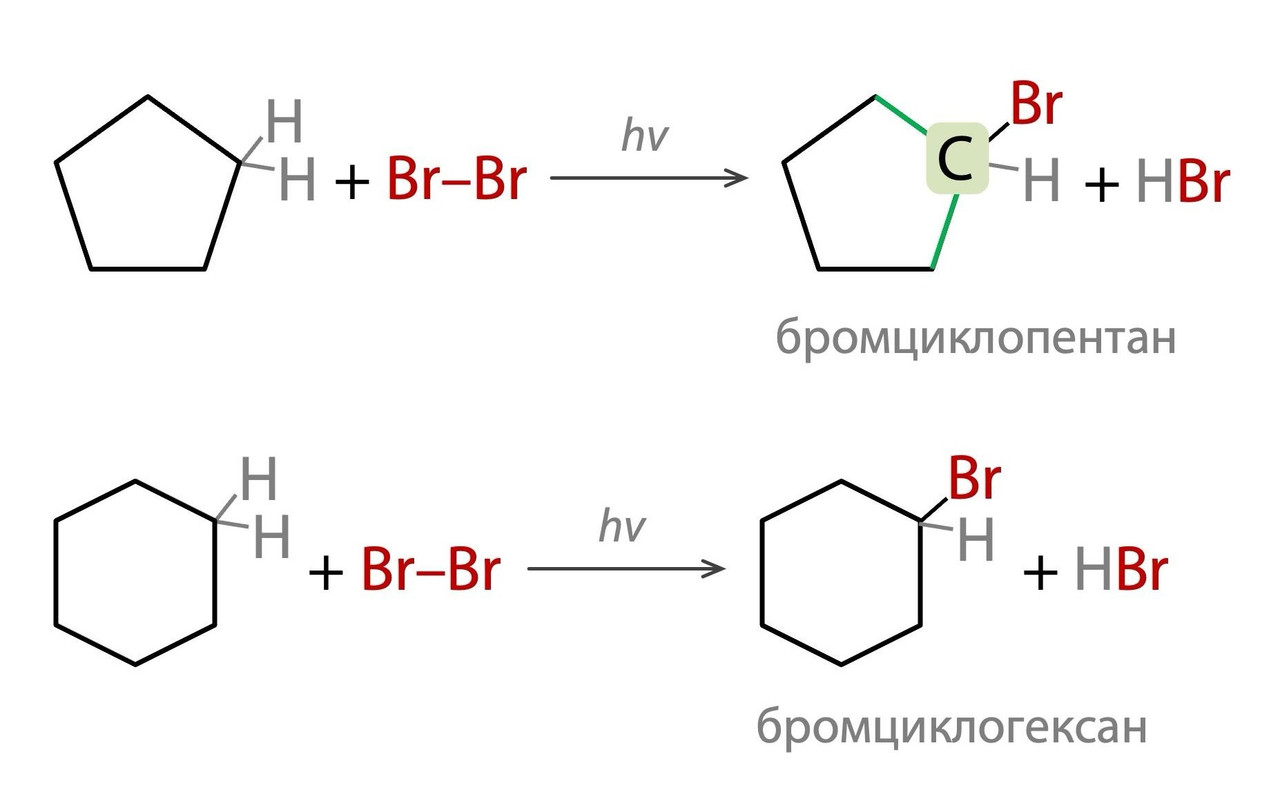
2. нитрование HNO₃ с аналогичным замещением водорода, но уже на нитрогруппу -NO₂
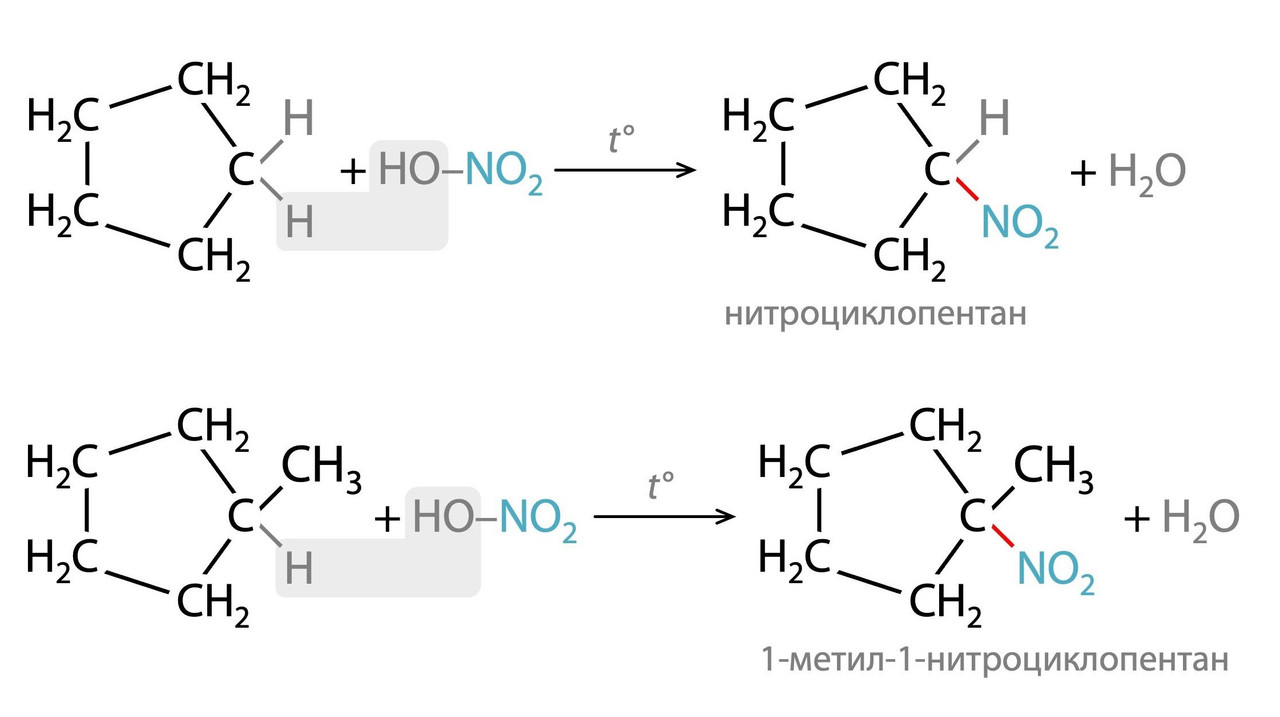
Напомню правило, что водород будет замещаться при разных атомах углерода в разной очередности. Порядок легкости замещения оцениваем по следующему ряду:
третичный С > вторичный С > первичный С
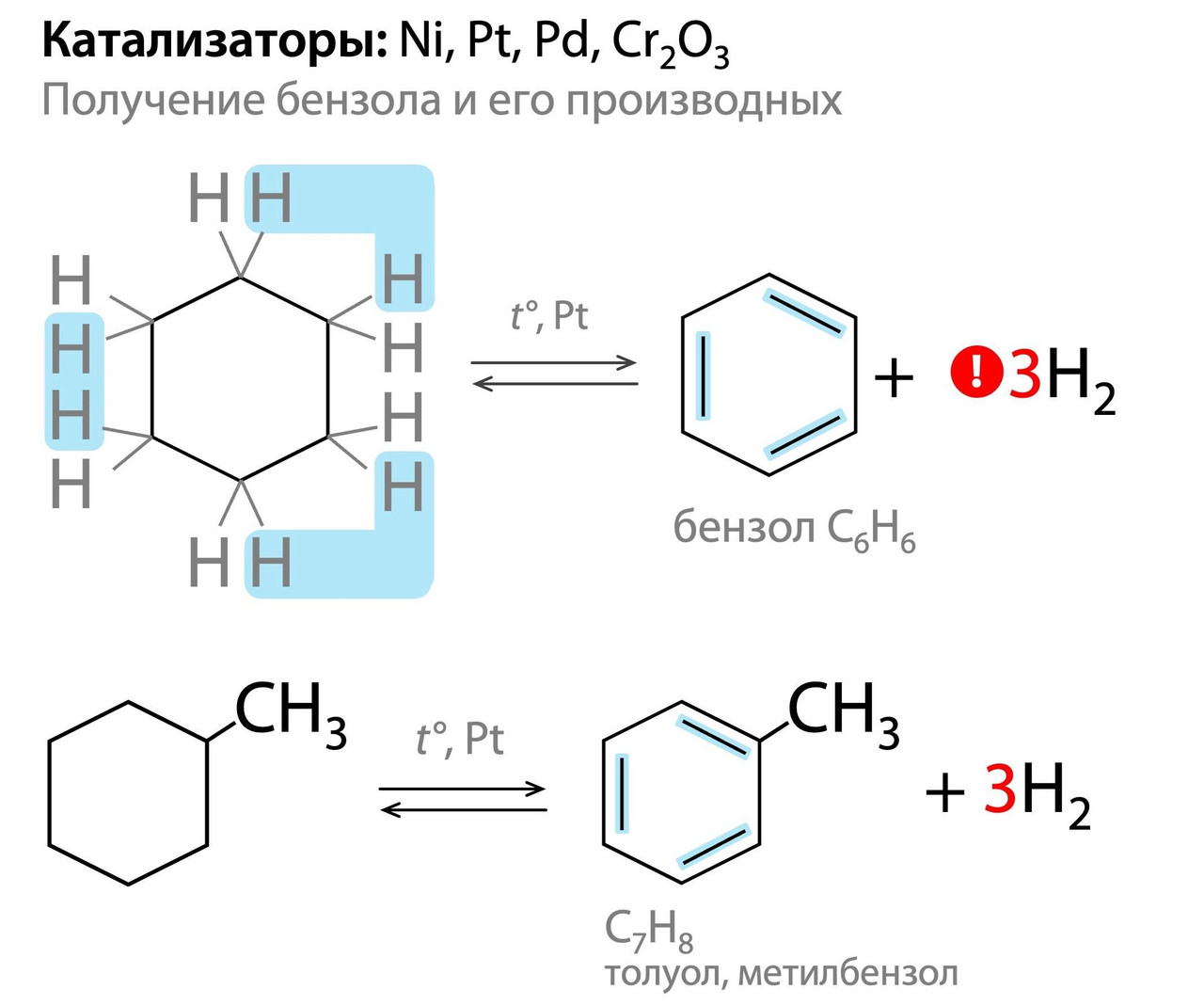
Посмотрим на дегидрирование (отщепление водорода). Циклогексан и его производные, например, метилциклогексан, при нагревании в пристутсвии катализаторов Ni, Pt, Pd, Cr₂O₃ подвергаются отщеплению трех молекул водорода и образованию трех двойных связей в цикле.
Почему так? Образующееся кольцо называется «бензольным», оно обладает аномальной утойчивостью, а молекулы стараются стремиться к тому, что ее повышать в ходе реакции. Это переход от циклоалканов к классу ароматических углеводородов, о которых мы еще будем говорить в следующих статьях.
Какие НЕТ мы дружно говорим циклоалканам? Список реагентов, с которыми они либо не реагируют, либо про которые просто не будут спрашивать на ЕГЭ.
Циклопропан с:
— H₂O
— KMnO₄
— HNO₃
Циклобутан с:
— H₂O
— KMnO₄
— HNO₃
Циклопентан с:
— H₂O
— KMnO₄
— Br₂ (водн. р-р)
— HCl, HBr
Циклогексан с:
— H₂O
— KMnO₄
— Br₂ (водн. р-р)
— HCl, HBr
— Н₂
Способы получения циклоалканов
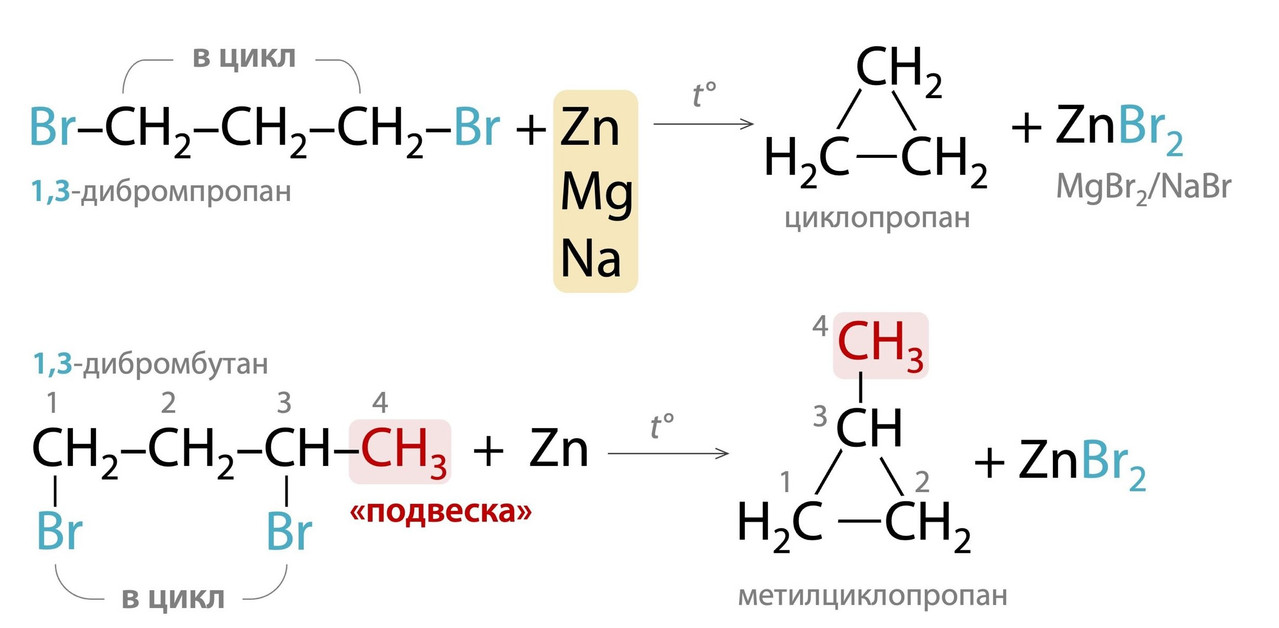
Дегалогенирование с помощью Zn/Mg и реже Na. Если атомы галогена в дигалогеналкане находятся не при соседних атомах углерода, а на расстоянии друг от друга, то при их отщеплении образуется связь между этими атомами углерода и цепь замыкается в цикл. Таким способом можно получить даже циклоалканы с одним или несколькими заместителями.
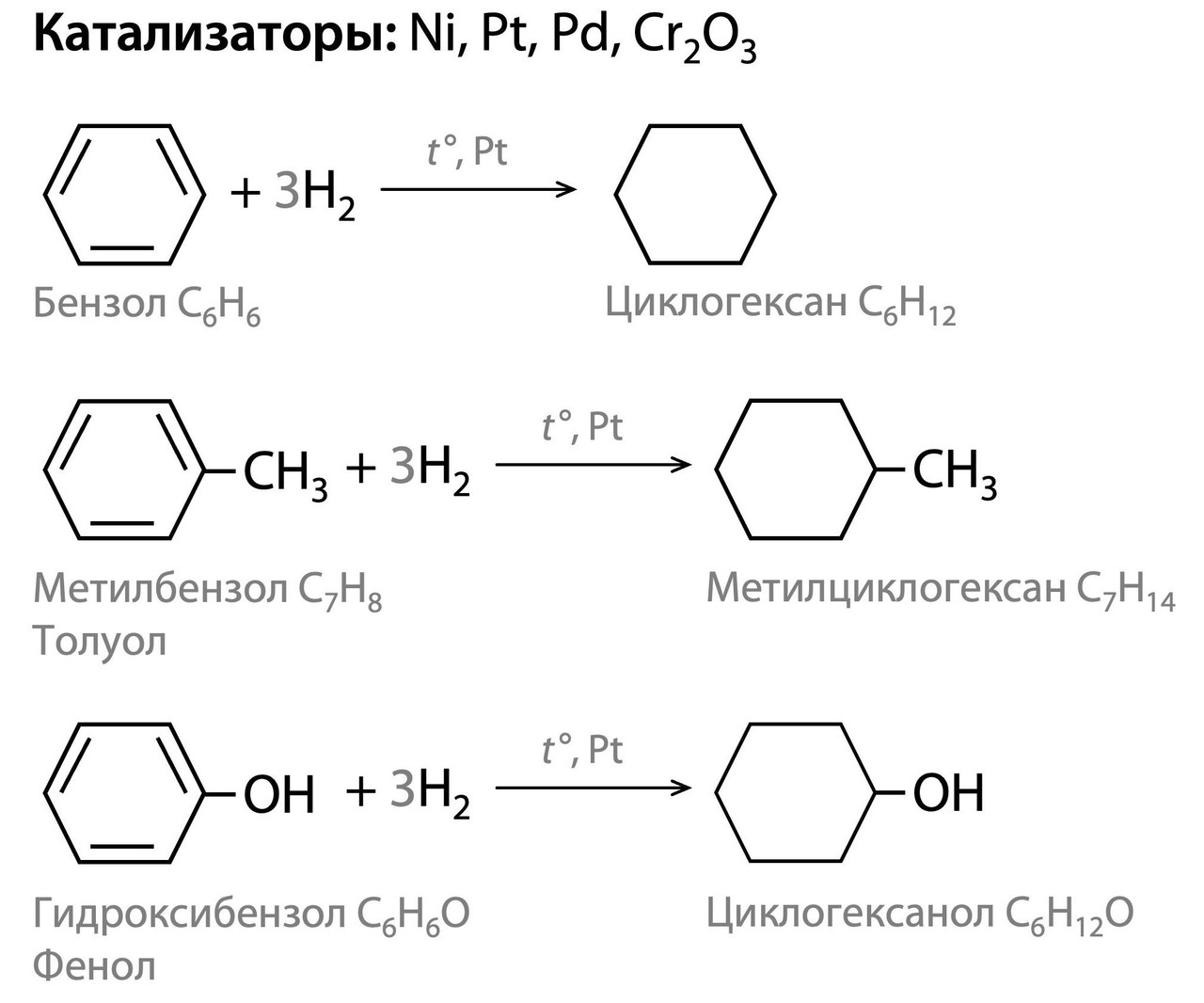
Гидрирование бензольного кольца на катализаторах Ni, Pt, Pd или Cr₂O₃. К бензольному кольцу ароматических углеводородов можно присоединить три молекулы водорода с разрывом трех π-связей. Так можно получить циклогексан из бензола или производные циклогексана из производных бензола. К сожалению (или счастью, что учить меньше), тут не такое разнообразие получаемых циклоалканов, как в предыдущем способе с дегалоганированием.
Что порешать?
На нашем сайте есть бесплатные тесты, которые помогут усвоить материал по теме "Циклоалканы". Прямые ссылки на них:
- 103 тестовых задания по строению, изомерии, номенклатуре, свойствам и получению циклоалканов: https://stepenin.ru/lesson/563
- 10 цепочек формата №32 ЕГЭ с участием циклоалканов и алкадиенов (с подробным видеоразбором каждого решения): https://stepenin.ru/lesson/988
🏆 На странице платного курса для 10 класса по органике намного больше заданий к этой теме в самом первом модуле. Прямая ссылка на тему "Циклоалканы": https://stepenin.ru/chapter/356
Понравилось такое обобщение изученного материала? Поделись статьей с друзьями, которые учат органику. Учим химию вместе! 🫶🏼