Алкадиены. Строение, свойства, получение
Органика с нуля | Stepenin.ruВ этой статье собраны все теоретические посты, опубликованные в период изучения алкадиенов на курсе 10 класса по органике в телеграм-канале "Органика с нуля". Если читать вайба нет, то держите запись вебинара 2025 года, в котором обсуждается все то, что написано ниже, но сильно подробнее и с разбором заданий:
Качайте конспект PDF "Все про алкадиены", нажав на его название. Подходит для печати и быстрого повторения. Рассказал обо всем, стартуем!
Строение и номенклатура алкадиенов
Алкадиены — непредельные углеводороды, содержащие две двойные связи. Атомы углерода при кратных связях находятся в sp²-гибридизации. Гомологический ряд алкадиенов нормального строения и их соответствующие систематические названия:
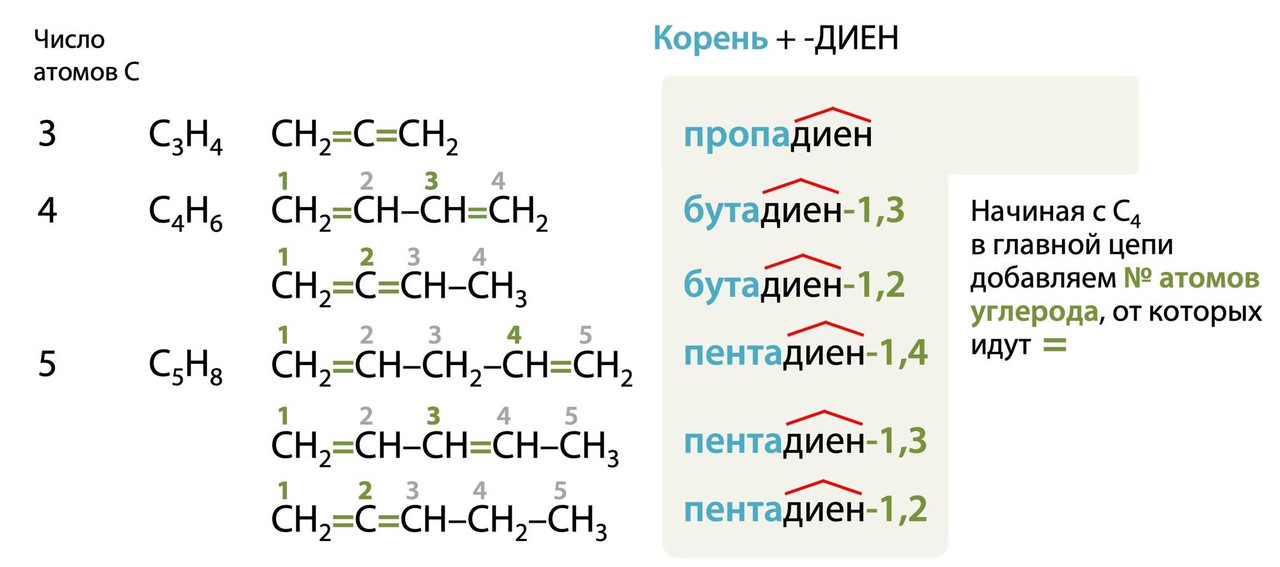
Подробнее про номенклатуру алкадиенов разветвленного строения читайте в этой главе электронного учебника по органике для 10 класса: stepenin.ru/tasks/ebook-10/test2256
Бесплатные тесты, видео и конспекты по органике для 10 класса и ЕГЭ: stepenin.ru/courses/organic10
Исходя из длины углеродного скелета и положения кратных связей, алкадиены можно разделить на три группы:
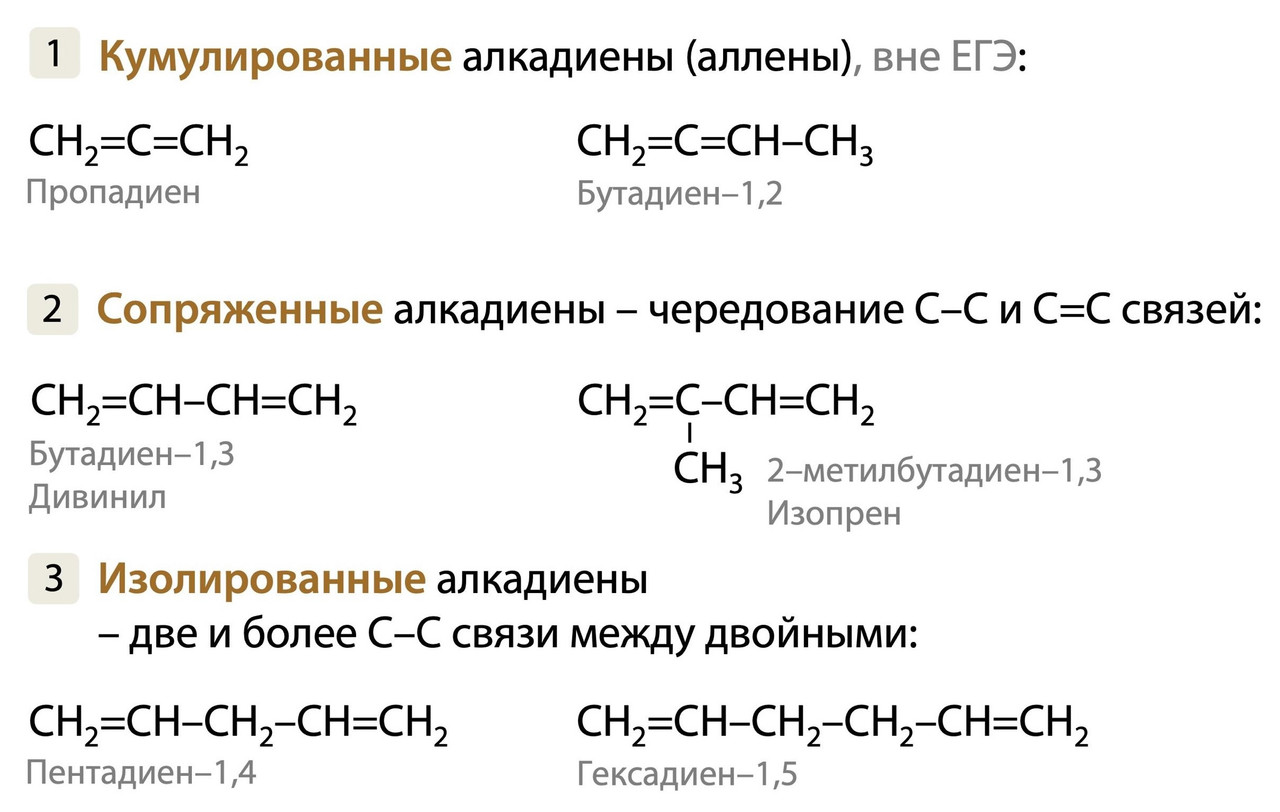
1. Если две двойные связи находятся при одном атоме углерода, то это кумулированные алкадиены (аллены). На экзамене они могут попасться только в заданиях на классификацию. Если видите пропадиен, то дружно отвечайте, что это углеводород/алкадиен! Все!
2. Если двойные связи чередуются с одинарными, то это сопряженные алкадиены
3. Если двойные связи разделены двумя и более одинарными связями между углеродами, то это изолированные алкадиены
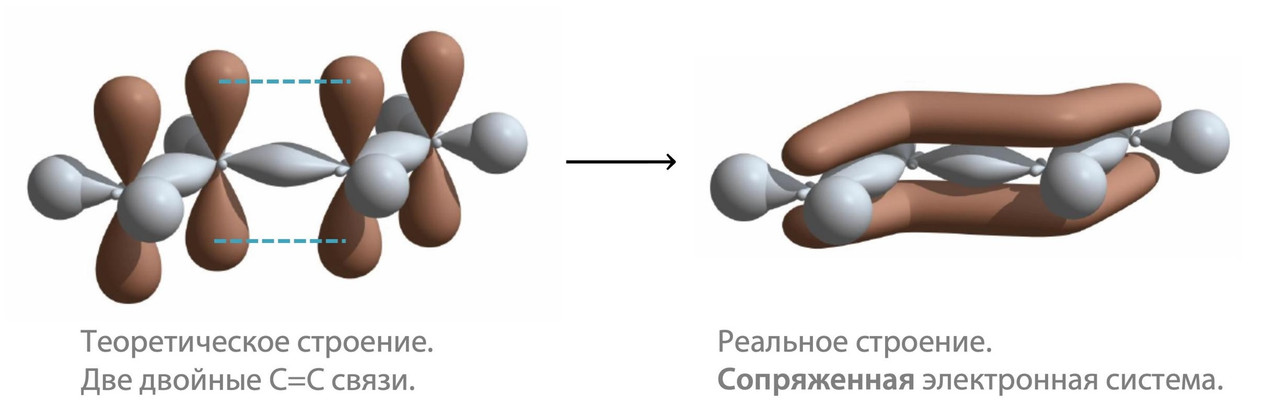
В чем прикол сопряженных алкадиенов? Чередование двойных С=С и одинарных С-С связей приводит к объединению электронной плотности π-связей. И это влияет на длину углерод-углеродных связей (условно говоря, происходит их «выравнивание»):
— одинарная связь С-С в алкадиене укорачивается примерно на 5%
— двойная связь немного удлиняется
Все перечисленное влияет на стабильность молекул алкадиенов. И когда в реакциях отщепления будет возможно получение сопряженной системы, то она будет преимущественно образовываться.
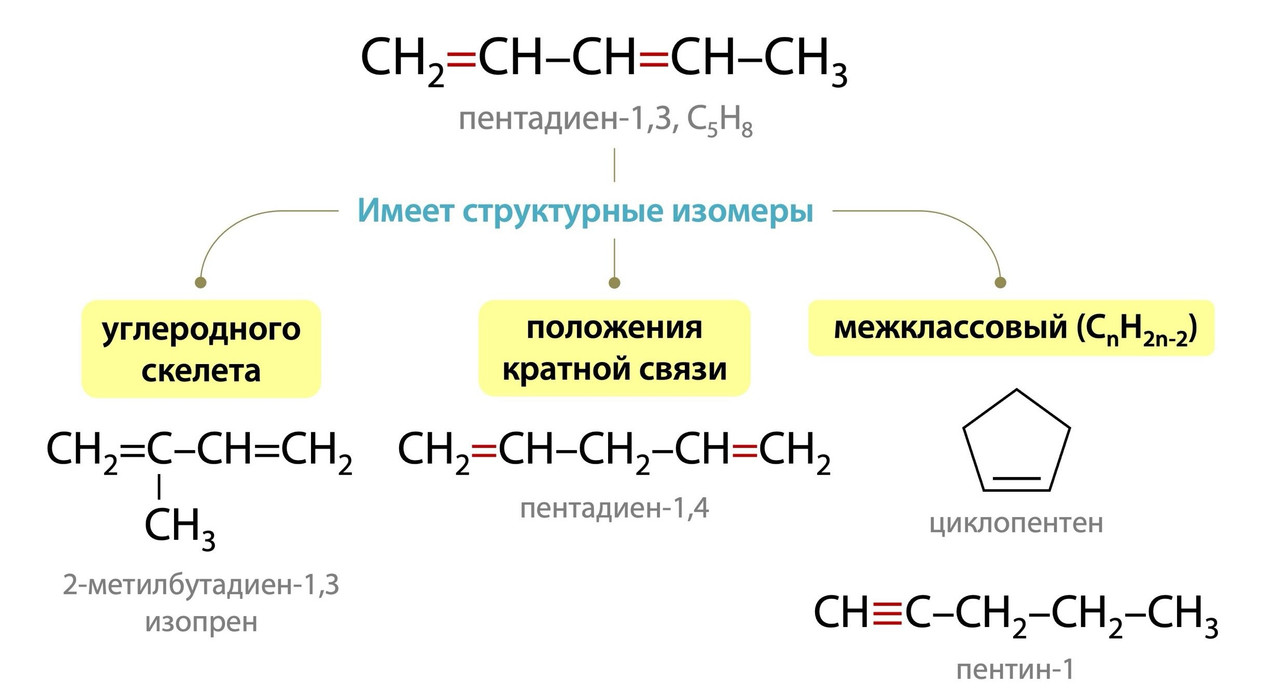
У алкадиенов есть нестандартные структурные изомеры, о которых нужно помнить при решении заданий №11 ЕГЭ! Если с изомерией углеродного скелета и положения кратной связи проблем обычно не возникает, то при поиске межклассовых изомеров иногда можно войти в ступор.
Как понять, что два вещества являются межклассовыми изомерами?
1. Изобразить их структурные формулы и посчитать молекулярные
2. Определить, что вещества относятся к разным классам органических веществ
3. Если молекулярные формулы при этом совпали, то вещества — межклассовые изомеры
Напомню, что у тех классов веществ, предаствители которых при одинаковом числе атомов углерода могут быть структурными изомерами, общая формула совпадает!
Химические свойства алкадиенов
В первую очередь для ЕГЭ по химии необходимо знать свойства сопряженных алкадиенов на примере бутадиена-1,3 (дивинила) и 2-метилбутадиена-1,3 (изопрена). Их самая важная особенность — два вида реакций присоединения!
1. либо к соседним атомам углерода, как в случае обычных алкенов с разрывом π-связи — это 1,2-присоединение
2. либо к двум концам сопряженной системы, включающей четыре атома углерода — это 1,4-присоединение
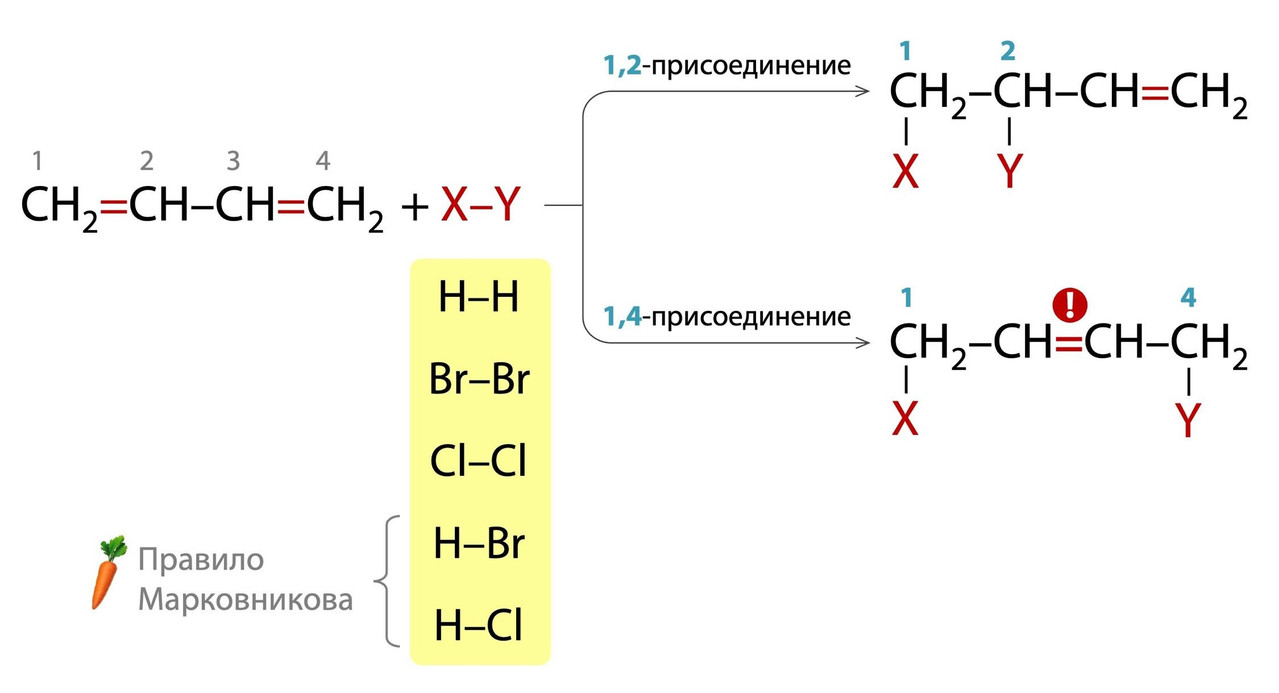
Заметьте, что во втором случае оставшаяся π-связь «мигрирует» ко 2 атому углерода. Не ошибайтесь в записи формулы продукта!
Интересно, что в таких реакциях всегда образуется смесь продуктов 1,2- и 1,4-присоединения. Но при повышенной температуре в смеси будет больше 1,4-продукта, а при охлаждении — больше 1,2-продукта. Именно по температуре мы понимаем преимущественный продукт и его записываем на экзамене в бланк!
Помимо сопряженных алкадиенов на ЕГЭ будут встречаться свойства изолированных алкадиенов. Они ведут себя в реакциях как обычные алкены, т.к. двойные С=С связи находятся далеко друг от друга в молекуле и не оказывают взаимного влияния. Например, реакция гексадиена-1,5 с избытком бромной воды приводит к образованию тетрагалогеналкана, типичное присоединение по двойным связям:
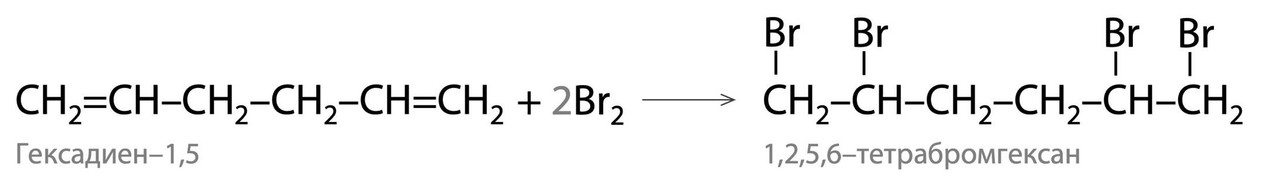
Гидрирование сопряженных алкадиенов (+ Н2):
1. Если водород в избытке и используются катализаторы Pt, Pd, Ni или Cr₂O₃, то образуются алканы, т.к. в этих условиях у π-связей «выжить» не получится.
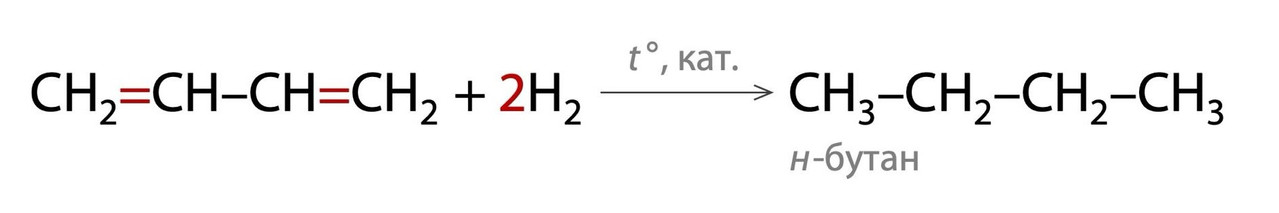
2. Если «водород в недостатке» или используются специфические катализаторы/ реагенты, то в результате реакции образуются алкены (одна π-связь «выживает»):
— бутен-1 в случае 1,2-присоединения
— бутен-2 в случае 1,4-присоединения
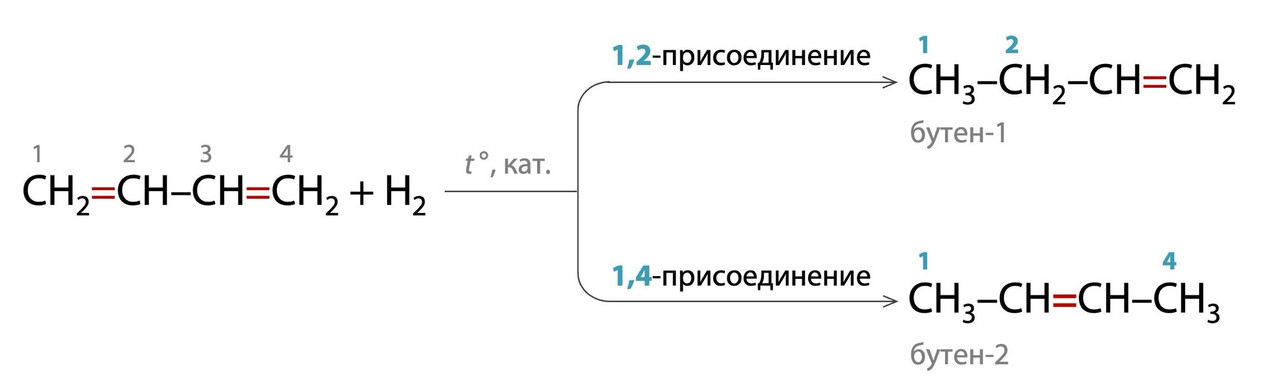
На ЕГЭ в гирировании алкадиенов до алкенов просто пишут +H₂, кат., «экзотику» не приводят. Но для самых любознательных из вас я ее покажу! Избирательно получить бутен-2 из бутадиена-1,3 можно при использовании амальгамы натрия Na(Hg) в водно-спиртовой среде.
Галогенирование сопряженных алкадиенов (+ Cl2/Br2):
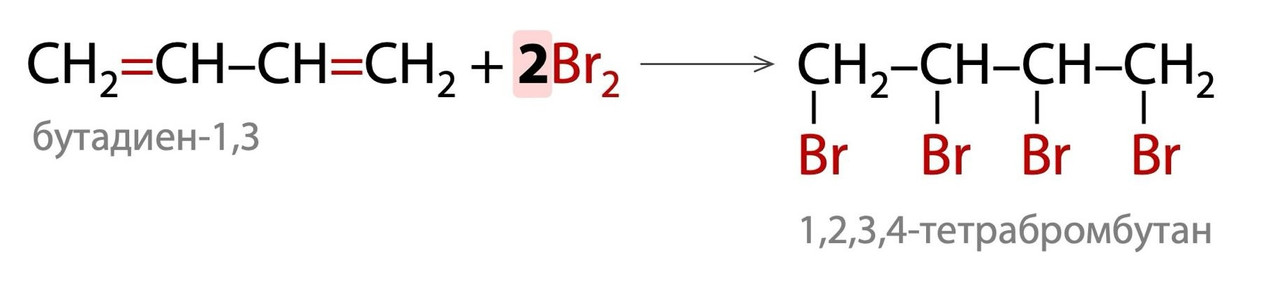
1. В избытке галогена присоединение протекает по двум π-связям и образуются тетрагалогеналканы. Это работает и для сопряженных, и для изолированных алкадиенов!
2. Если галогенирование протекает при охлаждении (t < 0ᵒ), то образуется продукт 1,2-присоединения, как и для обычных алкенов.
3. Если галогенирование протекает при нагревании (t > 0ᵒ), то образуется продукт 1,4-присоединения по концам сопряженной системы, а одна π-связь «мигрирует» ко второму атому углерода.
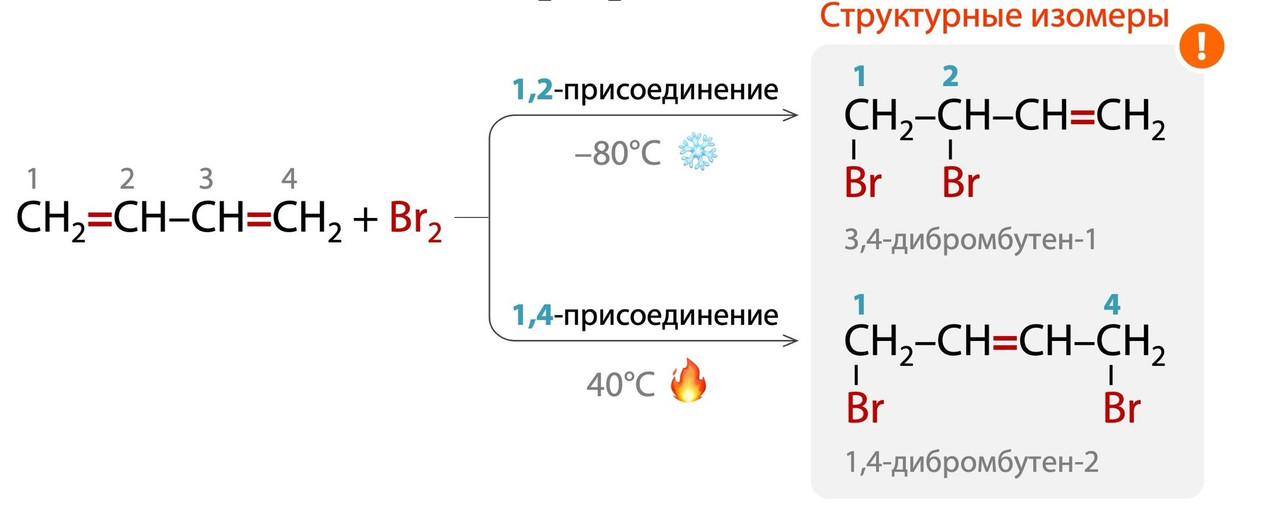
В галогенировании уже нет «экзотики», как в гидрировании, здесь все решает только температура, поэтому будьте внимательны с условиями реакций.
Интересно, что если мы проведем галогенирование при охлаждении, получим смесь с преимущественным содержанием 1,2-продукта, а затем нагреем эту смесь, то 1,2-продукт изомериуется в более устойчивый при повышенной температуре 1,4-продукт. Магия органики!
Гидрогалогенирование сопряженных алкадиенов (+ HCl/HBr):
1. Если присоединение HCl/HBr протекает при охлаждении (t < 0ᵒ), то образуется продукт 1,2-присоединения по правилу Марковникова, как и для обычных алкенов.
2. Если присоединение HCl/HBr протекает при нагревании (t > 0ᵒ), то образуется продукт 1,4-присоединения по концам сопряженной системы, а одна π-связь «мигрирует» ко второму атому углерода.
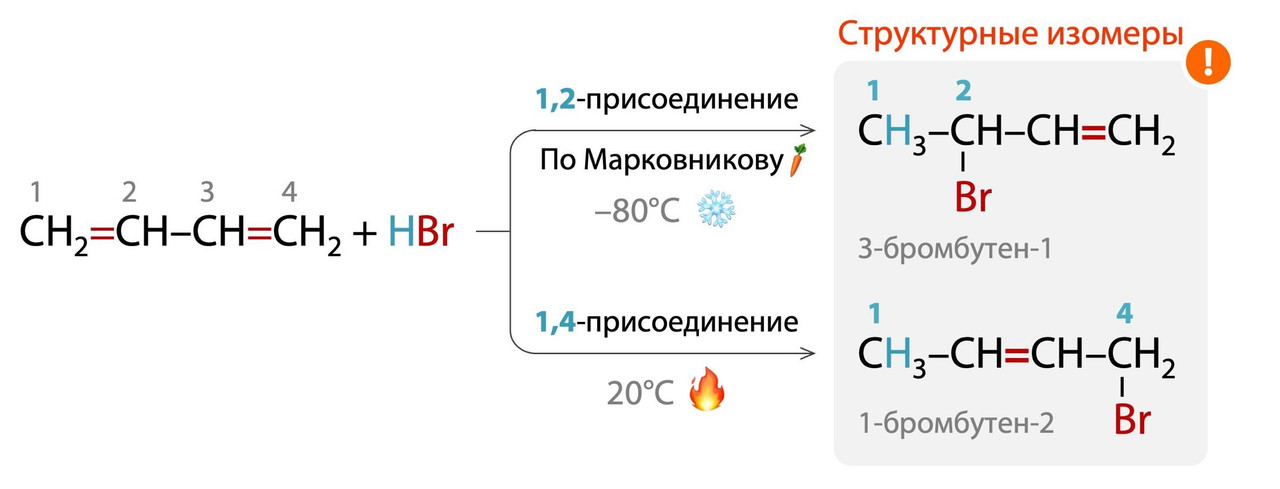
3. В случае изолированных алкадиенов присоединение HCl/HBr протекает как для обычных алкенов по правилу Марковникова.
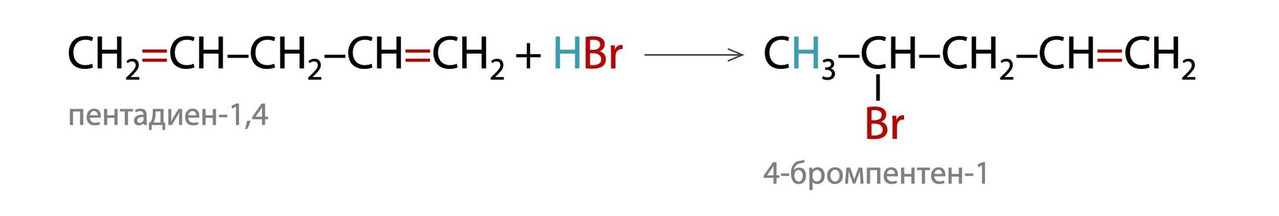
На ЕГЭ до сих пор встречаются реакции гидрогалогенирования алкадиенов только в соотношении 1:1, а присоединение второй молекулы HCl/HBr не рассматривается.
Полимеризация алкадиенов — одна из важнейших тем, связанная с нашей жизнью! Из сопряженных алкадиенов получают полимеры, строение которых указывает на предпочтительность 1,4-присоединения в таких реакциях. Обсудим те, которые встретятся на ЕГЭ:
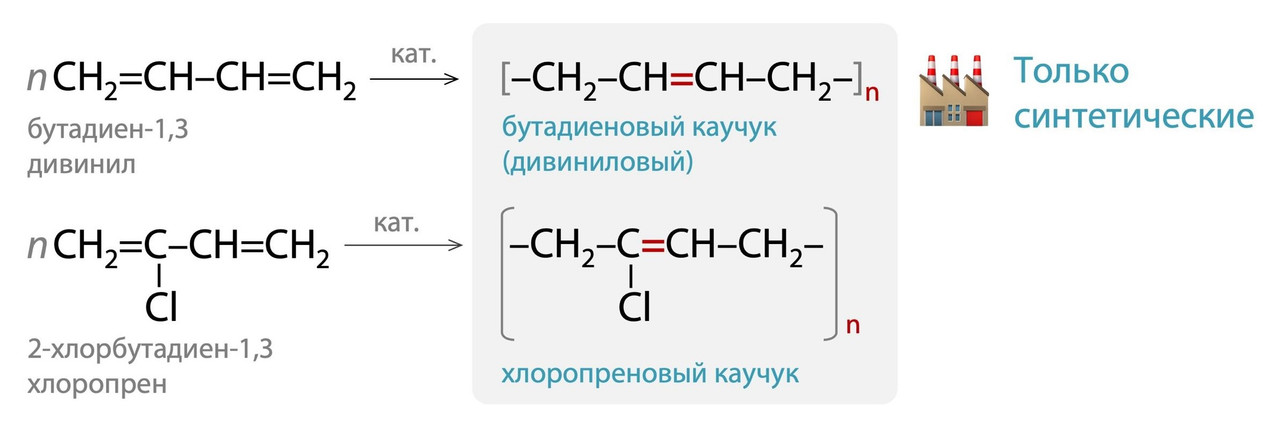
1. Бутадиен-1,3 → бутадиеновый каучук
Дивиниловый каучук: его нет в природе, он синтетический. Используется при изготовлении уплотнителей, шлангов или подошв обуви.
2. Хлоропрен → хлоропреновый каучук
Его тоже нет в природе, он синтетический. Используется при изготовлении гидрокостюмов, противопожарных покрытий, ортопедических изделий или непромокаемой обуви.
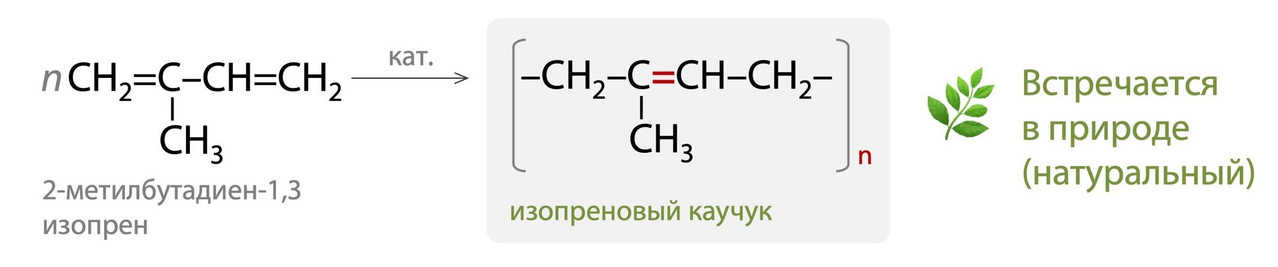
3. Изопрен → изопреновый каучук
Он есть в природе, относится к натуральным. Используется при изготовлении шин, медицинских перчаток, мячей или спортивного инвентаря.
Обратите внимание, что в составе каждого звена есть двойная С=С связь, которой не было полимерах, полученных из алкенов. Из-за этих связей можно проводить вулканизацию каучука (реакцию с серой, «сшивание» молекул каучука мостиками -S-S-) для получения резины, увеличения прочности и избавления от липкости.
Окислительно-восстановительные реакции с участием алкадиенов. Что про них нужно знать?
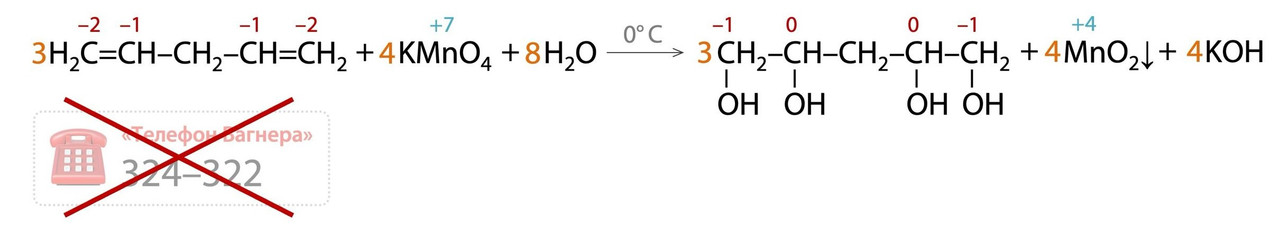
1. Мягкое окисление водным раствором перманганата при охлаждении встречается для изолированных алкадиенов с образованием четырехатомных спиртов. И тут не нужно «звонить Вагнеру», алкадиены ≠ алкены!
2. Жесткое окисление алкадиенов нормального строения в кислой среде протекает с полным разрывом С=С связей и образованием:
— СО₂ из бутадиена-1,3
— СО₂ и двухосновных кислот из изолированных алкадиенов
3. Жесткое окисление алкадиенов нормального строения в щелочной среде протекает с полным разрывом С=С связей и образованием:
— K₂CO₃/Na₂CO₃ из бутадиена-1,3
— K₂CO₃/Na₂CO₃ и солей двухосновных кислот из изолированных алкадиенов
4. Если при С=С связи находится третичный атом углерода в составе алкадиена, то в результате жесткого окисления он войдет в состав кетогруппы С=О. Пример на картинке ниже:
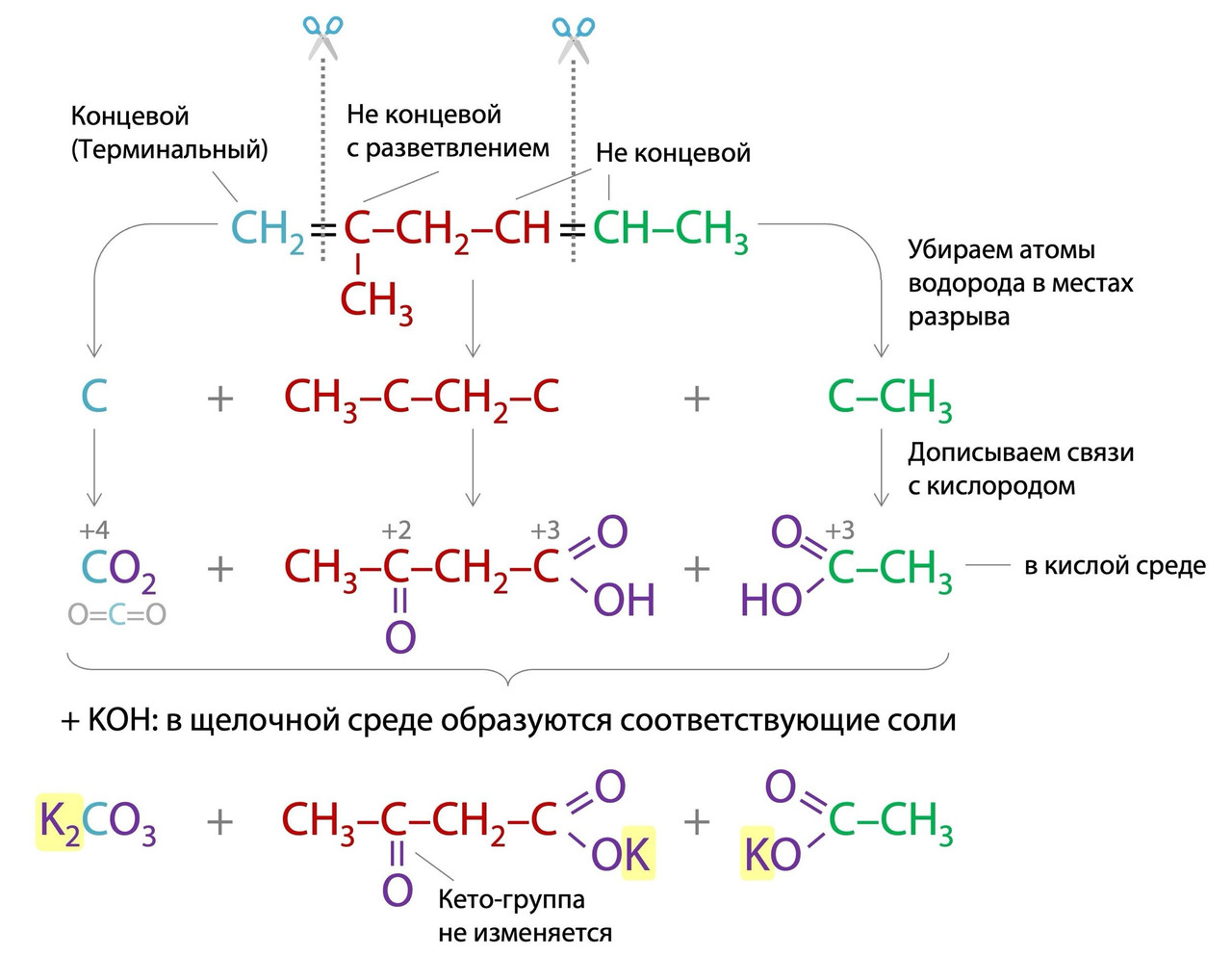
Бутадиен-1,3 (дивинил) окисляется перманганатом калия в кислой среде до углекислого газа СО2, т.к. щавелевая кислота, которая гипотетически должна была получиться из центрального фрагмента с двумя углеродами, продолжит реагировать с перманганатом и "не выживет" в условиях проведения реакции:
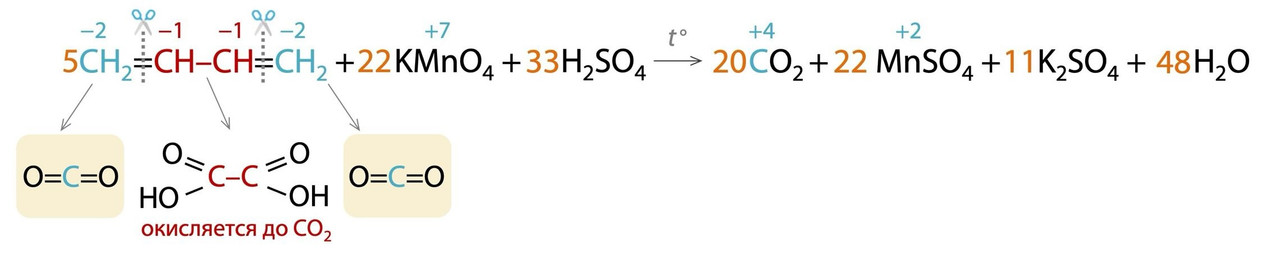
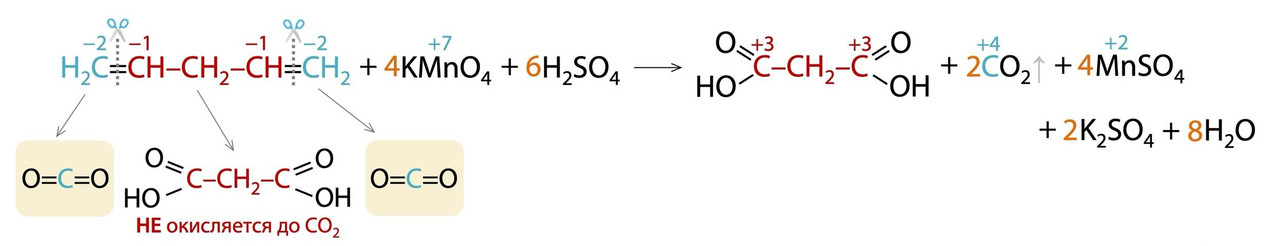
Пентадиен-1,4 окисляется перманганатом калия в кислой среде без сюрпризов: образуется двухосновная (с двумя СООН группами) кислота из центрального фрагмента из трех углеродов и углекислый газ СО2 из концевых фрагментов СН2.
Способы получения алкадиенов
Реакция Лебедева. Одна из красивейших реакций в углеводородах. Если бутадиен-1,3 получить из этанола по реакции Лебедева, потом из него сделать бутадиеновый каучук, а из него резиновый прорезыватель для зубок младенца — это законно? Шучу, конечно, законно. Запомните ее, потому что она будет часто встречаться и в тесте, и в цепочках!
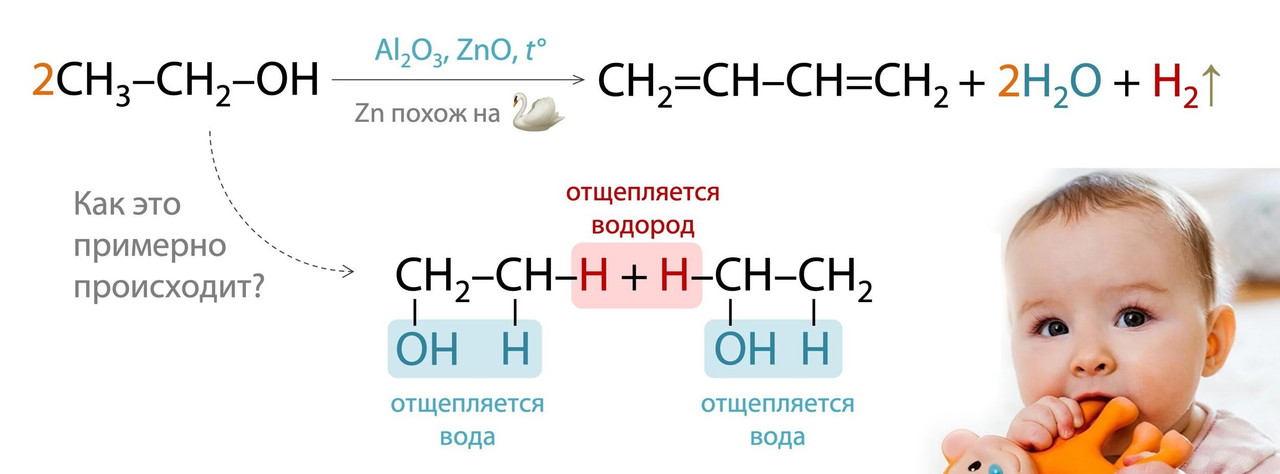
Дегидрирование алканов (отщепление водорода -Н2). Если у алкана 4 и более атомов углерода в главной цепи, то энергетически выгодно получить сопряженную систему С=С связей. Поэтому в результате дегидрирвоания н-бутана или метилбутана преимущественно образуются алкадиены, а не алкены/алкины:
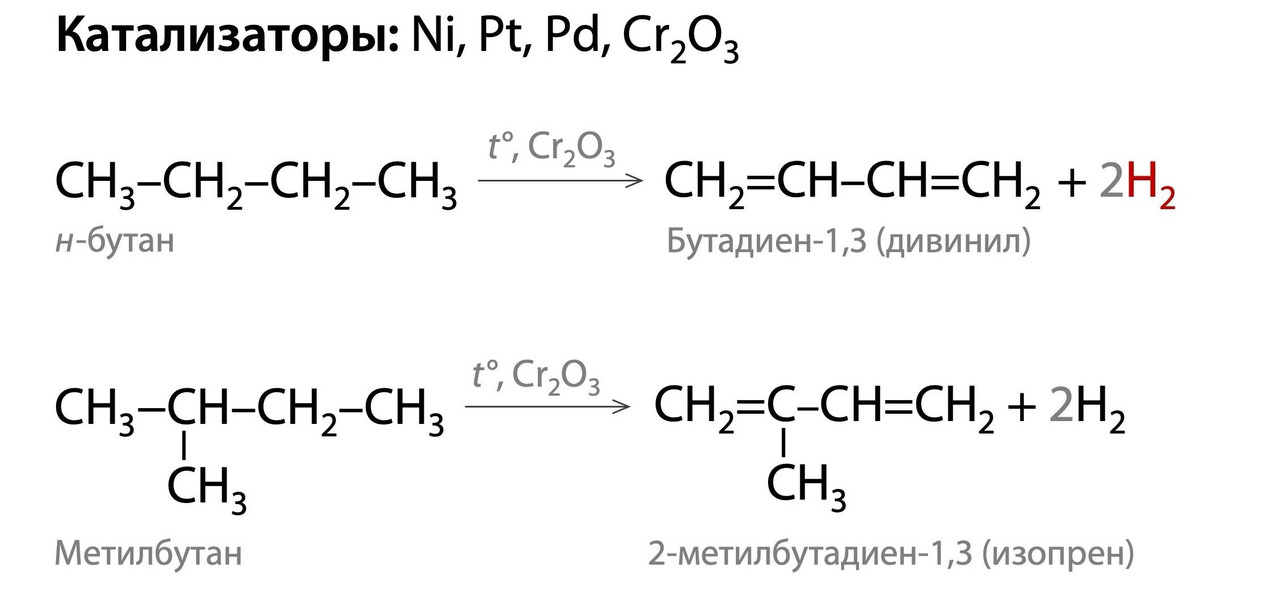
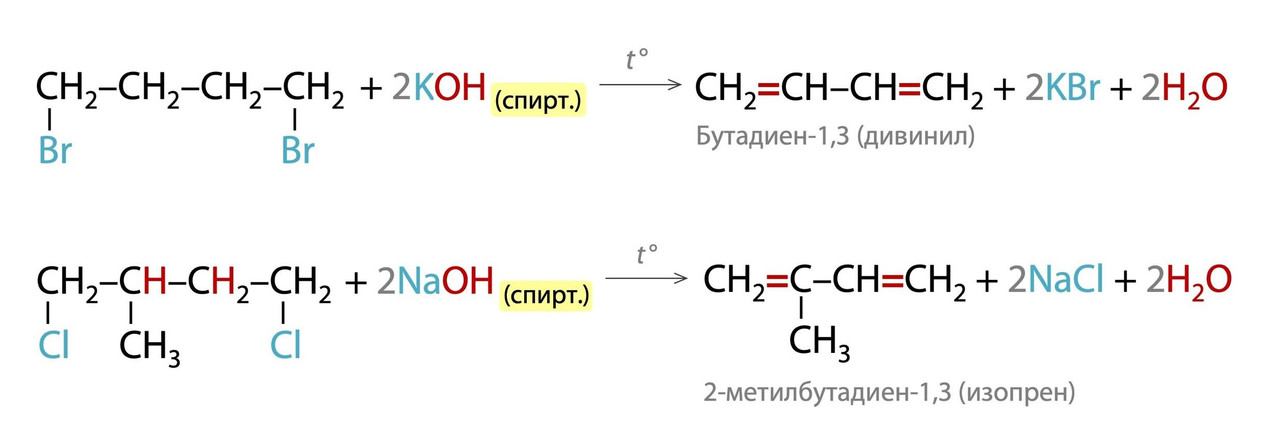
Дегидрогалогенирование. Если при добавлении спиртового раствора щелочи и отщеплении двух HCl/HBr/HI можно получить сопряженную систему из чередующихся С=С и С-С связей, то именно она и будет образовываться. Вспомните про устойчивость сопряженных алкадиенов! Такие реакции часто встречаются в тестовых заданиях и цепочках №32 ЕГЭ:
Что порешать?
На нашем сайте есть бесплатные тесты, которые помогут усвоить материал по теме "Алкадиены". Прямые ссылки на них:
- 65 тестовых заданий по строению, изомерии, номенклатуре, свойствам и получению алкадиенов: https://stepenin.ru/lesson/516
- 10 цепочек формата №32 ЕГЭ с участием циклоалканов и алкадиенов (с подробным видеоразбором каждого решения): https://stepenin.ru/lesson/988
🏆 На странице платного курса для 10 класса по органике намного больше заданий к этой теме в самом первом модуле. Прямая ссылка на тему "Алкадиены": https://stepenin.ru/chapter/357
Понравилось такое обобщение изученного материала? Поделись статьей с друзьями, которые учат органику. Учим химию вместе! 🫶🏼