NEUROANATOMÍA, NÚCLEO ESPINAL DEL TRIGÉMINO
Nelson Rubal
20 de enero de 2023
www.ncbi.nlm.nih.gov - Neel M. Patel, Felix Jozsa, Joe M Das, Erzurumlu Rs, Killackey Hp., Arends Jj, Woelders-Blok A, Dubbeldam20 de enero de 2023
Introducción
El núcleo espinal del nervio trigémino (SN) es un tracto sensorial situado en la parte lateral médula oblongada del tronco encefálico cuya función principal es transmitir sensaciones de dolor y temperatura desde la cavidad oral y la superficie de la cara. Se subdivide en tres segmentos que representan regiones topográficas de la cara de forma invertida; la frente se representa ventralmente (distalmente), y la región oral se representa dorsalmente (proximalmente).
Las lesiones del SN causan importantes síndromes clínicos debido a la utilidad crucial en la vida diaria de la región orofacial.
Estructura y función
El núcleo espinal del trigémino (SN) está situado en la parte lateral de la médula oblongada del tronco encefálico. Se extiende inferiormente hasta el nivel de la vértebra C3, en cuyo punto se hace continuo con el asta espinal dorsal [1]. Es responsable de la transmisión de diversas modalidades sensoriales, como la temperatura, el tacto y el dolor de la porción ipsilateral de la cara, así como de las entradas nociceptivas de la duramadre supratentorial [2].
El núcleo espinal también recibe información sensorial de otros nervios craneales, pero sus entradas y su importancia fisiológica proceden principalmente de las tres divisiones extracraneales del nervio trigémino (V1, oftálmico; V2, maxilar; V3, mandibular). Estos nervios extracraneales se fusionan inicialmente en el ganglio del trigémino y penetran en la bóveda craneal a través de la fisura orbitaria superior, el agujero redondo y el agujero oval [3]. Después del ganglio del trigémino, las fibras se dividen en raíces sensitivas y motoras, que se distribuyen a los núcleos del trigémino (núcleo mesencefálico, núcleo motor, núcleo sensitivo principal y núcleo espinal) antes de proyectarse hacia la corteza [4].
El núcleo espinal del nervio trigémino es un núcleo de forma longitudinal situado en la parte inferior del puente, médula oblongada y superior de la ME, que recibe sensibilidad relacionadas con el dolor y la temperatura de la región orofacial suministrada por el nervio trigémino y, junto con el núcleo sensorial principal, a veces se denomina complejo nuclear sensorial del trigémino (CNST) [1]. El núcleo espinal también recibe fibras aferentes de otros nervios craneales, como el nervio facial (CN VII) a través del ganglio geniculado, el nervio glosofaríngeo (CN IX) a través del ganglio petroso y el nervio vago (CN X) a través del ganglio nodoso [5].
El núcleo espinal se subdivide anatómicamente en pars oralis, pars interporalis y pars caudalis [6]. La pars oralis es la terminación de las conexiones aferentes de las regiones oral y nasal y contiene circuitos implicados en los reflejos del tronco encefálico. La pars interpolaris recibe entradas de la cara ipsilateral y forma el tracto trigeminotalámico anterior ascendente con la pars oralis. La pars caudalis también recibe información de la cara, la frente, las mejillas y la mandíbula, y está implicada en la transmisión de la sensación de temperatura desde esta zona. La representación topográfica de las entradas al núcleo trigémino espinal está invertida, de forma que el área que codifica la frente está representada ventralmente (distalmente), y el área que codifica la región oral está representada dorsalmente (proximalmente).
El núcleo espinal se proyecta tanto contralateral como ipsilateralmente al núcleo posteromedial ventral del tálamo a través de los tractos trigeminotalámicos ventral y dorsal [1]. Esta información sensorial se transmitirá del tálamo a la corteza motora primaria a través de la corteza sensorial primaria, lo que permitirá responder a los estímulos de la cara. Esta capacidad de reaccionar ante estímulos nocivos para la cara y de protegernos del daño hace que el núcleo espinal del trigémino sea un componente fundamental de la vía sensorial.
Embriología
Durante el desarrollo embriológico, los núcleos de los nervios craneales son algunas de las estructuras más tempranas del cerebro en emerger y son distinguibles en el día 28. Los núcleos sensoriales del trigémino se desarrollan a partir de células de la cresta neural, una población altamente migratoria de células multipotentes que se origina en el tubo neural dorsal [7]. Los núcleos del trigémino se desarrollan inicialmente en el metencéfalo y el mielencéfalo antes de desplazarse parcialmente al mesencéfalo [8].
Riego sanguíneo y linfático
La zona del tronco encefálico donde se sitúa el núcleo espinal del trigémino está irrigada por la arteria cerebelosa inferior posterior (PICA)[9]. La PICA está formada por las cuatro ramas de las arterias vertebrales pares y nace aproximadamente 16 mm antes de que las arterias vertebrales se unan para formar la arteria basilar [10]. A continuación, se divide en cinco segmentos anatómicos: el segmento medular anterior, el segmento medular lateral, el segmento amigdalomedular, el segmento telovelotonsilar y el segmento cortical [11].
Específicamente relacionados con el núcleo espinal del nervio trigémino están el primero y el segundo de estos segmentos, que pasan por la parte ventrolateral del tronco encefálico. Cualquier interrupción del flujo sanguíneo a través de la arteria vertebral o la arteria cerebelosa posterior inferior interrumpiría el procesamiento de la información sensorial procedente del nervio trigémino. Tales patologías incluyen la disección de la arteria vertebral, la oclusión trombótica y la estenosis por compresión extrínseca, como la producida por un tumor o una banda fibrosa [12].
Nervios
El núcleo espinal del trigémino incorpora información sensorial de las tres ramas del nervio trigémino (CN V). El CN V1, también conocido como nervio oftálmico, transmite información sensorial de la cara en regiones situadas por encima de la órbita de los ojos. El CN V2, también conocido como nervio maxilar, es el principal responsable de la información sensorial entre la órbita y la boca. La última rama es el CN V3, también conocido como nervio mandibular. El CN V3 tiene tanto un componente sensorial como un componente motor; sin embargo, sólo el componente sensorial se proyecta al núcleo espinal.
El núcleo espinal del trigémino también consolida la información sensorial de los nervios facial, glosofaríngeo y vago; se trata de una función menor en comparación con su integración de la información sensorial de las tres ramas del nervio trigémino.
Consideraciones quirúrgicas
Debe tenerse en cuenta que, dado que el tracto trigémino espinal se extiende inferiormente hasta el nivel de C3, este tracto puede verse afectado clínicamente en pacientes con patologías de la unión craneovertebral. Por la misma razón, la intervención quirúrgica a este nivel, por ejemplo, la descompresión de la fosa posterior, podría afectar a esta zona y a las estructuras del tronco encefálico relacionadas.
El extremo caudal del núcleo trigémino espinal termina a nivel del obex del cuarto ventrículo en un tubérculo elevado, denominado tubérculo trigémino. Se trata de un valioso punto de referencia para los neurocirujanos que operan en esta región.
Importancia clínica
Síndrome Medular Lateral
El síndrome medular lateral, también conocido como síndrome medular o de la arteria cerebelosa inferior posterior, se produce debido a la oclusión de la arteria cerebelosa inferior posterior o de la arteria vertebral. La oclusión de cualquiera de estas arterias puede provocar una falta de flujo sanguíneo a la médula lateral, donde se encuentra el núcleo espinal. Los eventos isquémicos primarios que desencadenan el síndrome medular lateral pueden ser el resultado de vasos sanguíneos estenóticos, como se observa en adultos, a menudo con otras afecciones comórbidas. En los niños, sin embargo, la isquemia puede deberse a una lesión de la arteria vertebral tras una lesión por hiperextensión del cuello [13].
El síndrome medular lateral se presenta con muchos síntomas, incluida la pérdida contralateral de la sensación de dolor y temperatura en el cuerpo con síndrome de Horner ipsilateral, disfagia y pérdida de la sensación en la cara [14]. Esta pérdida ipsilateral de la sensación facial se debe a la falta de riego sanguíneo a través de la arteria cerebelosa inferior posterior al núcleo espinal. Este núcleo es responsable de transmitir la información sensorial del nervio trigémino a la corteza sensorial primaria, lo que lo convierte en un actor clave en la presentación del síndrome medular lateral.
Neuralgia del trigémino
La neuralgia del trigémino es una afección que suele cursar con sensaciones dolorosas unilaterales, punzantes y paroxísticas de la cara a lo largo de la distribución del nervio trigémino [15] Existen múltiples teorías sobre el mecanismo subyacente de esta afección. Las etiologías se han dividido en neuralgia del trigémino idiopática, primaria y secundaria. Los mecanismos periféricos sugeridos implican defectos a lo largo de la vía del nervio trigémino antes de entrar en el tronco encefálico. Una hipótesis reciente atribuye el dolor de la neuralgia del trigémino a un mecanismo central que implica a la pars oralis del núcleo trigémino espinal [16].
Esta teoría tiene como base la caracterización de la neuralgia del trigémino como epilepsia focal e hiperactividad neuronal. Se ha demostrado que un aumento de la actividad en el núcleo espinal precipita el dolor observado en la neuralgia del trigémino tanto en gatos como en monos. Además, la administración de medicamentos antiepilépticos en gatos y monos fue capaz de disminuir la intensidad y duración de los ataques. La dificultad de los enfoques terapéuticos hace imperativa la comprensión de la neuralgia del trigémino. Aunque no hay consenso sobre el mecanismo subyacente de la neuralgia del trigémino, pruebas recientes sugieren que el núcleo espinal, en particular la pars oralis, desempeña un papel vital en este proceso [17].
Dolor orofacial crónico
Es importante comprender el dolor orofacial crónico, ya que se ha determinado que es una fuente de angustia psicológica significativa en los pacientes. Es probable que esta angustia se deba a que los procedimientos y los medicamentos a menudo no pueden aliviar los síntomas [18] Una mejor comprensión del mecanismo subyacente puede ayudar a crear nuevas soluciones a esta falta de eficacia del tratamiento. En el procesamiento del dolor orofacial, el núcleo trigémino espinal, concretamente la pars caudalis, se proyecta al núcleo talámico ventral posteromedial y al núcleo parabraquial [19].
Recientemente se ha realizado un estudio en humanos para demostrar los cambios en las sinapsis de pacientes con dolor neuropático orofacial crónico. Utilizando imágenes de RM ponderadas en T1, el estudio demostró que las alteraciones en la anatomía de las sinapsis primarias del nervio trigémino, especialmente en la pars oralis, son fundamentales tanto para la generación como para el mantenimiento del dolor crónico en la distribución del nervio trigémino. Estos cambios incluyen una reducción significativa del volumen regional de materia gris, una disminución de la difusividad media y un aumento de la anisotropía fraccional [20]. Las imágenes de las vías periféricas del nervio trigémino no mostraron cambios significativos en la anatomía en el contexto del dolor orofacial crónico, lo que disminuye la probabilidad de su implicación en la fisiopatología de esta afección. Los cambios anatómicos de la pars oralis del nervio trigémino espinal son responsables de la presentación del dolor orofacial crónico.
Distonía cráneo-cervical
La distonía craniocervical es un trastorno neurológico poco conocido, que forma parte del grupo de las distonías focales primarias que cursan con contracciones musculares involuntarias, sostenidas o intermitentes [21].[21] No se ha encontrado ninguna causa ni gen patológico candidato, y el tratamiento de esta afección, que tiene efectos deletéreos significativos en la calidad de vida, sigue siendo limitado. [22] Los reflejos trigeminales, que indican la vía de funcionamiento del nervio y los núcleos trigeminales (y, por tanto, del n. espinal), incluyen la retracción de la cabeza, el reflejo corneal y los reflejos de sacudida mandibular. [23]
La observación de que estos reflejos asociados con los ganglios del trigémino son aberrantes en pacientes con distonía craneocervical ha llevado a la hipótesis de que la plasticidad aberrante en los ganglios basales que conduce a la inhibición tónica del complejo sensorial del trigémino puede estar implicada en el proceso patológico de esta afección. [24] Además, las pruebas experimentales anatómicas y electrofisiológicas han demostrado la necesidad de la función normal del complejo sensorial del trigémino para el control motor normal de los músculos de la cabeza y el cuello [6]. Por estos motivos, se plantea la hipótesis de que la neuromodulación de esta zona, incluido el núcleo espinal del trigémino, ya sea por medios invasivos o no invasivos, puede proporcionar beneficios terapéuticos en pacientes con esta afección [6].
Otras cuestiones
Existen pruebas en ratas que sugieren la presencia de receptores de oxitocina tanto en la médula oblonga como en el puente de Varolio [25]. Estos receptores de oxitocina están presentes en el núcleo espinal; sin embargo, al igual que ocurre con los receptores de oxitocina en otras regiones de la médula y el puente de Varolio, desaparecen en el día 10 postnatal. En el momento del nacimiento, se produce un aumento de la liberación materna de oxitocina, que probablemente actúa también sobre estos receptores de oxitocina; esto indica un papel temprano y transitorio de la oxitocina en el desarrollo neuronal del periodo neonatal. Aún está por determinar el alcance total del efecto de la oxitocina en el desarrollo neuronal postnatal.
Neuroanatomy, Spinal Trigeminal Nucleus
January 20, 2023

Introduction
The spinal trigeminal nucleus (SN) is a sensory tract located in the lateral medulla of the brain stem whose principal function is relaying pain and temperature sensations from the oral cavity and the surface of the face. It is subdivided into three segments representing topographical regions of the face in an inverted fashion; the forehead is represented ventrally (distally), and the oral region is represented dorsally (proximally). Lesions of the SN cause important clinical syndromes owing to the crucial utility in the daily life of the orofacial region.
Structure and Function
The spinal trigeminal nucleus (SN) is located in the lateral medulla of the brainstem. It extends down to the level of the C3 vertebra, at which point it becomes continuous with the dorsal spinal horn. [1] It is responsible for relaying various sensory modalities, including temperature, touch, and pain from the ipsilateral portion of the face, as well as nociceptive inputs from the supratentorial dura mater. [2]
The SN incorporates sensory information from different cranial nerves, but its inputs and physiological importance come principally from the three extracranial divisions of the trigeminal nerve (V1, ophthalmic; V2, maxillary; V3, mandibular). These extracranial nerves initially fuse at the trigeminal ganglion, entering the cranial vault through the superior orbital fissure, foramen rotundum, and foramen ovale.[3] After the trigeminal ganglion, the fibers divide into sensory and motor rootlets, which are then distributed to the trigeminal nuclei (mesencephalic nucleus, motor nucleus, principal sensory nucleus, and spinal nucleus) before projecting onwards to the cortex. [4]
The spinal nucleus of the trigeminal nerve is a longitudinally-shaped nucleus situated in the caudal pons and medulla, which receives sensory afferents relating to pain and temperature from the orofacial region supplied by the trigeminal nerve and, together with the principal sensory nucleus, is sometimes termed the trigeminal sensory nuclear complex (TSNC) [1]. The SN also receives afferent fibers from other cranial nerves, including the facial nerve (CN VII) via the geniculate ganglion, the glossopharyngeal nerve (CN IX) via the petrosal ganglion, and the vagus nerve (CN X) via the nodose ganglion [5].
The spinal trigeminal nucleus is further subdivided anatomically into the pars oralis, pars interporalis, and pars caudalis [6]. The pars oralis is the termination of afferent connections from the oral and nasal regions and contains circuits involved in brain stem reflexes. The pars interpolaris receives inputs from the ipsilateral face and forms the ascending anterior trigeminothalamic tract with the pars oralis. The pars caudalis also receives input from the face, forehead, cheek, and jaw, as well as being involved in transmitting temperature sensation from this area. The topographical representation of the inputs to the spinal trigeminal nucleus is inverted, such that the area encoding the forehead is represented ventrally (distally), and the area encoding the oral region is represented dorsally (proximally).
The SN projects both contralaterally and ipsilaterally to the ventral posteromedial nucleus of the thalamus via the ventral and dorsal trigeminothalamic tracts [1]. This sensory information will be relayed from the thalamus to the primary motor cortex via the primary sensory cortex, allowing response to stimuli of the face. This ability to react to noxious stimuli to the face and remove ourselves from harm makes the spinal trigeminal nucleus a pivotal component of the sensory pathway.
Embryology
During embryological development, the cranial nerve nuclei are some of the earliest structures in the brain to emerge and are distinguishable by day 28. The trigeminal sensory nuclei develop from neural crest cells, a highly migratory population of multipotent cells that originates in the dorsal neural tube. [7] The trigeminal nuclei develop initially in the metencephalon and myelencephalon before being partly displaced into the mesencephalon. [8]
Blood Supply and Lymphatics
The area of the brainstem where the spinal trigeminal nucleus is situated is supplied by the posterior inferior cerebellar artery (PICA) [9]. The PICA is the four branches from the paired vertebral arteries and arises approximately 16 mm before the vertebral arteries join to form the basilar artery. [10] It is then divided into five anatomical segments: the anterior medullary segment, lateral medullary segment, tonsillomedullary segment, telovelotonsillar segment, and cortical segment. [11]
Specifically related to the spinal nucleus of the trigeminal nerve are the first and second of these segments, which pass over the ventrolateral part of the brainstem. Any disruption of blood flow through the vertebral artery or posterior inferior cerebellar artery would interrupt the processing of sensory information from the trigeminal nerve. Such pathologies include vertebral artery dissection, thrombotic occlusion, and stenosis from extrinsic compression, such as from a tumor or fibrous band.[12]
Nerves
The spinal trigeminal nucleus incorporates sensory information from all three branches of the trigeminal nerve (CN V). CN V1, also known as the ophthalmic nerve, relays sensory information from the face in regions located above the orbit of the eyes. CN V2, also known as the maxillary nerve, is primarily responsible for sensory information between the orbit and the mouth. The final branch is CN V3, also known as the mandibular nerve. CN V3 has both a sensory component as well as a motor component; however, only the sensory component projects to the SN.
The spinal trigeminal nucleus also consolidates sensory input from the facial, glossopharyngeal, and vagus nerves; this is a minor role of SN in comparison to its integration of sensory information from the three branches of the trigeminal nerve.
Surgical Considerations
It should be kept in mind that since the spinal trigeminal tract extends inferiorly down to the level of C3, this tract can be involved clinically in patients with craniovertebral junction pathologies. For the same reason, surgical intervention at this level, for example, posterior fossa decompression, could affect this area and related brainstem structures.
The caudal end of the spinal trigeminal nucleus terminates at the obex of the fourth ventricle in a raised tubercle, termed the trigeminal tubercle. This is a valuable landmark for neurosurgeons operating in this region.
Clinical Significance
Lateral Medullary Syndrome
Lateral medullary syndrome, also known as medullary or posterior inferior cerebellar artery syndrome, occurs due to the occlusion of the posterior inferior cerebellar artery or the vertebral artery. An occlusion to either of these arteries can result in a lack of blood flow to the lateral medulla, the location of the spinal trigeminal nucleus. The primary ischemic events that trigger lateral medullary syndrome can result from stenotic blood vessels, as seen in adults, often with other comorbid conditions. In children, however, ischemia can be due to injury to the vertebral artery following a hyperextension neck injury.[13]
The lateral medullary syndrome presents with many symptoms, including contralateral loss of pain and temperature sensation in the body with ipsilateral Horner syndrome, dysphagia, and loss of sensation in the face.[14] This ipsilateral loss of facial sensation is due to a lack of blood supply via the posterior inferior cerebellar artery to the spinal trigeminal nucleus. This nucleus is responsible for relaying sensory information from the trigeminal nerve to the primary sensory cortex, making it a key player in the presentation of lateral medullary syndrome.
Trigeminal Neuralgia
Trigeminal neuralgia is a condition that most often presents with unilateral, stabbing, and paroxysmal painful sensations from the face along the trigeminal nerve distribution. [15] There are myriad theories regarding the underlying mechanism of this condition. The etiologies have been broken down into idiopathic, primary, and secondary trigeminal neuralgia. Suggested peripheral mechanisms involve defects along the trigeminal nerve pathway before entering the brainstem. A recent hypothesis attributes the pain of trigeminal neuralgia to a central mechanism involving the pars oralis of the spinal trigeminal nucleus. [16]
This theory has as its basis the characterization of trigeminal neuralgia as focal epileptic and neuronal hyperactivity. An increase in activity at the spinal trigeminal nucleus has been shown to precipitate the pain seen in trigeminal neuralgia in both cats and monkeys. Furthermore, the administration of anti-epileptic medications in cats and monkeys was able to decrease the intensity and duration of the attacks. The difficulty of treatment approaches makes the understanding of trigeminal neuralgia imperative. Though there is no consensus on the underlying mechanism of trigeminal neuralgia, recent evidence suggests that the spinal trigeminal nucleus, particularly the pars oralis, plays a vital role in this process. [17]
Chronic Orofacial Pain
Understanding chronic orofacial pain is important as it has been determined as a source of significant psychological distress in patients. This distress is likely because procedures and medications often cannot relieve symptoms. [18] A better understanding of the underlying mechanism may help create new solutions to this lack of treatment efficacy. In processing orofacial pain, the spinal trigeminal nucleus, specifically the pars caudalis, projects to the ventral posteromedial thalamic nucleus and the parabrachial nucleus. [19]
A recent study was conducted in humans to demonstrate changes in synapses of patients with chronic orofacial neuropathic pain. Utilizing T1-weighted MRI imaging, the study showed that alterations in the anatomy of primary synapses of the trigeminal nerve, particularly in the pars oralis, are critical for both the generation and maintenance of chronic pain in the distribution of the trigeminal nerve. These changes included significant regional gray matter volume reduction, a decrease in mean diffusivity, and a fractional anisotropy increase.[20] Imaging of the peripheral pathways of the trigeminal nerve showed no significant change in the anatomy in the setting of chronic orofacial pain, thus decreasing the likelihood of its involvement in the pathophysiology of this condition. Anatomical changes to the pars oralis of the spinal trigeminal nerve are responsible for the presentation of chronic orofacial pain.
Craniocervical Dystonia
Craniocervical dystonia is a poorly-understood neurological disorder, part of the group of primary focal dystonias which present with involuntary muscle contractions, sustained or intermittent. [21] No cause or candidate pathological gene has been found, and treatment for this condition, which has significant deleterious effects on quality of life, remains limited.[22] Trigeminal reflexes, which indicate the functioning pathway of the trigeminal nerve and nuclei (and therefore the SN), include head retraction, corneal reflex, and jaw jerk reflexes.[23]
The observation that these reflexes associated with the trigeminal ganglia are aberrant in patients with craniocervical dystonia has led to the hypothesis that aberrant plasticity in the basal ganglia leading to tonic inhibition of the trigeminal sensory complex may be involved in the pathological process of this condition.[24] Furthermore, anatomical and electrophysiological experimental evidence has demonstrated the need for the normal function of the trigeminal sensory complex for normal motor control of head and neck muscles.[6] For these reasons, it is hypothesized that neuromodulation of this area, including the trigeminal spinal nucleus, either by invasive or non-invasive means, may provide therapeutic benefits in patients with this condition.[6]
Other Issues
There is evidence in rats suggesting the presence of oxytocin receptors in both the medulla oblongata and pons.[25] These oxytocin receptors are present in the spinal trigeminal nucleus; however, as is seen with oxytocin receptors in other regions of the medulla and pons, they disappear by postnatal day 10. At the time of birth, there is an increase in the maternal release of oxytocin, likely acting on these oxytocin receptors as well; this indicates an early and transient role of oxytocin in the neuronal development of the neonatal period. The full extent of the effect of oxytocin on neuronal development postnatally is yet to be determined.
Figure
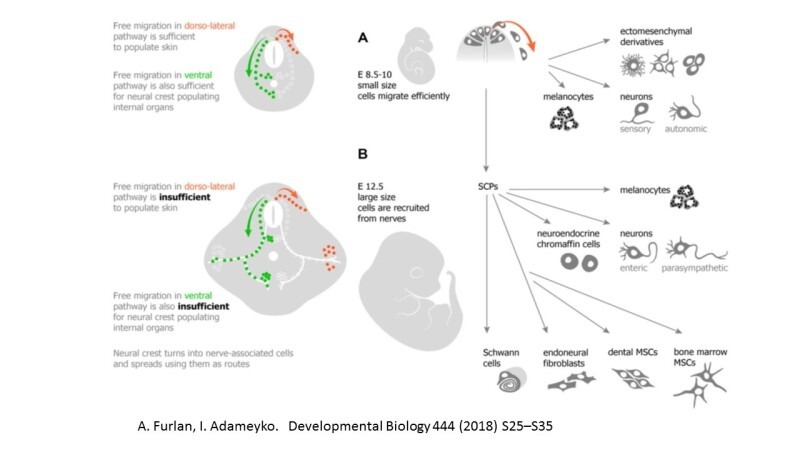
Neural Crest derivatives: Migratory neural crest and nerve-associated Schwann cell precursors represent a long-lasting source of multipotent progenitors available in any body location due to diversification of dissemination strategies. Outline of dissemination (more...)
Figure
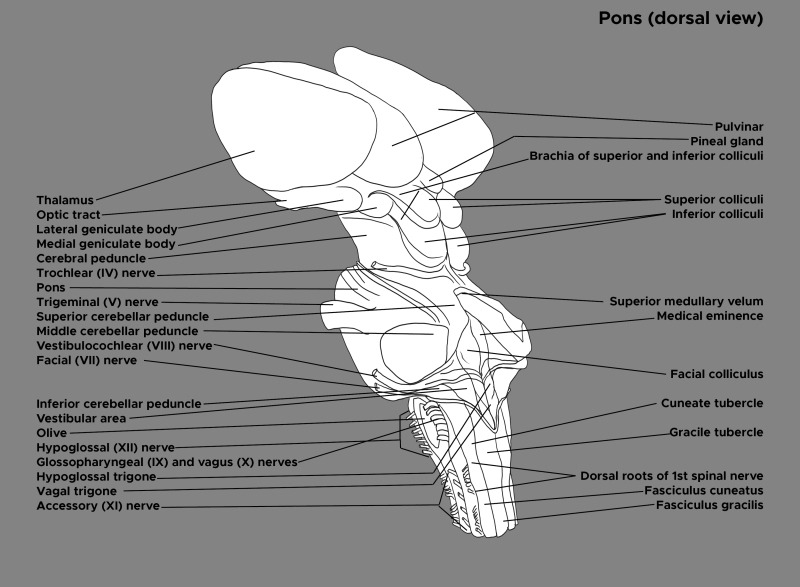
Illustration and labels of the brain stem. Dorsal view. Thalamus, optic tract, pons, trigeminal nerve, facial nerve, facial colliculus. Contributed by Chelsea Rowe
Figure
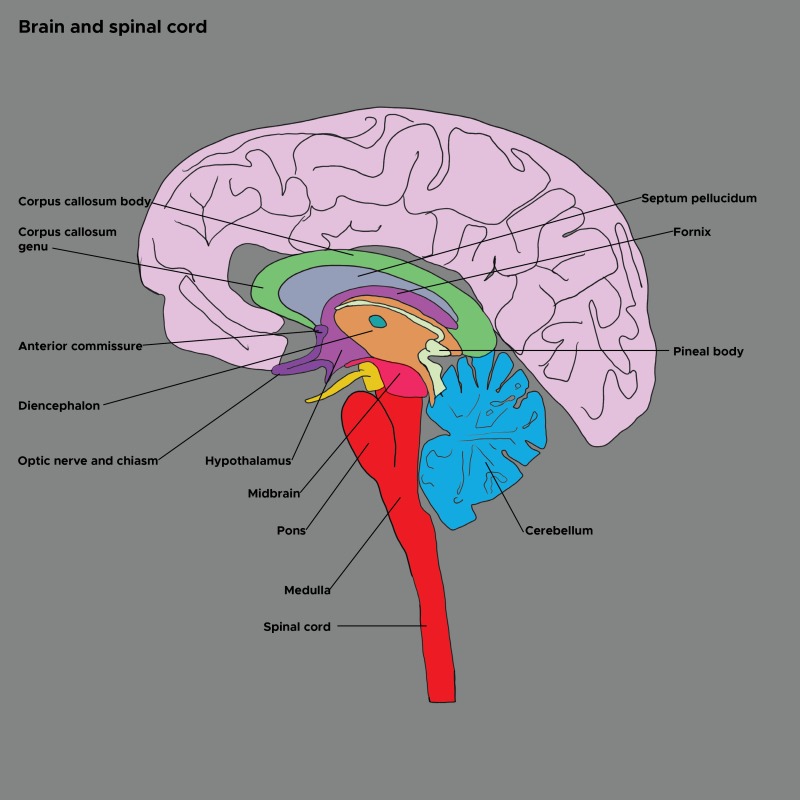
Illustration of the brain and spinal cord. Cerebellum, diencephalon, optic nerve, hypothalamus, midbrain, pons, medulla. Contributed by Chelsea Rowe
Figure
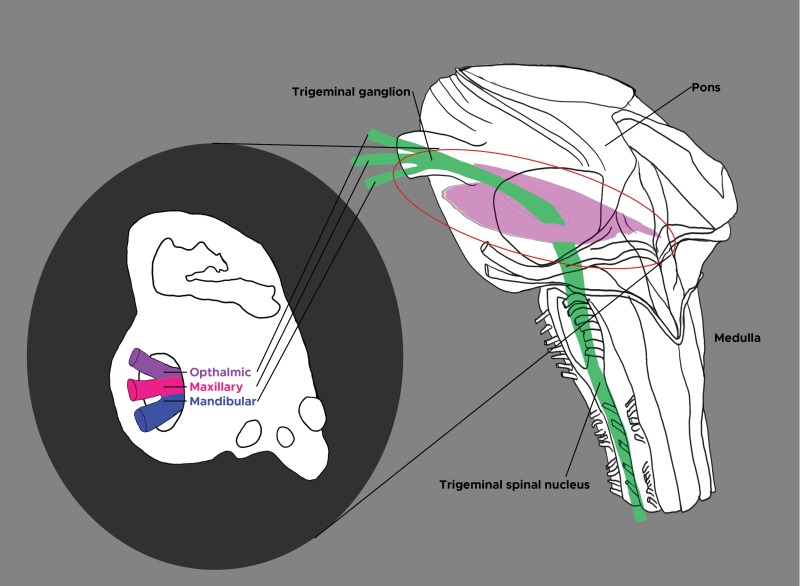
Trigeminal nucleus. Cross section of pons and medulla. Trigeminal ganglion, trigeminal spinal nucleus. Opthalmic, maxillary, and mandibular nerves. Contributed by Chelsea Rowe