Физика
Билет 1
- Основные положения МКТ:
1. Вещество состоит из частиц;
2. Эти частицы беспорядочно движутся;
3. Частицы взаимодействуют друг с другом. - Оценка размера молекулы: d(толщина слоя/размер молекулы)=V(объём слоя)/S(площадь поверхности).
- Масса молекул: m0=
1(грамм)/N(число молекул). - Диффузия – проникновение молекул одного вещества в межмолекулярное пространство другого вещества.
- Броуновское движение – это тепловое движение взвешенных в жидкости (или газе) частиц.
- В жидкостях существует так называемый ближний порядок, т. е. упорядоченное расположение молекул сохраняется на расстояниях, равных нескольким молекулярным диаметрам.
- Если соединить центры положений равновесия атомов или ионов твёрдого тела, то получится правильная пространственная решётка, называемая кристаллической.
Билет 2
- Один моль – это количество вещества, в котором содержится столько же молекул или атомов, сколько атомов содержится в углероде массой 0,012 кг.
- Постоянная Авагадро:


- Молярная масса M: масса вещества, взятого в количестве 1 моль.

Билет 3
Билет 4




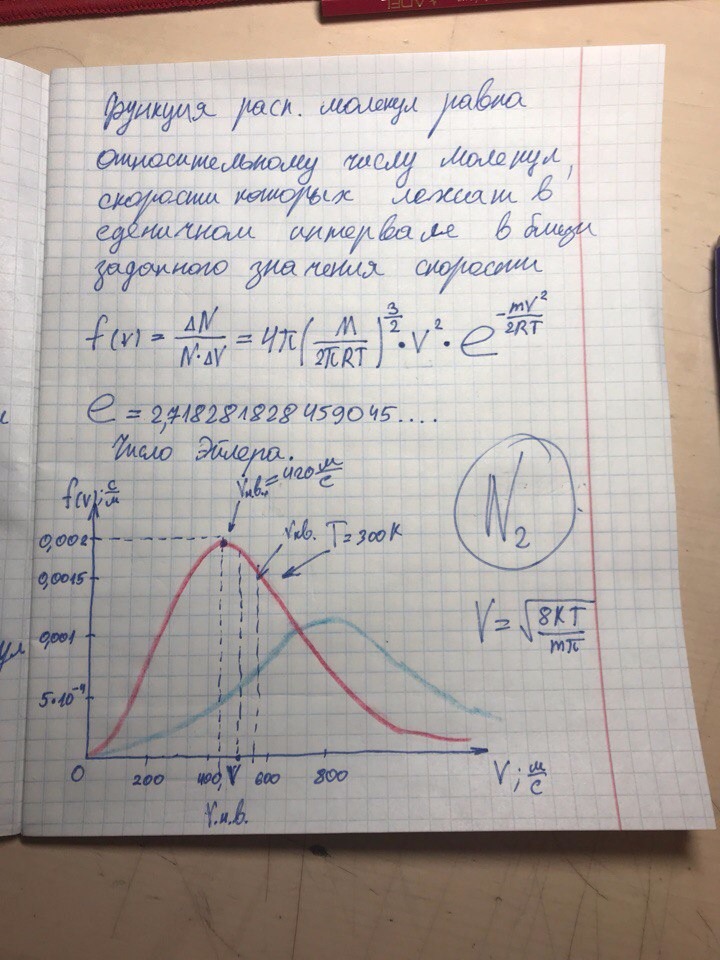
Билет 5
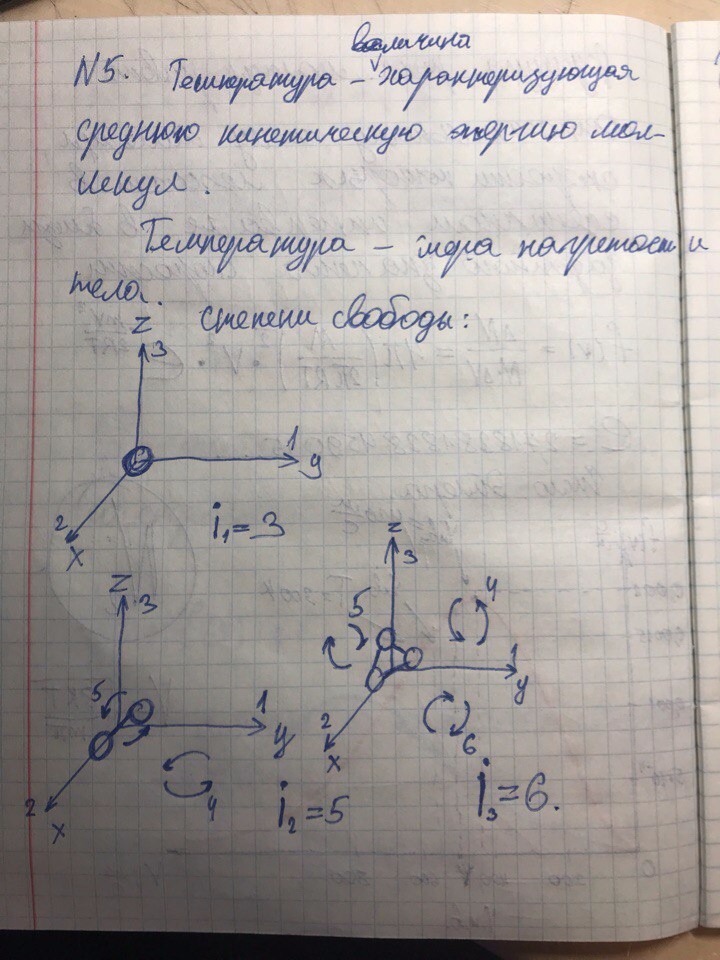

Билет 6


Билет 7
Билет 8
Билет 9
Билет 10
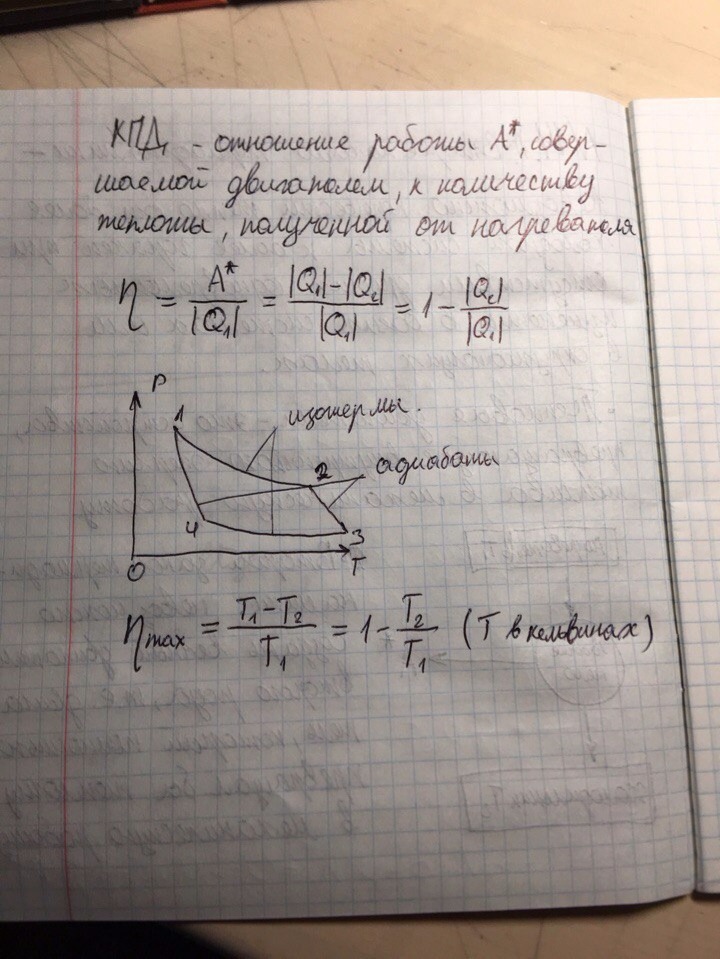
Первое начало термодинамики - количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы против внешних сил.
Внутренняя энергия тела (системы) - это сумма кинетической энергии хаотичного теплового движения молекул и потенциальной энергии их взаимодействия.

Вычисление работы:
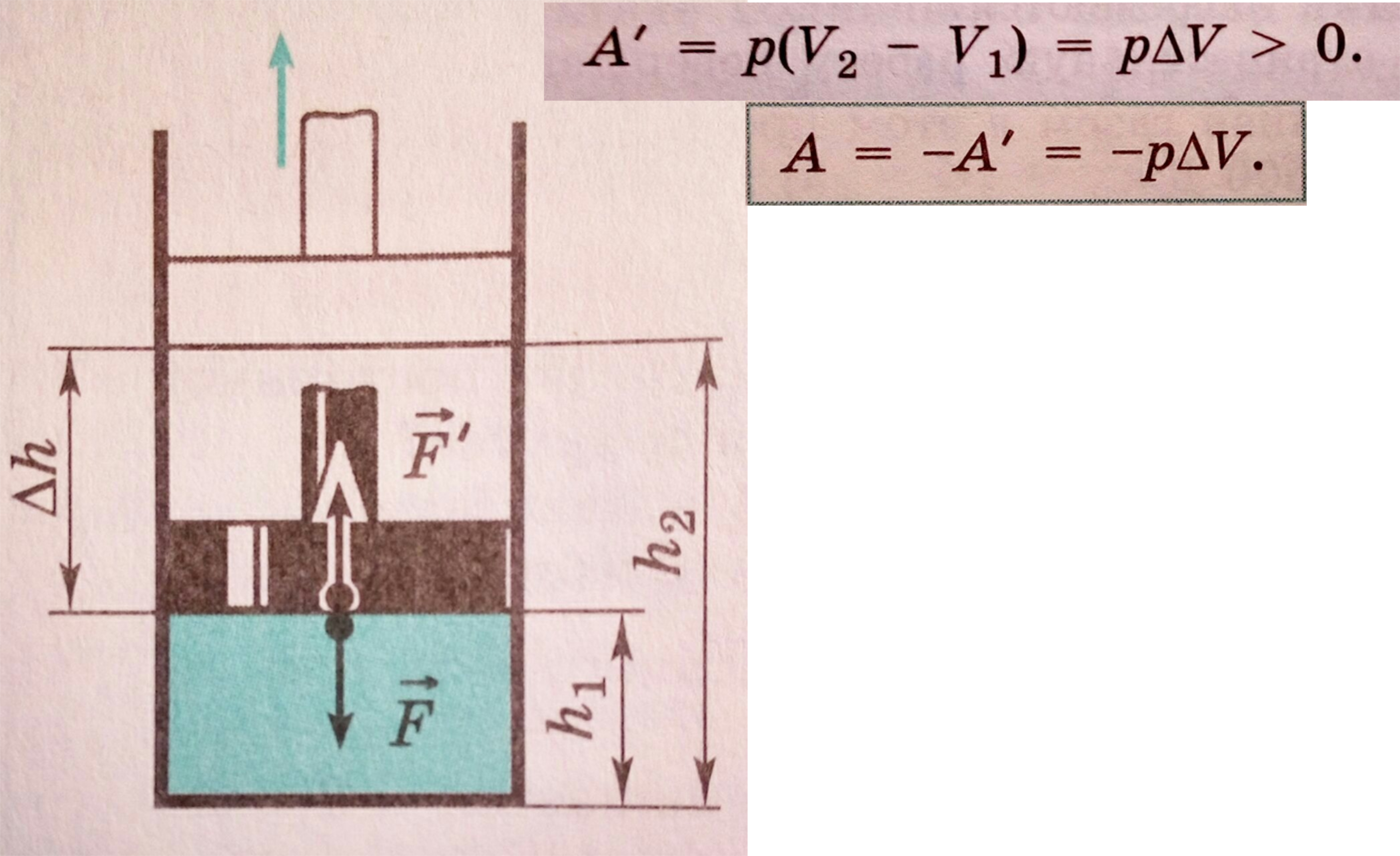

Теплообмен - процесс передачи энергии от одного тела другому без совершения работы.
Количество теплоты - количественная мера изменения внутренней энергии при теплообмене.
Билет 11

Билет 12
Билет 13
Билет 14
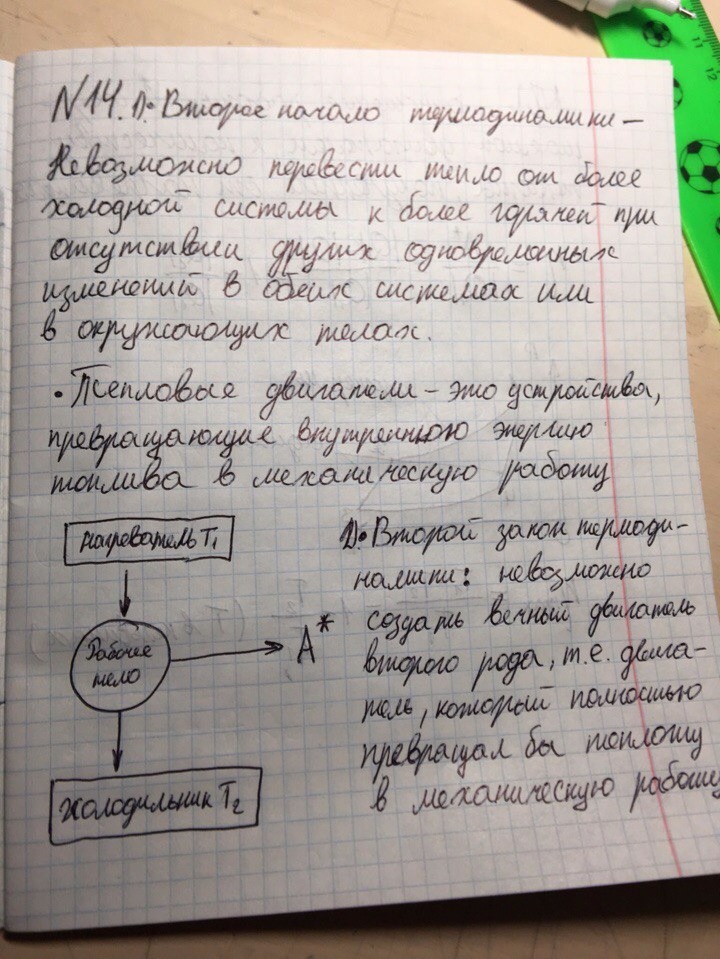
Билет 15

Билет 16
- Число молекул: N=V(объём капли)/V(объём на одну молекулу).
- Относительная молекулярная (атомная) масса вещества:

- Количество вещества:

- Молекула – это сложная система, состоящая из отдельных заряженных частиц: электронов и атомных ядер.
- Газы могут неограниченно расширяться. Они не сохраняют ни формы, ни объёма. Многочисленные удары молекул о стенки сосуда создают давление газа.
- Жидкости: малосжимаемы, текучи.
- Твёрдые тела сохраняют не только объём, но и форму.
- Если соединить центры положений равновесия атомов или ионов твёрдого тела, то получится правильная пространственная решётка, называемая кристаллической.
- Идеальный газ – это теоретическая модель газа, в которой не учитываются размеры молекул (они считаются материальными точками) и их взаимодействие между собой (за исключением случаев непосредственного столкновения).
- Скорости молекул беспорядочно меняются, но средний квадрат скорости вполне определённая величина.
- Основное уравнение молекулярно-кинетической теории газов:
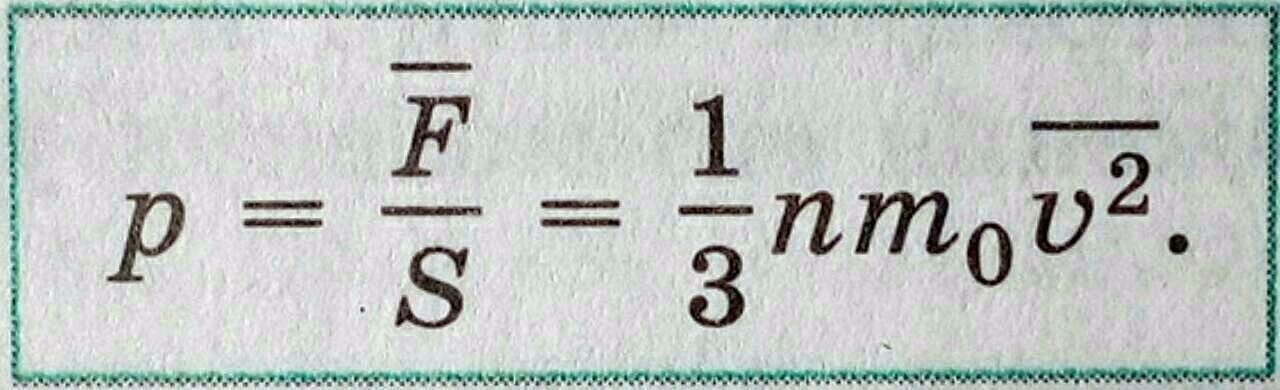
- В другом виде:

- Величины V, p, t, характеризующие состояние макроскопических тел без учёта их молекулярного строения, называют макроскопическими параметрами.
- Температура характеризует степень нагретости тела (холодное, тёплое, горячее).
- Тепловое равновесие – это состояние тела, при котором температура во всех точках системы одинакова.
- Температура характеризует состояние теплового равновесия системы тел: все тела системы, находящиеся друг с другом в тепловом равновесии, имеют одну и ту же температуру.