I. Клеточная биология
AndreyБЕЛКИ
Среди органических соединений клетки белки являются наиболее важными. Содержание белков в клетке колеблется от 50 % до 80 %.
Белки – это высокомолекулярные органические соединения, которые состоят из углерода, водорода, кислорода, серы и азота. В состав некоторых белков входит фосфор, а также катионы металлов.
Белки являются биополимерами, которые состоят из мономеров аминокислот. Их молекулярная масса варьируется от нескольких тысяч до нескольких миллионов, в зависимости от количества аминокислотных остатков.
В состав белков входит всего 20 типов аминокислот из 170, найденных в живых организмах.
Аминокислоты – органические соединения, в молекулах которых одновременно присутствует аминогруппа (-NH2) с основными свойствами и карбоксильная группа (-COOH) с кислотными свойствами. Часть молекулы, называемая радикалом (R), у разных аминокислот имеет различное строение.
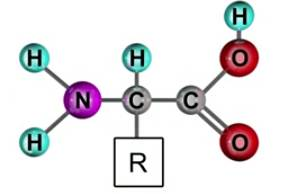
В зависимости от радикала аминокислоты делят на:
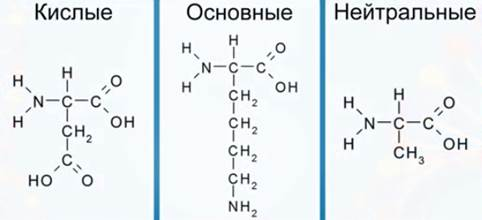
1. кислые (в радикале карбоксильная группа);
2. основные (в радикале аминогруппа);
3. нейтральные (не имеют заряженных радикалов).
Аминокислоты соединяются друг с другом посредством пептидной связи. Эта связь образуется путем выделения молекулы воды при взаимодействии аминогруппы одной аминокислоты с карбоксильной группой другой аминокислоты. Реакция, идущая с выделением воды, называется реакцией конденсации, а возникающая ковалентная азот-углеродная связь – пептидной связью.

Соединения, образующиеся в результате конденсации двух аминокислот, представляют собой дипептид. На одном конце его молекулы находится аминогруппа, а на другом – свободная карбоксильная группа. Благодаря этому дипептид может присоединять к себе другие молекулы. Если таким образом соединяется много аминокислот, то образуется полипептид.

Полипептидные цепи бывают очень длинными и могут состоять из различных аминокислот. В состав белковой молекулы может входить как одна полипептидная цепь, так и несколько таких цепей.
Многие животные, включая человека, в отличие от бактерий и растений не могут синтезировать все аминокислоты, которые составляют белковые молекулы. То есть существует ряд незаменимых аминокислот, которые должны поступать с пищей.
К незаменимым аминокислотам относятся: лизин, валин, лейцин, изолейцин, треонин, фенилаланин, триптофан, тирозин, метионин.
Ежегодно в мире производится более двухсот тысяч тонн аминокислот, которые используются в практической деятельности человека. Они применяются в медицине, парфюмерии, косметике, сельском хозяйстве.
В большей степени производят глутаминовую кислоту и лизин, а также глицин и метионин.
Назначение аминокислот
1. Глутаминовая кислота
Используется в психиатрии (при эпилепсии, для лечения слабоумия и последствий родовых травм), в комплексной терапии язвенной болезни и при гипоксии. Также она улучшает вкус мясных продуктов.
2. Аспарагиновая кислота
Аспарагиновая кислота способствует повышению потребления кислорода сердечной мышцей. В кардиологии применяют панангин – препарат, содержащий аспартат калия и аспартат магния. Панангин применяют для лечения различного рода аритмий, а также ишемической болезни сердца.
3. Метионин
Защищает организм при отравлениях бактериальными эндотоксинами и некоторыми другими ядами, в связи с этим используется для защиты организма от токсикантов окружающей среды. Обладает радиопротекторными свойствами.
4. Глицин
Является медиатором торможения в центральной нервной системе. Используется как успокаивающее средство, применяется при лечении хронического алкоголизма.
5. Лизин
Основная пищевая и кормовая добавка. Используется в качестве антиоксидантов в пищевой промышленности (предотвращает порчу пищевых продуктов).
Пептиды
Отличие между белками и пептидами заключается в количестве аминокислотных остатков. В белках их более 50, а в пептидах менее 50.
В настоящее время выделено несколько сотен различных пептидов, которые выполняют в организме самостоятельную физиологическую роль.
К пептидам относятся:
1. Пептидные антибиотики (грамицидин S).
2. Регуляторные пептиды – вещества, регулирующие многие химические реакции в клетках и тканях организма. К ним относятся: пептидные гормоны (инсулин), окситоцин, стимулирующий сокращение гладкой мускулатуры.
3. Нейропептиды.
Классификация белков
В зависимости от строения различают простые и сложные белки.
1. Простые белки состоят только из белковой части.
2. Сложные имеют небелковую часть.
Если в качестве небелковой части используется углевод, то это гликопротеиды.
Если в качестве небелковой части используются липиды, то это липопротеиды.
Если в качестве небелковой части используются нуклеиновые кислоты, то это нуклеопротеиды.
Структуры белка
Белки имеют 4 основных структуры: первичную, вторичную, третичную, четвертичную.

1. Под первичной структурой понимают последовательность аминокислотных остатков в полипептидной цепи. Она уникальна для любого белка и определяет его форму, свойства и функции.
Значительное совпадение первичной структуры характерно для белков, выполняющих сходные функции. Замена всего лишь одной аминокислоты в одной из цепей может изменить функцию молекулы белка. Например, замена глутаминовой кислоты на валин приводит к образованию аномального гемоглобина и к заболеванию, которое называется серповидноклеточная анемия.
2. Вторичная структура – упорядоченное свертывание полипептидной цепи в спираль (имеет вид растянутой пружины). Витки спирали укрепляются водородными связями, возникающими между карбоксильными группами и аминогруппами. Практически все СО- и NН-группы принимают участие в образовании водородных связей.
3. Третичная структура – укладка полипептидных цепей в глобулы, возникающая в результате возникновения химических связей (водородных, ионных, дисульфидных) и установления гидрофобных взаимодействий между радикалами аминокислотных остатков.
4. Четвертичная структура характерна для сложных белков, молекулы которых образованы двумя и более глобулами.
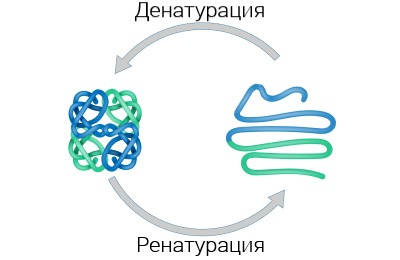
Утрата белковой молекулой своей природной структуры называется денатурацией. Она может возникнуть при воздействии температуры, химических веществ, при нагревании и облучении.
Если при денатурации не нарушены первичные структуры, то при восстановлении нормальных условий белок способен воссоздать свою структуру. Этот процесс носит название ренатурация. Следовательно, все особенности строения белка определяются первичной структурой.
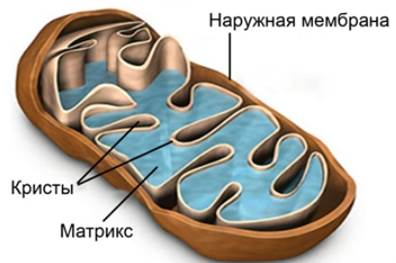
Митохондрии
Митохондрии имеются во всех эукариотических клетках. Они участвуют в процессах клеточного дыхания и запасают энергию в виде макроэргических связей молекулы АТФ, то есть в доступной форме для большинства процессов, связанных с затратой энергии в клетке.
Впервые митохондрии в виде гранул в мышечных клетках наблюдал в 1850 г. Р. Кёлликер (швейцарский эмбриолог и гистолог). Позднее, в 1898 г., Л. Михаэлис (германский биохимик и химик-органик) показал, что они играют важную роль в дыхании.

Число митохондрий в клетках не постоянно, оно зависит от вида организма и типа клетки. В клетках, потребность которых в энергии велика, содержится много митохондрий (в одной печеночной клетке их может быть около 1000), в менее активных клетках митохондрий гораздо меньше. Чрезвычайно сильно варьируются также размеры и формы митохондрий. Они могут быть спиральными, округлыми, вытянутыми и разветвленными. Их длина колеблется от 1,5 мкм до 10 мкм, а ширина – от 0,25 до 1 мкм. В более активных клетках митохондрии крупнее.
Митохондрии способны изменять свою форму, а некоторые могут перемещаться в более активные участки клетки. Такое перемещение способствует накоплению митохондрий в тех местах клетки, где выше потребность в АТФ.
Каждая митохондрия окружена оболочкой, состоящей из двух мембран. Наружную мембрану отделяет от внутренней небольшое расстояние (6-10 нм) – межмембранное пространство. Внутренняя мембрана образует многочисленные гребневидные складки – кристы. Кристы существенно увеличивают поверхность внутренней мембраны. На кристах происходят процессы клеточного дыхания, необходимые для синтеза АТФ. Митохондрии являются полуавтономными органеллами, содержащими компоненты, которые необходимы для синтеза собственных белков. Внутренняя мембрана окружает жидкий матрикс, в котором находятся белки, ферменты, РНК, кольцевые молекулы ДНК, рибосомы.
Пластиды
Пластиды характерны исключительно для растительных клеток. Каждая пластида состоит из оболочки, состоящей из двух мембран. Внутри пластиды можно наблюдать сложную систему мембран и более или менее гомогенное вещество – строму. Пластиды являются полуавтомными органеллами, так как содержат белоксинтезирующий аппарат и могут частично обеспечить себя белком.
Пластиды обычно классифицируют на основании содержащихся в них пигментов. Различают три типа пластид.
1. Хлоропласты – это пластиды, в которых протекает фотосинтез. Они содержат хлорофилл и каротиноиды. Обычно хлоропласты имеют форму диска диаметром 4-5 мкм. В одной клетке мезофилла (середина листа) может находиться 40-50 хлоропластов, а в квадратном миллиметре листа – около 500 000.

Внутренняя структура хлоропласта сложная. Строма пронизана развитой системой мембран, имеющих форму пузырьков – тилакоидов. Тилакоиды образуют единую систему. Как правило, они собраны в стопки – граны, напоминающие столбики монет. Тилакоиды отдельных гран связаны между собой тилакоидами стромы, или ламеллами. Хлорофиллы и каротиноиды встроены в тилакоидные мембраны. В строме хлоропластов находятся кольцевые молекулы ДНК, РНК, рибосомы, белки, липидные капли. Там же происходят первичные отложения запасного полисахарида – крахмала, в виде крахмальных зерен.

Крахмальные зерна – это временные хранилища продуктов фотосинтеза. Они могут исчезнуть из хлоропластов, если поместить растение на 24 часа в темноту. Появятся они снова через 2-3 часа, если вынести растение на свет.
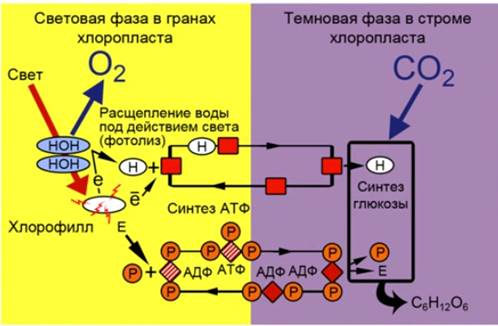
Как известно, фотосинтез делится на две фазы: световую и темновую. Световая фаза происходит на тилакоидах мембраны, а темновая – в строме хлоропласта.
2. Хромопласты – пигментированные пластиды. Они не содержат хлорофилл, но содержат каротиноиды, которые окрашивают плоды, цветки, некоторые корни и старые листья в красные, желтые и оранжевые цвета.
Хромопласты могут образовываться из хлоропластов, которые при этом теряют хлорофилл и внутренние мембранные структуры и начинают синтезировать каротиноиды. Такое происходит при созревании плодов.

3. Лейкопласты – непигментированные пластиды. Некоторые из них могут накапливать крахмал, например амилопласты, другие могут синтезировать и накапливать белки или липиды.
На свету лейкопласты могут превращаться в хлоропласты. Так, например, происходит с клубнем картофеля, который содержит много лейкопластов, накапливающих крахмал. Если вынести клубень картофеля на свет, он позеленеет.
