Талантливая молекула. Многогранный креатинфосфат
https://t.me/medach
Креатинфосфат (КрФ), он же креатинфосфорная кислота, он же фосфокреатин - высокоэнергетическое соединение, представляющее собой фосфорилированную форму азотистой кислоты – креатина (Кр), одного из важнейших метаболитов в биоэнергетической системе человека. Говоря о химизме креатинфосфата (рис. 1), его синтезе, накоплении и реализации его функций, всегда следует учитывать взаимозависимость фосфокреатина со своим предшественником – креатином (рис. 2), что дает основания утверждать о наличии цельной креатин-креатинфосфатной системы.

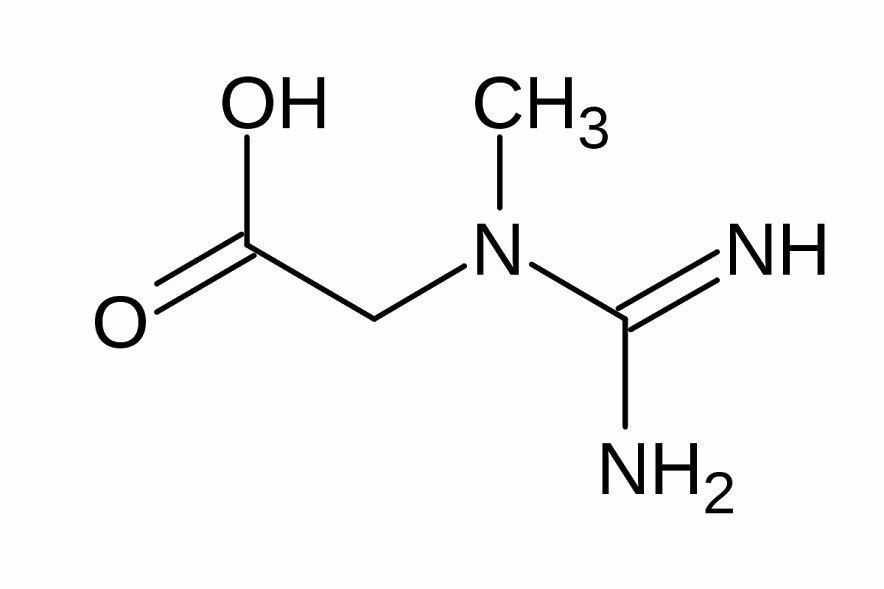
Метаболизм креатина и креатинфосфата, их взаимные превращения, непосредственно связаны с работой адениловой системы , и как следствие, со всеми основными элементами энергообеспечения организма. Однако, участие креатин-креатинфосфатной системы (Кр-КрФ) в биохимических превращениях не ограничивается рамками энергетического обмена. Далее будут рассмотрены отдельные элементы данной системы в ключе их совместной работы.
Общие сведения о креатине и фосфокреатине.
Органическая азотистая кислота креатин синтезируется в печени, почках и в небольших количествах в поджелудочной железе, при непосредственном участии трех аминокислот: заменимой- глицина и двух незаменимых- аргинина и метионина. Синтез (рис. 3) регулируется влиянием следующих ферментов: глицин-амидинотрансферазы ( перенос гуанидиновой группы от аргинина на глицин с образованием L-орнитина), метионин-аденозил трансферазы (образование активной формы метионина- S-аденозилметионина (SAM)из метионина и аденозина) и гуанидинацетат-метилтрансферазы.

Синтезированный креатин разносится кровотоком, в основном накапливаясь в предъявляющих высокие энергетические требования органах и тканях, таких как мышечные волокна и головной мозг. Основным депо Кр и КрФ являются скелетные мышцы, где концентрация этих веществ достигает 30 ммоль/г.
Количество креатина, образующегося ежесуточно в организме, находится в зависимости от ряда биологических и физиологических факторов (пол, возраст, специфическая тренированность, количество мышечной ткани и тд.) и колеблется от 1 до 2 г. Общее количество креатина (включающее обе формы в соотношении Кр и КрФ- 40:60 ) составляет 100-160 г у взрослого человека.
Фосфокреатин является продуктом обратимой реакции (рис. 4) фосфорилирования креатина, регулируемой креатинкиназой (креатинфосфокиназой)- ферментом, имеющим несколько изоферментных форм (табл. 1), из которых наибольшее биологическое значение имеют 3: креатинкиназа миокарда (КК-МВ), мозговая креатинкиназа (КК- ВВ) и самая распространенная- мышечная креатинкиназа (КК-ММ). Основная активность каждого из этих изоферментов происходит в соответствующих тканях и органах, и их концентрация в крови имеет особенное клиническое значение при лабораторной диагностике широкого спектра патологических состояний(инфаркт миокарда, ишемические повреждения головного мозга, разрушения структуры мышечных волокон и тд.).


Конечным продуктом метаболизма креатина и фосфокреатина в ходе необратимой химической реакции (рис. 5) является креатинин, который попадая в кровь затем проходит клубочковую фильтрацию в почках и выводится с мочой. Креатинин в анализе мочи также является значимым параметром при анализе функции мочевыделительной системы в целом и почек в частности. Данный показатель, как и цифры содержания креатина и креатинкиназы, рассматриваются в составе общего и специализированного биохимического анализа крови. Их средние значения приведены в таблице 2.


Особенностью превращения Кр и Крф в креатинин является отсутствие регулирующего фермента, что обеспечивает относительное постоянство уровня интенсивности реакции образования креатинина, а это в свою очередь обуславливает стабильную скорость распада креатина и креатинфосфата в течение суток на отметке в среднем 1-2 г. Значительное увеличение количества креатинина в моче при нормальном статусе возможно при использовании экзогенных пищевых добавок на основе Кр и КрФ.
Биологическая роль креатина и фосфокреатина.
С 20-х годов ХХ века, когда был открыт креатинфосфат и началась новая эпоха в изучении высокоэнергетических фосфатов и их роли в энергетическом обмене, звенья креатин-креатинфосфатной системы продолжают расширять список своих прикладных свойств. На данный момент многочисленные фундаментальные биохимические и физиологические исследования, как и данные полученные в ходе фокусных клинических разработок позволяют уверенно говорить о следующих функциях Кр и КрФ:
- участие в энергообеспечении мышечной работы в анаэробном режиме за счет непосредственного участия в сокращении миофибрилл (классическое понятие о креатинфосфатной системе ресинтеза АТФ);
- стимуляция окислительного фосфорилирования за счет работы в митохондриях так называемого креатинфосфатного челнока (или шаттла);
- регуляция водно-солевого обмена за счет способности удерживать воду в клетках мышечной ткани;
- кардиопротективное и общее защитное действие креатинфосфата для других типов клеток с помощью его способности к стабилизации клеточных мембран;
- регуляция работы адениловой системы с помощью воздействия на
концентрацию АДФ в митохондриях и цитоплазме миофибрилл
Креатинфосфатный анаэробный ресинтез АТФ выходит на первый план при высокоинтенсивной работе короткой продолжительности (до 10 сек.), когда эффективность дыхательной цепи недостаточна из-за долгого времени активации, либо за счет нарастания кислородного долга, а скорость гликолитического расщепления снижается вследствие истощения субстратов или ферментной базы. Так как все превращения Кр и КрФ регулируются только одним ферментом (креатинкиназой), это существенно снижает время необходимое для выхода на максимальные параметры работы анаэробно-алактатной системы. Отсутствие образования молочной кислоты и ее солей, что позволяет избавиться от закисления мышечных волокон, при таком типе энергообеспечения является еще одним положительным моментом в использовании Кр и КрФ как биоэнергетического агента. Существуют углубленные исследования более тонких механизмов влияния этих метаболитов на уровень pH мышечной ткани (в том числе миокарда), головного мозга и крови, однако формирование единой согласованной теории пока не произошло.
Креатинфосфатный шаттл (рис. 6) не только обеспечивает перенос органического фосфата от АТФ, которая не может самостоятельно покинуть матрикс митохондрий, до работающих миофибрилл, но и стимулирует работу дыхательной цепи. Это происходит за счет функционирования креатинкиназы на внутренней мембране митохондрий. Образовавшаяся вследствие реакции фосфорилирования креатина молекула АДФ поступает обратно в матрикс и стимулирует реакции окислительного фосфорилирования за счет изменения соотношения АТФ/АДФ. Таким образом Кр и КрФ имеют выраженное влияние на энергообеспечение не только в рамках анаэробных реакций но и при эробном ресинтезе АТФ.

Удержание молекул воды внутри клеток за счет присутствия креатина и креатинфосфата и их влияния на ионы Na не носит выраженного характера при исключительно эндогенном получении организмом этих метаболитов.
Взаимодействие креатинфосфата с клеточными мембранами обусловлено его химическим строением (рис. 1). Амфипатические свойства фосфокреатина, выраженные в наличие свободных ионных связей разной направленности, позволяют КрФ связывать с полярными фосфолипидными головками мембраны и таким образом стабилизировать весь поверхностный аппарат клетки. За счет этого стабилизирующего действия фосфокреатина вся клетка становится более устойчива к разрушению, вызванному различными факторами, такими как рост осмотического давления или присутствию цитотоксических агентов. На тканевом уровне это выражается в противоишемическом и антитоксическом действии креатинфосфата на клетки скелетной и сердечной мышечной ткани, а также на клетки головного мозга.

Способность регулировать постоянную концентрацию АДФ позволяет креатинфосфату поддерживать устойчивое состояние всей адениловой системы. Присутствие высокого уровня КрФ в клетках с высоким потреблением энергии снижает активность фермента аденилатдезаминазы, который участвует в расщеплении АМФ до мочевой кислоты. Активность этого фермента находится в тесной обратной зависимости от концентрации АДФ. Таким образом, фосфорилируя АДФ до АТФ, фосфокреатин повышает вероятность повторного включения всех элементов адениловой системы в цикл обмена фосфатами и уменьшает образование вредных продуктов обмена.
Очевидно, что Кр и КрФ являясь высокоэнергетическими биологически активными соединениями, участвуют в широком спектре жизненно необходимых реакций и процессов человеческого организма, оставаясь стабильной формой хранения и доставки энергии, а также универсальным клеточным протектором.
Источники:
- Северин Е. С. Биологическая химия. – 2008.
- Nelson D. L. i Cox, MM " Lehninger Principles of Biochemistry"(2013). – 2013.
- Bessman S. P., Carpenter C. L. The creatine-creatine phosphate energy shuttle //Annual review of biochemistry. – 1985. – Т. 54. – №. 1. – С. 831-862.
- Cooper R. et al. Creatine supplementation with specific view to exercise/sports performance: an update //Journal of the International Society of Sports Nutrition. – 2012. – Т. 9. – №. 1. – С. 33.
- Gaddi A. V., Galuppo P., Yang J. Creatine Phosphate Administration in Cell Energy Impairment Conditions: A Summary of Past and Present Research //Heart, Lung and Circulation. – 2017.